
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Корозія металів
|
|
Корозією зазвичай називають мимовільне руйнування металів у результаті їхньої хімічної й електрохімічної взаємодії із зовнішнім середовищем та перетворення їх у стійкі сполуки (оксиди, гідроксиди, солі).
Власне кажучи, корозія являє собою сукупність окисно-відновних процесів, які відбуваються при контакті металів з агресивним середовищем, що призводить до руйнування металевих виробів. Під агресивним середовищем мають на увазі окисну атмосферу (присутність кисню в атмосфері Землі робить її окисною), особливо в присутності води або розчинів електролітів.
За механізмом процесу розрізняють хімічну та електрохімічну корозію металів. Хімічна корозія являє собою звичайну хімічну реакцію між атомами металів і різних окисників. Прикладами хімічної корозії є високотемпературне окиснення металів киснем, окиснення поверхні алюмінію на повітрі, взаємодія металів із хлором, сіркою, сірководнем H2S тощо.
Електрохімічна корозія протікає в розчинах, тобто, в основному, при контакті металів з розчинамиелектролітів, особливо у тих випадках, коли метали перебувають у контакті з менш активними металами. Швидкість корозії істотно залежить від активності металів, а також від концентрації й природи домішок у воді. У чистій воді метали майже не піддаються корозії, а в контакті з більш активними металами навіть у розчинах електролітів не кородують.
Сумарне рівняння реакції корозії заліза можна записати так:
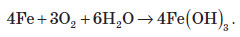
На сьогодні існує кілька способів запобігання корозії.
Відокремлення металу від агресивного середовища — фарбування, змащування маслами, покриття неактивними металами або емаллю (І). Приведення поверхні металів у контакт із більш активними металами (ІІ). Використання речовин, що сповільнюють корозію (інгібітори корозії), та сплавів, стійких до корозії (ІІІ).
I. Найпростіший спосіб захистити сталь від корозії — це ізолювати метал від атмосферного повітря. Це можна зробити за допомогою масляного, жирового змащування або нанесення захисного шару фарби.
Зараз широко застосовують захисні покриття з органічних полімерів. Покриття можна робити різних кольорів, і це досить гнучке розв’язання проблеми корозії. Навіть побіжний погляд на речі, які оточують нас у побуті, дає масу прикладів такого розв’язання: холодильник, сушарка для посуду, піднос, велосипед тощо.
II. Іноді залізо покривають тонким шаром іншого металу. Деякі виробники виготовляють кузовиавтомобілів зі сталі з гальванічним цинковим покриттям. При такій обробці утворюється міцно зчеплений з основою шар цинк оксиду, і якщо гальванічне покриття не ушкоджене, воно добре захищає від іржі.
Дуже розповсюдженим розв’язанням проблеми захисту від корозії є використання іржостійкихсплавів. Багато зі сталевих виробів, використовуваних у побуті, особливо ті, що перебувають у постійному контакті з водою: кухонний посуд, ложки, виделки, ножі, бак пральної машини тощо — виготовлені з іржостійкої сталі, яка не вимагає додаткового захисту.
Сплави
Сплав — це суміш металу з одним або кількома компонентами. Компоненти змішують при плавці; при застиганні матеріалу утворюється однорідний твердий матеріал. Через присутність інших хімічних елементів у складі сплавів властивості металів змінюються, і часто новий матеріал стає більш міцним.
Найпоширеніші сплави — це чавун і сталь. Обидва ці сплави є сплавами на основі заліза. Головна відмінність між ними — це вміст вуглецю. Якщо вміст вуглецю перевищує 4 %, то такий сплавназивають чавуном. Якщо ж вміст вуглецю менший 4 %, то такий сплав називають сталлю. Вміст вуглецю в цих сплавах посутньо впливає на їхні фізичні властивості. Якщо чавун є твердим і крихким, то, на відміну від нього, сталь являє собою більш м’який і пластичний сплав. Окрім того, до складу сталі додають ще деякі інші метали задля добування сталі з необхідними характеристиками.
Так, додавання до сталі марганцю підвищує її зносостійкість, що дозволяє використовувати її длявиготовлення залізничних рейок. А додавання хрому збільшує стійкість до корозії; таку сталь називають іржостійкою.
Як сировину для виробництва чавуну використовують залізну руду, що складається з оксидів Феруму, найчастіше Fe2O3. Вона містить також порожню породу, до складу якої входять сполуки Силіцію (SiО2), Мангану (MnО2), Алюмінію (Аl2О3), Фосфору (Ca3(PO4)2), Сульфуру (FeS2, CaSO4) та ін.
У доменній печі протікає величезна кількість реакцій, які поділяють на кілька груп.
1-ша група реакцій.
Горіння коксу й утворення відновника — карбон (II) оксиду. Сьогодні в домни, окрім повітря, надходить природний газ, який інтенсифікує процес плавки й дозволяє зменшувати ви трату дорогого коксу:
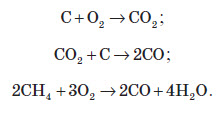
2-га група реакцій.
Відновлення ферум (III) оксиду карбон (II) оксидом протікає трьома послідовними стадіями:
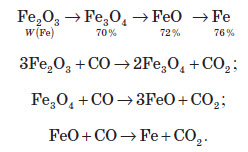
3-тя група реакцій.
Відновлення домішок. Завдяки цій групі реакцій багато елементів порожньої породи переходять у чавун:
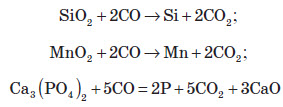
Частина Сульфуру з природних сполук переходить у чавун у вигляді сполуки FeS, а частина — в сірчистий газ SO2, який виходить із доменної печі в суміші з іншими газами, а потім уловлюється.
4-та група реакцій.
Утворення чавуну найчастіше описують за допомогою рівняння реакції між залізом та коксом, а також між залізом та чадним газом:
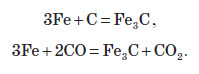
5-та група реакцій.
Утворення шлаку відбувається в такий спосіб. Флюси під впливом високих температур розкладаються з утворенням реакційноздатних основних оксидів СаО та MgО. Вони реагують із тими компонентами порожньої породи, які мають кислотні або амфотерні властивості, наприклад із SiО2 та Аl2О3.
Утворювані в процесі плавки силікати, алюмосилікати, алюмінати, деякі сульфіди утворюють побічний продукт доменного виробництва — шлак. Він відзначається невеликою густиною й тому накопичується на поверхні чавуну, запобігаючи його окисненню.