
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Физическая поглотительная способность.
|
|
Физическая поглотительная способность — способность почвы поглощать из раствора целые молекулы растворенных минеральных и органических веществ и молекул воды.
Физическая поглотительная способность почвы зависит от гранулометрического, минералогического состава, а также гумусности почв.
Песчаные и малогумусные почвы обладают пониженной адсорбционной способностью в сравнении с глинистыми и высокогумусными.
С увеличением содержания гидратов железа и алюминия, как и минералов монтмориллонитовой группы, активность почв к поглощению повышается.
Физико-химическая поглотительная способность (полярная адсорбция). Физико-химическая (обменная) поглотительная способность, или коллоидно-химическая адсорбция, обусловлена наличием на поверхности коллоида электрического заряда.
Так как в почве преобладают отрицательно заряженные коллоиды (ацидоиды), то сильнее выражена способность почвы к обменному поглощению катионов, нежели анионов
2.Почвенные коллоиды
Поглотительная способность почвы неразрывно связана с наличием в ней высокодисперсных частиц—коллоидов, учение о которых создавалось в первой четверти 20 век.
В состав почвенной массы входят частицы самых разных размеров. Самые мелкие из них, размерами от 0, 2 до 0.001 мкм относятся к коллоидам.
Почвенные коллоиды образуются в процессе выветривания и почвообразования, в результате дробления крупных частиц, или путем соединения молекулярно раздробленных веществ и подчиняются законам, установленным для таких систем в физической и коллоидной химии.
В почвах коллоиды образуют двухфазную систему, состоящую из дисперсной фазы (твердые коллоидные частицы) и дисперсионной среды (почвенный раствор). Высокодисперсные системы по величине частиц делятся на три группы.
Таблица 1.Классификация высокодисперсионных систем почвы
| Предколлоидные системы | Коллоидные системы | Молекулярные растворы |
| диаметр частиц I мкм-100 нм | диаметр частиц 100-1 нм | диаметр частиц < 1 нм |
Коллоиды в почвах представлены сложной системой минеральных, органических и органоминеральных соединений. В большинстве почв преобладают минеральные коллоиды, на долю которых приходится 85—90% их общей массы.
К минеральным относятся глинистые минералы (каолинит, монтмориллонит, галлуазит, гидрослюда, иллит, вермикулит и др.); гидроксиды железа, алюминия, марганца, кремния и их комплексные соли — коагели.
К органическим относятся гумусовые вещества, их соли, (гуматы, фульваты), некоторые полисахариды.
Органо-минеральные коллоиды широко распространены в верхних горизонтах всех почв. Они представляют собой сложные образования высокодисперсных минералов и гумусовых веществ.
Основными минералами, входящими в состав этих коллоидов, являются монтмориллонитовая и гидрослюдистая группы, а также всегда сопутствующие им в почве полуторные окислы и кремнезем, в меньшей степени распространено участие в их образовании каолинитовых минералов.
Формируются эти коллоиды в почве в процессе склеивания (адгезии) гумусовых кислот и их производных с поверхностью минеральной частицы, вследствие чего вещества минеральной природы в них преобладают.
В любой почве основная масса коллоидов находится в форме гелей, различных по степени гидратации и прочности связи с поверхностью твердых частиц.
Часть коллоидов находится в почве в свободном состоянии,
часть образует пленки на поверхности более крупных гранулометрических фракций, сильно дегидратирована.
Первая категория коллоидов легко пептизируется при щелочной реакции и насыщении их диффузного слоя натрием.
Вторая категория очень прочно связана с поверхностью крупных гранулометрических фракций, и их пептизация затруднена.
Основное свойство коллоидов — способность к поглощению веществ из растворов как в виде молекул, так и в виде ионов.
Поглощенные вещества могут обмениваться на другие, находящиеся в растворе, т.е. коллоиды обусловливают поглотительную и обменную способность почв.
Это свойство определяется высокой реакционной способностью, обусловленной большой суммарной и удельной поверхностью, которая тем больше, чем выше дисперсность коллоидов (табл. 2). Если в почве содержится 10% коллоидных частиц, то сумма их поверхности на площади 1 га составит 70 тыс. га.
С увеличением суммарной поверхности растет суммарная поверхностная энергия и возрастает химическая активность коллоидов.
Удельная поверхность выше в суглинистых почвах, чем в песках и супесях, и выше в гумусовом горизонте, чем в нижележащих.
Таблица 2
Роль частиц различного размера в формировании общей поверхности среднесуглинистой почвы
| Размер частиц, мм | Содержание. % к массе | Поверхность, м2 на 1 г почвы | Доля общей поверхности, % |
| 0, 25-0, 05 | 0, 5 | 0, 2 | |
| 0, 05-0, 01 | 4, 1 | 1.7 | |
| 0, 01-0, 005 | 9, 9 | 4, 1 | |
| 0, 005-0, 001 | 12, 7 | 5, 2 | |
| 0, 001-0, 0001 | 18, 8 | 7, 8 | |
| 0, 0001 | 194, 0 | 81, 0 | |
| Сумма | 240.0 | 100, 0 |
Коллоид имеет сложное строение.
Внутренняя часть, состоящая из агрегатов аморфного или кристаллического вещества разного химического состава, называется ядром (рис.1).
На его поверхности расположен слой прочно удерживаемых потенциалопределяющих ионов, которые вместе с ядром образуют гранулу.
Вокруг гранулы двумя слоями располагаются ионы противоположного (компенсирующего) заряда.
К грануле примыкает слой неподвижных противоионов, прочно удерживаемых электростатическими силами ионов потенциалопределяюшего слоя, образуя вместе с гранулой частицу.
Часть противоионов удалена от частицы, их связь с ней по мере удаления уменьшается. Это диффузный слой, ионы которого способны к эквивалентному обмену на ионы того же заряда из дисперсионной среды и вместе с частицей образуют коллоидную мицеллу.
Свободный электрический заряд коллоидной частицы (дзета-потенциал) — разность потенциалов вследствие удаления частиц противоионов от границы компенсирующего слоя к внешней границе диффузного слоя, колеблется от 0 до 40—60 мВ. Коллоидная мицелла электронейтральна при дзета-потенциале, равном нулю, что является изоэлектрической точкой коллоида.
Заряд коллоида появляется в связи с нарушением равновесия между зарядами, расположенными на поверхности раздела твердая частица — раствор, а также в связи с изменением химического состава и структуры коллоидного вещества.
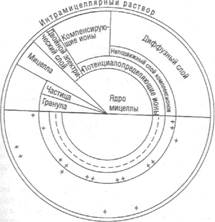
Рис.1. Схема строения коллоидной мицеллы (по Н. И. Горбунову
Классификация коллоидов в зависимости от заряда ионов потенциал -определяющего слоя.
В зависимости от заряда ионов потенциал - определяющего слоя коллоиды делятся на
ацидоиды — отрицательно заряженные,
базоиды — положительно заряженные и
амфолитоиды, которые в кислой среде имеют положительный заряд, в шелочной — отрицательный.
К ацидоидам относятся глинистые минералы, гидроксиды кремния и марганца, гумусовые кислоты и органоминеральные коллоиды.
В качестве базоидов в кислой среде выступают гидроксиды железа и алюминия, белки, тела мелких бактерий, которые в щелочной среде имеют свойства ацидоидов.
Коллоиды в почве могут находиться в состоянии геля (коллоидный осадок) или золя (коллоидный раствор).
Золь может переходить в гель – процесс называется коагуляцией.
Коагуляция может происходить при встрече разнозаряженных коллоидных частиц, которые, соединяясь друг с другом, образуют коагелъ.
Гель может переходить в золь.
Это — пептизация. При прочих равных условиях она происходит при уменьшении концентрации солей в растворе.
Переход коллоидов из одного состояния в другое обусловлен изменением электрического потенциала коллоидных частиц и зависит от степени их гидратации.
Коллоиды, легко переходящие из геля в золь, называются обратимыми.
Обратимыми являются гидрофильные коллоиды, насыщенные высокогидратированными одновалентными катионами,
необратимыми — гидрофобные коллоиды, насыщенные двух-и особенно трехвалентными катионами с низкой степенью гидратации (низкой обводненностью).
Особым видом коагуляции является тиксотропия: когда масса геля неотделима от золя, образуется студень, который можно превратить в состояние золя при механическом воздействии.
Тиксотропия распространена в почвах, образующихся под воздействием вечной мерзлоты.
От состава и свойств коллоидов зависит поглотительная способность почвы.
В почве под влиянием различных факторов — периодическое высушивание, нагревание, увлажнение, промораживание, изменение реакции среды и др. — происходит изменение вновь образующихся при выветривании и почвообразовании органических минеральных коллоидов.
Одним из таких изменений является процесс старения коллоидов, под которым понимается самопроизвольное уменьшение их свободной поверхностной энергии.
Старение обычно не сопровождается изменением химического и минералогического состава коллоидов, но при этом резко изменяются их свойства: они становятся более гидрофобными, уменьшается их сорбционная способность, связь с дисперсионной средой, может произойти частичная кристаллизация гелей.
Для некоторых коллоидов причиной старения является окисление кислородом воздуха, например переход оксида Fe (II) в оксид lll). Свет, особенно ультрафиолетовое излучение, ускоряет старение коллоидов.
3.Состав обменных катионов в почвах и его регулирование
На свойства почвы и условия произрастания растений большое влияние оказывает состав обменных катионов. Так, у почв, насыщенных кальцием, реакция близка к нейтральной; коллоиды находятся в состоянии необратимых гелей и не подвергаются, пептизации при избытке влаги; почвы хорошо оструктурены| обладают благоприятными физическими свойствами.
Черноземы являются примером таких почв. Почвы, у которых в составе обменных катионов в значительном количестве ионы натрия имеют щелочную реакцию, отрицательно влияющую на состояний коллоидов и рост растений. Насыщенные натрием коллоиды пептизируются; содержащие их почвы плохо оструктурены, имеют неблагоприятные водно-физические свойства: повышенную плотность, плохую водопроницаемость, слабую водоотдачу, низкую доступность почвенной влаги (солонцы, солонцеватые почвы).
Всоставе обменных катионов всех почв присутствуют Са2+, Mg2+ и в небольших количествах К+ и NH4. Кроме того, в некоторых почвах содержатся катион Н+ и А13+ или Na+.
В зависимости от состава обменных катионов К. К. Гедройц разделил все почвы на две группы:
почвы, насыщенные основаниями, в составе обменных катионов которых присутствуют Са2+, Mg2+ и Na+, и
почвы, ненасыщенные основаниями, содержащие наряду с Са2+ и Mg2+ катионы Н+ и А13+.
В разных почвах количество и состав обменных катионов, а следовательно, и емкость обменного поглощения катионов различны.
В черноземах в составе обменных катионов доминируют Са2+ и Mg2+ и отмечается высокая емкость поглощения,
в подзолистых почвах наряду с Са2+ и Mg2+ присутствуют Н+ и А13+, емкость поглощения этих почв значительно ниже.
В составе обменных катионов солонцов много обменного натрия.
В профиле почвы величина емкости поглощения обычно уменьшается параллельно снижению количества гумуса.
Состав обменных катионов оказывает большое влияние на свойства почвы и условия произрастания растений. Состав обменных катионов влияет на реакцию и тип коагуляции коллоидов почвы, на ее физические свойства и структурообразование.
У почв, насыщенных Са2+ и Mg2+, реакция близка к нейтральной, коллоиды находятся в состоянии необратимых гелей и не подвергаются пептизации при избытке влаги, почвы хорошо оструктурены и обладают благоприятными физическими свойствами. Таковы черноземы, дерновые почвы.
Почвы, содержащие в составе обменных катионов наряду с Са2+ и Mg2+ значительное количество Na+, характеризуются щелочной реакцией, отрицательно влияющей на состояние коллоидов и рост растений. Коллоиды в этих почвах легко пептизируются, почвы плохо оструктуриваются и имеют неблагоприятные для жизни растений водно-физические свойства (повышенную плотность сложения, плохую водопроницаемость, высокую влагоемкость).
К таким почвам относятся солонцы и сильно солонцеватые почвы.
Почвы, не насыщенные основаниями, в составе обменных катионов которых наряду с обменными Са2+ и Mg2+ содержатся Н+ и А13+, имеют кислую реакцию, токсичную для многих культурных растений, в них легко разрушаются коллоиды в результате кислотного гидролиза, они плохо оструктуриваются. Типичные представители таких почв — подзолистые.
Для характеристики количества катионов и их свойств введено понятие ЕКО.
Емкостью поглощения или емкостью катионного обмена (ЕКО) называется общее количество катионов, которое может быть вытеснено из почвы.
ЕКО характеризует физико-химическую поглотительную способность почв и зависит от минералогического и гранулометрического состава почв, а также от содержания в них гумуса.
Емкость поглощения колеблется в широких пределах: она выше в суглинистых почвах, чем в песчаных, и выше в черноземах, чем в дерново-подзолистых.
Органическая часть почвы обладает более высокой поглотительной способностью, чем минеральная. Емкость катионного обмена возрастает также в условиях нейтральной и щелочной реакции почвы, когда сильнее проявляется отрицательный заряд ацидоидов и может меняться в зависимости от энергии катиона вытеснителя.
Различные почвы отличаются не только по ЕКО, но и по составу поглощенных катионов. Он разнообразен: все почвы содержат в поглощенном состоянии почти все катионы, среди них больше катионов кальция, магния, калия, аммония, присутствуют микроэлементы, катионы водорода и алюминия.