
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Уравнение состояния идеального газа
|
|
Уравнение состояния идеального газа (иногда уравнение Клапейрона или уравнение Менделеева — Клапейрона) — формула, устанавливающая зависимость между давлением, молярным объёмом и абсолютной температурой идеального газа. Уравнение имеет вид:
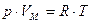
где
- p — давление,
- VM — молярный объём,
- R — универсальная газовая постоянная
- T — абсолютная температура, К.
Так как 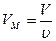 , где
, где 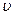 — количество вещества, а
— количество вещества, а 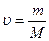 , где m — масса, M — молярная масса, уравнение состояния можно записать:
, где m — масса, M — молярная масса, уравнение состояния можно записать:

Эта форма записи носит имя уравнения (закона) Менделеева — Клапейрона.
В случае постоянной массы газа уравнение можно записать в виде:
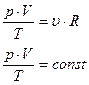
Последнее уравнение называют объединённым газовым законом. Из него получаются законы Бойля — Мариотта, Шарля и Гей-Люссака:
T = const => pV=const — закон Бойля — Мариотта.
p=const => V/T=const — Закон Гей-Люссака.
V=const => p/T=const — закон Шарля (второй закон Гей-Люссака, 1808 г.)
А в форме пропорции  этот закон удобен для расчёта перевода газа из одного состояния в другое.
этот закон удобен для расчёта перевода газа из одного состояния в другое.