
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Общие принципы расчета материального баланса металлургического процесса
|
|
Расчет материального баланса МЕТАЛЛУРГИЧЕСКОГО процесса
Новокузнецк
2009
Федеральное агентство по образованию
Государственное образовательное учреждение
высшего профессионального образования
«Сибирский государственный индустриальный университет»
Кафедра информационных технологий в металлургии
Расчет материального баланса МЕТАЛЛУРГИЧЕСКОГО процесса
Методические указания к выполнению лабораторных работ
по дисциплинам «Математические модели и автоматизированные технологии», «Физико-химические модели в металлургии».
Специальность: 230201 - Информационные системы и технологии
Новокузнецк
УДК 658.012.122: 669.1(07)
М 341
Рецензент:
Доктор технических наук, профессор СибГИУ
К.М. Шакиров
М 341 Расчет материального баланса металлургического процесса: Метод. указ./ Сост.: И.А. Рыбенко, С.П. Мочалов: СибГИУ.- Новокузнецк, 2009.- 26с.
Изложены принципы расчета материального баланса металлургического процесса. Рассмотрен пример расчета, приведены варианты заданий.
Предназначено для студентов специальности: 230201 – Информационные системы и технологии.
Общие принципы расчета материального баланса металлургического процесса
Металлургический агрегат представляет собой реактор, в который поступают конденсированные и газообразные входные потоки и отводятся металл, шлак и газ.
Уравнение материального баланса для всей системы на уровне входных – выходных потоков имеет вид:
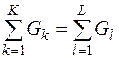 . (1)
. (1)
где К, L - общее количество входных и выходных потоков; Gk, Gl – массы входных и выходных потоков соответственно, кг.
Для любого металлургического процесса выходными потоками являются металл, шлак и газ. С учетом этого, а также при разделении входных потоков на конденсированные и газообразные, уравнение материального баланса можно представить следующим образом:
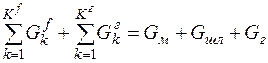 . (2)
. (2)
где K f, K г, G fk, G гk – количество и масса соответственно конденсированных и газообразных потоков, кг; 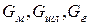 - масса металла, шлака и газа, кг.
- масса металла, шлака и газа, кг.
Общая масса веществ, поступающих в систему с входными потоками соответственно равна:
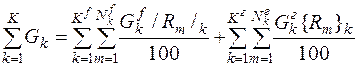 . (3)
. (3)
где N fк, N гк – количество веществ в k- ом потоке; /Rm/k, {Rm}k –содержание вещества Rm в k -ом потоке, %.
Масса веществ выходных потоков определяется массой веществ в металлической, шлаковой и газовой фазах:
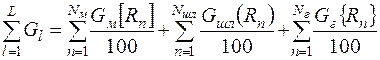 , (4)
, (4)
где Nм, Nшл, Nг – количество веществ в металле, шлаке и газе; [ Rn ], (Rn), { Rn } – содержание n -го вещества в металле, шлаке и газе, %.
Таким образом, материальный баланс на уровне потоков веществ имеет вид:
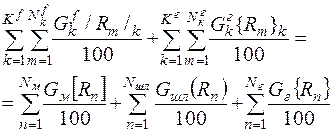 (5)
(5)
Для того, чтобы определить состав фаз выходных потоков, составляются уравнения баланса по каждому элементу Еi, который может присутствовать в разных фазах в виде различных соединений:
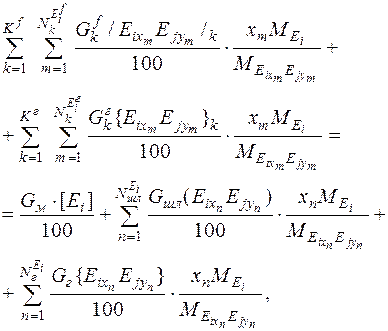 (6)
(6)
где 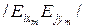 ,
, 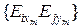 - концентрация m -го вещества, содержащего элемент Еi в k- ом конденсированном либо газообразном входном потоке соответственно, %, [Ei]- концентрация вещества, состоящего из элемента Еi, в металле, %;
- концентрация m -го вещества, содержащего элемент Еi в k- ом конденсированном либо газообразном входном потоке соответственно, %, [Ei]- концентрация вещества, состоящего из элемента Еi, в металле, %; 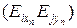 ,
, 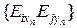 – концентрация n -го вещества, содержащего элемент Еi в шлаковой и газовой фазах выходного потока соответственно, %;
– концентрация n -го вещества, содержащего элемент Еi в шлаковой и газовой фазах выходного потока соответственно, %; 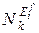 ,
, 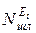 ,
, 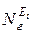 , – количество веществ, содержащих элемент Еi, в k -ом входном потоке, шлаке и газе, хm, ym – стехиометрические коэффициенты m -го соединения элемента Еi; МЕi,
, – количество веществ, содержащих элемент Еi, в k -ом входном потоке, шлаке и газе, хm, ym – стехиометрические коэффициенты m -го соединения элемента Еi; МЕi, 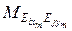 – молярные массы Еi элемента и его соединений, кг/моль.
– молярные массы Еi элемента и его соединений, кг/моль.
2. Пример расчета материального баланса
Рассмотрим пример расчета материального баланса металлургического процесса. В таблице 1 заданы расходы материалов, поступающих в металлургический агрегат. В составе конденсированного входного потока, в зависимости от варианта технологии, могут присутствовать: металлошихта (жидкий и чушковый чугун, металлический лом, металлодобавки); твердые окислители (металлургический агломерат, железная руда, окатыши, окалина); шлакообразующие материалы (известь, известняк, плавиковый шпат, кварцит, боксит, доломит); науглероживатели (графит, орешек коксовый, кокс металлургический, уголь). Газообразными входными потоками являются кислород и природный газ.
Параметры процесса, необходимые для расчета, и коэффициенты распределения элементов по фазам приведены в таблицах 2-3. Химический состав исходных материалов приведен в таблице 4.
Таблица 1 – Исходные данные для расчета. Расходы материалов.
| Наименование материала | Температура, материала, 0С | Масса материала, кг |
| Металлошихта | ||
| 1. Жидкий чугун | 30, 00 | |
| 2. Чушковый чугун | 0, 00 | |
| 3. Металлический лом | 90, 00 | |
| 4. Металлодобавки | 5, 00 | |
| Твердые окислители | ||
| 1. Агломерат металлургический | 3, 00 | |
| 2. Железная руда | 1, 00 | |
| 3. Окатыши | 0, 50 | |
| 4. Окалина | 0, 20 | |
| Шлакообразующие | ||
| 1. Известь | 6, 20 | |
| 2. Известняк | 1, 20 | |
| 3. Плавиковый шпат | 0, 30 | |
| 4. Кварцит | 0, 50 | |
| 5. Боксит | 0, 41 | |
| 6. Доломит | 0, 05 | |
| Науглероживатели | ||
| 1. Графит | 0, 10 | |
| 2. Орешек коксовый | 0, 20 | |
| 3. Кокс металлургический | 0, 10 | |
| 4. Уголь | 0, 10 | |
| Дутье | ||
| 1. Технический кислород, кг | 3, 08 | |
| 2. Прир.газ, кг | 0, 177 |
Таблица 2 – Исходные данные для расчета. Параметры процесса
| Параметры процесса | |
| Окисление железа до FeO | 67, 00% |
| Окисление железа до Fe2O3 | 33, 00% |
| Окисление углерода до CO | 90, 00% |
| Окисление углерода до CO2 | 10, 00% |
| Растворение кислорода в металле | 0, 100% |
Таблица 3 – Исходные данные для расчета. Коэффициенты распределения элементов по фазам
| Элемент | Коэффициенты распределения | Сумма | ||
| металл | шлак | газ | ||
| C | 0, 30 | 0, 00 | 0, 70 | 1, 00 |
| Mn | 0, 48 | 0, 52 | 0, 00 | 1, 00 |
| Si | 0, 02 | 0, 98 | 0, 00 | 1, 00 |
| S | 0, 40 | 0, 50 | 0, 10 | 1, 00 |
| P | 0, 90 | 0, 10 | 0, 00 | 1, 00 |
| Al | 0, 00 | 1, 00 | 0, 00 | 1, 00 |
| Ca | 0, 00 | 1, 00 | 0, 00 | 1, 00 |
| Mg | 0, 00 | 1, 00 | 0, 00 | 1, 00 |
| Ni | 0, 50 | 0, 50 | 0, 00 | 1, 00 |
| Ti | 0, 10 | 0, 90 | 0, 00 | 1, 00 |
| V | 0, 12 | 0, 88 | 0, 00 | 1, 00 |
| Cr | 0, 16 | 0, 84 | 0, 00 | 1, 00 |
Таблица 4 – Исходные данные для расчета. Химический состав материалов
| Металлошихта | FeO | Fe2O3 | MnO | SiO2 | CaO | MgO | Al2O3 | CaF2 | P2O5 | TiO2 | V2O5 | Cr2O3 | NiO |
| 1. Жидкий чугун | - | - | - | - | - | - | - | - | - | - | - | - | - |
| 2. Чушковый чугун | - | - | - | - | - | - | - | - | - | - | - | - | - |
| 3. Металлический лом | - | - | - | - | - | - | - | - | - | - | - | - | - |
| 4. Металлодобавки | - | - | - | - | - | - | - | - | - | - | - | - | - |
| Твердые окислители | |||||||||||||
| 1. Агломерат мет-кий | 28, 00% | 63, 71% | 2, 00% | 3, 00% | 1, 00% | 0, 80% | 0, 41% | - | 0, 08% | - | - | - | - |
| 2. Железная руда | 12, 00% | 62, 34% | 0, 52% | 11, 70% | 7, 05% | 1, 60% | 2, 83% | - | 0, 26% | 0, 20% | 0, 50% | - | - |
| 3. Окатыши | 65, 00% | 18, 00% | 3, 00% | 2, 00% | 2, 00% | 1, 00% | 1, 00% | - | 1, 00% | 1, 00% | 1, 00% | 1, 00% | 1, 00% |
| 4. Окалина | 30, 40% | 67, 55% | 1, 00% | 1, 00% | - | - | - | - | 0, 05% | - | - | - | - |
| Шлакообразующие | |||||||||||||
| 1. Известь | 0, 50% | - | - | 1, 50% | 91, 80% | 1, 80% | 1, 00% | - | - | - | - | - | - |
| 2. Известняк | 1, 10% | 0, 34% | - | 0, 89% | 65, 70% | 1, 05% | 0, 55% | - | 0, 07% | - | - | - | - |
| 3. Плавиковый шпат | 6, 00% | - | - | - | - | - | - | 92, 00% | - | - | - | - | - |
| 4. Кварцит | 5, 50% | - | - | 93, 91% | - | - | - | - | - | - | - | - | - |
| 5. Боксит | 3, 00% | - | - | - | - | - | 91, 00% | 0, 99% | 1, 01% | 0, 94% | 1, 06% | 1, 00% | 1, 00% |
| 6. Доломит | 2, 20% | - | - | 15, 00% | 10, 00% | 72, 80% | - | - | - | - | - | - | - |
| Науглероживатели | |||||||||||||
| 1. Зола графита | 1, 00% | 7, 00% | 1, 00% | 56, 00% | 7, 00% | 2, 20% | 25, 20% | - | 0, 60% | - | - | - | - |
| 2. Зола орешка кокс-го | 0, 12% | 14, 00% | 0, 88% | 49, 33% | 5, 80% | 2, 30% | 26, 80% | - | 0, 77% | - | - | - | - |
| 3. Зола кокса мет-го | - | 14, 12% | 0, 88% | 49, 33% | 5, 80% | 2, 30% | 26, 80% | - | 0, 77% | - | - | - | - |
| 4. Зола угля | 0, 90% | 7, 07% | 1, 08% | 59, 59% | 6, 21% | 2, 48% | 22, 29% | - | 0, 38% | - | - | - | - |
| Металлошихта | Fe мет | C | Si | Mn | Al | S | P | H2O | CO2 | Зола | Итого |
| 1. Жидкий чугун | 94, 41% | 4, 70% | 0, 44% | 0, 34% | - | 0, 02% | 0, 09% | - | - | - | 100, 00% |
| 2. Чушковый чугун | 94, 41% | 4, 70% | 0, 44% | 0, 34% | - | 0, 02% | 0, 09% | - | - | - | 100, 00% |
| 3. Металлический лом | 99, 10% | 0, 30% | 0, 20% | 0, 40% | - | - | - | - | - | - | 100, 00% |
| 4. Металлодобавки | 100, 00% | - | - | - | - | - | - | - | - | - | 100, 00% |
| Твердые окислители | |||||||||||
| 1. Агломерат мет-кий | 1, 00% | - | - | - | - | - | - | - | - | - | 100, 00% |
| 2. Железная руда | 1, 00% | - | - | - | - | - | - | - | - | - | 100, 00% |
| 3. Окатыши | 1, 00% | 2, 00% | - | - | - | - | - | - | - | - | 100, 00% |
| 4. Окалина | 100, 00% | ||||||||||
| Шлакообразующие | |||||||||||
| 1. Известь | - | - | - | - | - | 0, 40% | - | 2, 00% | 1, 00% | - | 100, 00% |
| 2. Известняк | - | - | - | - | - | 0, 30% | - | 5, 00% | 25, 00% | - | 100, 00% |
| 3. Плавиковый шпат | - | - | - | - | - | 2, 00% | - | - | - | - | 100, 00% |
| 4. Кварцит | - | - | - | - | - | 0, 59% | - | - | - | - | 100, 00% |
| 5. Техн-ий глинозем | - | - | - | - | - | - | - | - | - | - | 100, 00% |
| 6. Гравий керамзит-й | - | - | - | - | - | - | - | - | - | - | 100, 00% |
| - | |||||||||||
| Науглероживатели | |||||||||||
| 1. Графит | - | 88, 00% | - | - | - | 2, 00% | - | 1, 00% | - | 9, 00% | 100, 00% |
| 2. Орешек коксовый | - | 83, 00% | - | - | - | 2, 70% | - | 3, 30% | - | 11, 00% | 100, 00% |
| 3. Кокс металлургический | - | 85, 00% | - | - | - | 2, 97% | 0, 03% | - | - | 12, 00% | 100, 00% |
| 4. Уголь | - | 79, 70% | - | - | - | 2, 30% | - | - | - | 18, 00% | 100, 00% |
| Дутье | O2 | CH4 | СO | CO2 | N2 | H2 | H2O | SO2 | Итого |
| 1. Кислород | 99, 5% | - | - | - | 0, 50% | - | - | - | 100, 0% |
| 2. Прир.Газ | 100, 00% | 100, 0% |
Как видно из таблицы 4, с входными потоками в реактор могут поступать различные вещества, среди которых можно выделить следующие: конденсированная фаза - Fe, C, Mn, Si, S, P, Al, Ni, V, Ti, Cr, FeO, Fe2O3, Al2O3, CaO, SiO2, MgO, MnO, P2O5, CaS, CaF2, NiO, V2O5, Cr2O3, TiO2, B 2 O 3; газовая фаза - H2O, CO2, O2, CH4, CO, N2, H2. Элементами, образующими эти вещества являются: Fe, C, O, Mn, Si, S, P, Al, Ca, Mg, H, F, Ni, Ti, V, Cr, N.
Первым этапом расчета является определение масс всех веществ, которые поступают в систему с исходными материалами.
Общая масса конденсированного вещества R, поступающего в металлургический агрегат с входными потоками равна:
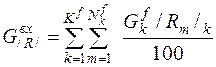 , (7)
, (7)
где K f, G fk – количество и масса конденсированных входных потоков, кг; N fк, – количество веществ в k- ом потоке; /Rm/k –содержание вещества Rm в k -ом потоке, %.
Масса газообразного вещества R, поступающего в печь с входными потоками, также определяется с учетом его содержания в газообразных входных потоках:
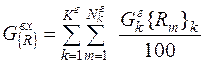 , (8)
, (8)
где K г, G гk – количество и масса газообразных входных потоков, кг; N гк – количество веществ в k- ом газообразном потоке; {Rm}k –содержание вещества Rm в k -ом газообразном входном потоке, %.
Таким образом, общая масса вещества R определяется как сумма его составляющих в каждом материале. Масса вещества в материале, в свою очередь, определяется его процентным содержанием (таблица 4).
Используя данные таблиц (1) и (4), рассчитываем количество всех веществ, поступивших в систему.
Например, общее количество FeO в системе будет равно:
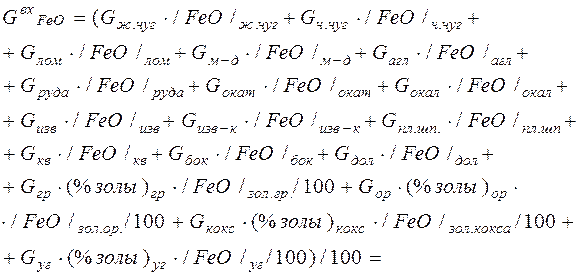 =(30*0% + 0*0% + 90*0% + 5*0% + 3*28% + 1*12% + +0, 5*65% + 0, 2*30, 4% + 6, 2*0, 5% + 1, 2*1, 1% + 0, 3*6, 0% + +0, 5*5, 5%+0, 41*3, 0% + 0, 05*2, 2% + 0, 1*9%*1%/100 + +0, 2*11%*0, 12%/100 + 0, 1*12%*0%/100 + +0, 1*18%*0, 9%/100)/100 = 1, 449 кг (8)
=(30*0% + 0*0% + 90*0% + 5*0% + 3*28% + 1*12% + +0, 5*65% + 0, 2*30, 4% + 6, 2*0, 5% + 1, 2*1, 1% + 0, 3*6, 0% + +0, 5*5, 5%+0, 41*3, 0% + 0, 05*2, 2% + 0, 1*9%*1%/100 + +0, 2*11%*0, 12%/100 + 0, 1*12%*0%/100 + +0, 1*18%*0, 9%/100)/100 = 1, 449 кг (8)
Результаты расчета массы всех веществ, поступивших в систему, представлены в таблице 5.
Затем следует рассчитать массы всех элементов в системе, которые образуют вещества, представленные в таблице 5.
Масса элемента будет определяться массой веществ, содержащих данный элемент с учетом стехиометрических коэффициентов, например:
GFe = GFe + GFeO*MFe/MFeO + GFe2O3*2MFe/MFe2O3 =
= 122, 558 + 1, 449*0, 056/0, 072 + 2, 635*2*0, 056/0, 160 =
=125, 624 кг (9)
В таблице 6 приведены результаты расчетов масс всех элементов, образующих систему.
Следующим этапом расчета является перераспределение элементов по фазам. Элементы, поступающие в систему с входными потоками, распределяются по фазам в соответствии с коэффициентами распределения L. Количество элемента Еi в металле определяется по формуле:
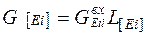 , (10)
, (10)
где L[Ei] – коэффициент распределения элемента Ei в металл.
Таблица 5 - Состав входных потоков, поступающих в агрегат
| Вещество | Расчетная формула | Молярная масса, кг/моль | Масса, кг | % |
| Fe | 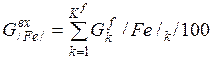
| 0, 056 | 122, 558 | 86, 24% |
| C | 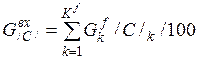
| 0, 012 | 2, 109 | 1, 48% |
| Mn | 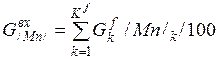
| 0, 055 | 0, 462 | 0, 33% |
| Si | 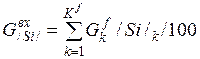
| 0, 028 | 0, 312 | 0, 22% |
| S | 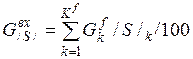
| 0, 032 | 0, 056 | 0, 04% |
| P | 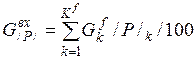
| 0, 031 | 0, 027 | 0, 02% |
| FeO | 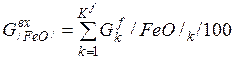
| 0, 072 | 1, 449 | 1, 02% |
| Fe2O3 | 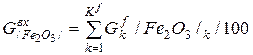
| 0, 160 | 2, 771 | 1, 95% |
| МnO | 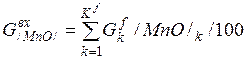
| 0, 071 | 0, 083 | 0, 06% |
| Al2O3 | 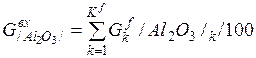
| 0, 102 | 0, 503 | 0, 35% |
| CaO | 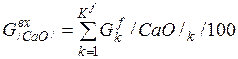
| 0, 056 | 6, 599 | 4, 64% |
| SiO2 | 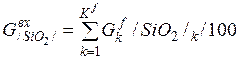
| 0, 060 | 0, 832 | 0, 59% |
| MgO | 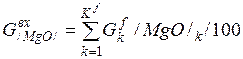
| 0, 040 | 0, 207 | 0, 15% |
| TiO2 | 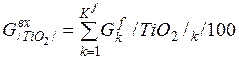
| 0, 080 | 0, 011 | 0, 01% |
| V2O5 | 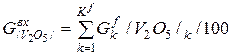
| 0, 182 | 0, 014 | 0, 01% |
| P2O5 | 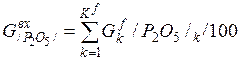
| 0, 142 | 0, 015 | 0, 01% |
| Cr2O3 | 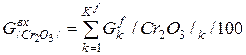
| 0, 152 | 0, 009 | 0, 01% |
| NiO | 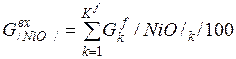
| 0, 075 | 0, 009 | 0, 01% |
| CaF2 | 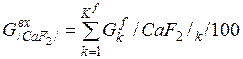
| 0, 078 | 0, 280 | 0, 20% |
| H2O | 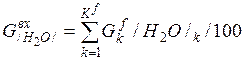
| 0, 018 | 0, 192 | 0, 13% |
| CO2 | 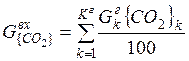
| 0, 044 | 0, 362 | 0, 25% |
| CO | 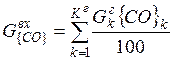
| 0, 028 | 0, 000 | 0, 00% |
| N2 | 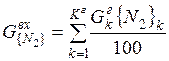
| 0, 028 | 0, 015 | 0, 01% |
| CH4 | 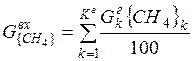
| 0, 016 | 0, 177 | 0, 12% |
| H2 | 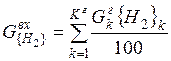
| 0, 002 | 0, 000 | 0, 00% |
| O2 | 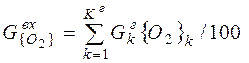
| 0, 032 | 3, 065 | 2, 16% |
| Всего: | 142, 117 | 100, 00% |
Таблица 6 - Поэлементный состав входных потоков, поступающих в агрегат
| Элемент | Расчетная формула | Молярная масса, кг/моль | Масса, кг | % |
| Fe | 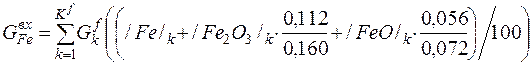
| 0, 056 | 125, 624 | 88, 39% |
| C | 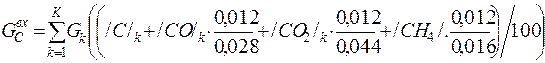
| 0, 012 | 2, 340 | 1, 65% |
| Si | 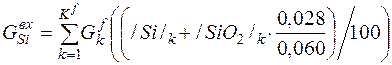
| 0, 028 | 0, 700 | 0, 49% |
| Mn | 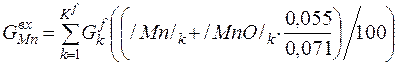
| 0, 055 | 0, 526 | 0, 37% |
| Ca | 
| 0, 040 | 4, 857 | 3, 42% |
| S | 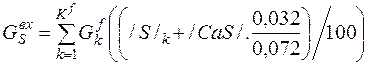
| 0, 032 | 0, 056 | 0, 04% |
| P | 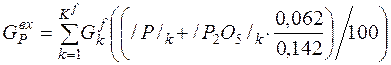
| 0, 031 | 0, 034 | 0, 02% |
| Ti | 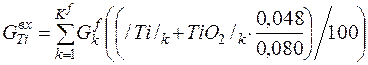
| 0, 048 | 0, 007 | 0, 00% |
| Cr | 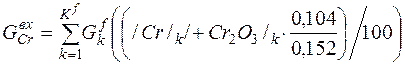
| 0, 052 | 0, 006 | 0, 00% |
| Al | 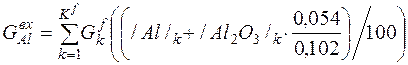
| 0, 027 | 0, 266 | 0, 19% |
| Mg | 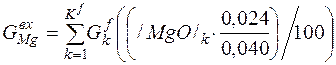
| 0, 024 | 0, 124 | 0, 09% |
| Ni | 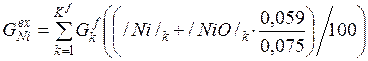
| 0, 059 | 0, 007 | 0, 01% |
| V | 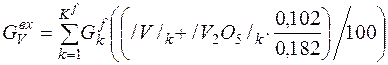
| 0, 051 | 0, 008 | 0, 01% |
| N | 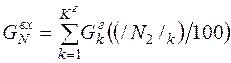
| 0, 014 | 0, 015 | 0, 01% |
| H | 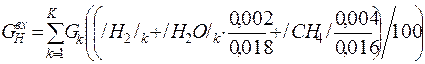
| 0, 001 | 0, 066 | 0, 05% |
| F | 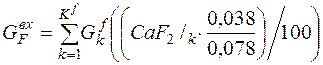
| 0, 019 | 0, 136 | 0, 10% |
| O | 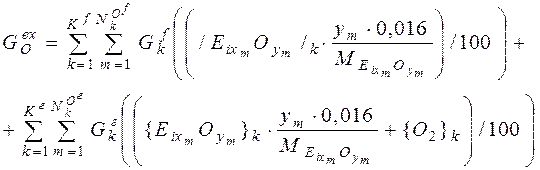
| 0, 016 | 7, 343 | 5, 17% |
| Всего | 141, 117 | 100, 0% |
Определяем количество элемента Еi в металле по формуле (10).
Например, количество марганца в металле равно:
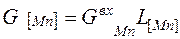 = 0, 526*0, 48 = 0, 253 кг (11)
= 0, 526*0, 48 = 0, 253 кг (11)
Аналогично определяем переход в металл следующих элементов: Si, P, S, Al, Ca, Mg, Ni, Ti, V, Cr.
Фтор в металл не переходит, он будет присутствовать в соединении CaF2 в шлаковой фазе. Азот и водород переходят в газовую фазу. Кислород частично растворяется в металле, его количество будет определяться степенью растворения кислорода в металле (таблица 2). Количество кислорода и железа в металле определим позже, после расчета баланса кислорода в системе.
Количество углерода в металле определим следующим образом:
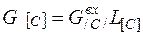 = 2, 34*0, 3 = 0, 633 кг, (12)
= 2, 34*0, 3 = 0, 633 кг, (12)
где 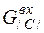 - масса углерода как вещества (таблица 5).
- масса углерода как вещества (таблица 5).
Результаты расчетов количества компонентов металлической фазы (без учета кислорода и железа) приведены в таблице 7.
Таблица 7 – Массы компонентов металла
| Элемент | С | Mn | Si | S | P | Ti |
| кг | 0, 633 | 0, 253 | 0, 014 | 0, 023 | 0, 030 | 0, 001 |
| Элемент | V | Ni | Al | Mg | Ca | Cr |
| кг | 0, 001 | 0, 004 | 0, 000 | 0, 000 | 0, 000 | 0, 001 |
Количество оксида элемента Еi в шлаке также определяем в соответствии с коэффициентом распределения элемента в шлак:
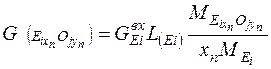 , (13)
, (13)
где L(Ei) – коэффициент распределения элемента Ei в шлак; 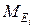 ,
, 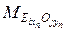 - молярные массы элемента Е и его оксида; хn, y n – стехиометрические коэффициенты.
- молярные массы элемента Е и его оксида; хn, y n – стехиометрические коэффициенты.
По формуле (13) рассчитываем массы оксидов, образующих шлаковую фазу. Например, количество (MnO) в шлаке равно:
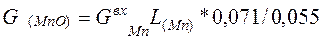 =
=
= 0, 526*0, 52*0, 071/0, 055 = 0, 353 кг (14)
Таким образом, определяем массы всех оксидов, кроме оксидов железа.
Особое внимание следует уделить распределению кальция между соединениями CaO, CaS и CaF 2.
Масса CaF 2 в шлаке определяется его количеством в исходных материалах:
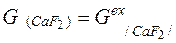 = 0, 280 кг. (15)
= 0, 280 кг. (15)
Массу CaS определим с учетом коэффициента распределения серы в шлак:
G(CaS) = GS*L(S)* 0, 072/0, 032 = 0, 056*0, 5* * 0, 072/0, 032 =
= 0, 063кг, (16)
тогда количество CaO в шлаке будет равно
G(CaО) = GвхCaO – G(CaS) *0, 056/0, 072 = 6, 599 –
– 0, 063*0, 056/0, 072 = 6, 550 кг. (17)
Результаты расчетов количества компонентов шлаковой фазы (без оксидов железа) приведены в таблице 8.
Таблица 8 – Массы компонентов шлака
| Компонент | CaO | CaF2 | SiO2 | Al2O3 | MgO | MnO |
| кг | 6, 550 | 0, 280 | 1, 471 | 0, 503 | 0, 207 | 0, 353 |
| Компонент | CaS | TiO2 | V2O5 | Cr2O3 | NiO | P2O5 |
| кг | 0, 063 | 0, 010 | 0, 013 | 0, 008 | 0, 005 | 0, 008 |
Далее, определяем состав газовой фазы. Для расчета состава и масс компонентов газовой фазы в печи предложен следующий механизм образования отходящих газов. В технологии с применением природного газа предполагается его полное сгорание. Принимаем, что природный газ полностьюсгорает и в газообразном выходном потоке отсутствует.
При полном горении природного газа образуются СО2 и Н2О:
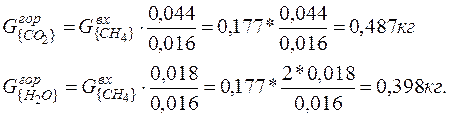 (18)
(18)
Количество СО, образующееся при горении углерода шихты, можно определить следующим образом:
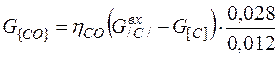 =
=
= 0, 9*(2, 109-0, 633)*0, 028/0, 012 = 3, 100 кг. (19)
где 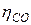 - степень окисления углерода до СО.
- степень окисления углерода до СО.
С учетом горения природного газа и наличия СО 2 во входных потоках, его количество в отходящих газах будет равно:
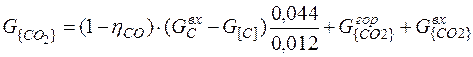 = (20)
= (20)
(1- 0, 9)* (2, 109-0, 633)*0, 044/0, 012 + 0, 487 + 0, 362 = 1, 390 кг.
Водород в отходящих газах отсутствует:
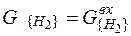 = 0, 000 кг (21)
= 0, 000 кг (21)
Количество водяных паров определяется как сумму следующих составляющих:
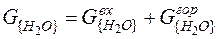 = 0, 192 + 0, 398 = 0, 590 кг. (22)
= 0, 192 + 0, 398 = 0, 590 кг. (22)
Количество азота в отходящих газах равно количеству азота, поступающего с газообразными входными потоками:
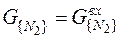 = 0, 015 кг. (23)
= 0, 015 кг. (23)
Количество SO2 в отходящих газах определяется в соответствии с коэффициентом перехода серы в газовую фазу:
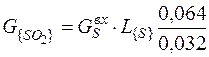 == 0, 056*0, 1*0, 064/0, 032 = 0, 011 кг (24)
== 0, 056*0, 1*0, 064/0, 032 = 0, 011 кг (24)
Теперь следует рассчитать количество железа в металле и его оксидов в шлаке. Для этого определяем количество кислорода, которое остается в системе после окисления всех компонентов.
Общее количество кислорода в исходной системе равно (таблица 6):
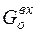 = 7, 343 кг. (25)
= 7, 343 кг. (25)
Этот кислород расходуется на образование всех оксидов шлаковой и газовой фазы: CaO, SiO2, Al2O3, MgO, MnO, TiO2, V2O5, Cr2O3, NiO, P2O5, СО, СО2, Н2О, SO2.
Количество кислорода, затраченное на образование оксидов определим следующим образом:
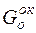 = G(CaO) * 0, 016/0, 056+ G(SiO2) * 0, 032/0, 060 +
= G(CaO) * 0, 016/0, 056+ G(SiO2) * 0, 032/0, 060 +
+G(Al2O3) * 0, 048/0, 102+ G(MgO) * 0, 016/0, 040+
G(MnO) * 0, 016/0, 055+ G(TiO2) * 0, 032/0, 080+
+G(V2O5) * 0, 080/0, 182+ G(Cr2O3) * 0, 048/0, 152+
+G(NiO) * 0, 016/0, 075+ G(Р2O5) * 0, 080/0, 142+
+G{CO} * 0, 016/0, 028+ G{CO2} * 0, 032/0, 044+
+G{H2O} * 0, 016/0, 018+ G{SO2} * 0, 032/0, 064= (26)
=6, 550*0, 016/0, 056+1, 471*0, 032/0, 060+
+0, 503*0, 048/0, 102+0, 207*0, 016/0, 040+
+0, 353*0, 016/0, 071+0, 01*0, 032/0, 080+
+0, 013*0, 080/0, 182+0, 008*0, 048/0, 152+
+0, 005*0, 016/0, 075+0, 008*0, 080/0, 142+
+3, 100*0, 016/0, 028+1, 39 *0, 032/0, 044+
+0, 59 *0, 016/0, 018+ 0, 011*0, 032/0, 064 = 6, 385 кг.
Оставшееся количество кислорода будет равно:
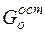 = 7, 343 - 6, 385 = 0, 958 кг. (27)
= 7, 343 - 6, 385 = 0, 958 кг. (27)
Часть этого кислорода растворяется в металле
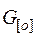 = 0, 958*0, 10%/100 = 0, 001 кг. (28)
= 0, 958*0, 10%/100 = 0, 001 кг. (28)
А оставшийся кислород расходуется на окисление железа: 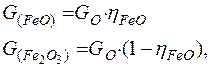 (29)
(29)
где  - степень окисления железа до FeO.
- степень окисления железа до FeO.
Из таблицы 2 следует, что степень окисления железа до FeO составляет 67%, а до Fe2O3 -33%
Тогда количество оксидов железа в шлаке соответственно равно:
G(FeO) = 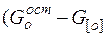 )*67%/100*0, 072/0, 016 =
)*67%/100*0, 072/0, 016 =
0, 957*67%/100*0, 072/0, 016=2, 887 кг
G(Fe2O3) = 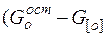 )*33%/100*0, 160/0, 048= (30)
)*33%/100*0, 160/0, 048= (30)
0, 957*33%/100*0, 160/0, 048=1, 053 кг
Количество железа в металле определим следующим образом:
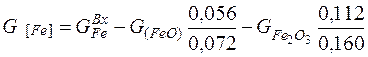 =
=
=125, 530 – 2, 887*0, 056/0, 072 – 1, 053*0, 112/0, 160
=122, 642 кг. (31)
Теперь имеются все данные для определения массы фаз выходных потоков: металла, шлака, газа.
Определяем массу металла как сумму всех компонентов в металле:
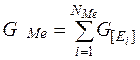 = G[Fe] + G[C]+G[Mn] +G[Si] + G[S] + G[P] +
= G[Fe] + G[C]+G[Mn] +G[Si] + G[S] + G[P] +
+ G[Al] + G[Ca] + G[Mg] + G[Ti] + G[Cr] + G[V] + G[O] + G[Ni] = (32)
=122, 642+0, 633+0, 253+0, 014+0, 023+0, 030+0, 000+0, 000+
+0, 000+0, 0007+0, 001+0, 001+0, 001+0, 004=123, 601 кг.
Аналогичным образом, определяем массу шлака:
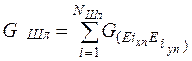 = G(FeO)+ G(Fe2O3) + G(CaO) + G(MnO) +
= G(FeO)+ G(Fe2O3) + G(CaO) + G(MnO) +
+ G(SiO2) + GAl2O3) + G(P2O5) + G(MgO) + G(CaF2) + G(CaS) + (33)
+ G(TiO2) + G(V2O5) + G(Cr2O3) + G(NiO) = =2, 887+1, 053+6, 550+0, 353+1, 471+0, 503+0, 008+0, 207+
+ 0, 280+0, 063+0, 010+0, 013+0, 008+0, 005=13, 409 кг.
И соответственно масса газа:
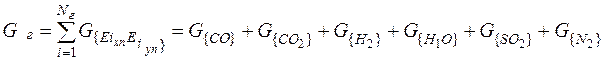 = 3, 100+ 1, 390 + 0, 000 + 0, 590 + 0, 011+ 0, 015 = 5, 107 кг. (34)
= 3, 100+ 1, 390 + 0, 000 + 0, 590 + 0, 011+ 0, 015 = 5, 107 кг. (34)
Результаты расчетов по составу фаз приведены в таблицах 7-9.
Таблица 7 – Состав металла
| Металл | Fe | С | Mn | Si | S | P | Ti |
| % | 99, 224% | 0, 512% | 0, 204% | 0, 011% | 0, 018% | 0, 025% | 0, 001% |
| кг | 122, 642 | 0, 633 | 0, 253 | 0, 014 | 0, 023 | 0, 030 | 0, 0007 |
| Итого | V | Ni | Al | Mg | Ca | O | Cr |
| 100, 00% | 0, 001% | 0, 003% | 0, 000% | 0, 000% | 0, 000% | 0, 001% | 0, 001% |
| 123, 601 | 0, 001 | 0, 004 | 0, 000 | 0, 000 | 0, 000 | 0, 001 | 0, 001 |
Таблица 8 – Состав шлака
| Шлак | FeO | Fe2O3 | CaO | MnO | SiO2 | Al2O3 | P2O5 |
| % | 21, 53% | 7, 85% | 48, 85% | 2, 63% | 10, 97% | 3, 75% | 0, 06% |
| кг | 2, 887 | 1, 053 | 6, 550 | 0, 353 | 1, 471 | 0, 503 | 0, 008 |
| Итого | MgO | CaF2 | CaS | TiO2 | V2O5 | Cr2O3 | NiO |
| 100% | 1, 54% | 2, 09% | 0, 47% | 0, 07% | 0, 09% | 0, 06% | 0, 03% |
| 13, 409 | 0, 207 | 0, 280 | 0, 063 | 0, 010 | 0, 013 | 0, 008 | 0, 005 |
Таблица 9 – Состав газа
| Газ | СО | СО2 | N2 | H2 | H2O | SO2 | Итого |
| % | 60, 70% | 27, 22% | 0, 30% | 0, 00% | 11, 55% | 0, 22% | 100, 00% |
| кг | 3, 100 | 1, 390 | 0, 015 | 0, 000 | 0, 590 | 0, 011 | 5, 107 |
Таким образом, рассчитаны массы выходных потоков – металла, шлака, газа, а также массы и процентное содержание образующих эти фазы веществ. Составляем материальный баланс потоков, веществ и элементов. Баланс потоков представлен в таблице 10, веществ – в таблице 11, элементов – в таблице 12.
Таблица 10 – Материальный баланс потоков
| Наименование | Расход, кг | Наименование | Выход, кг |
| Входные потоки | Выходные потоки | ||
| Металлошихта | Металл | 123, 601 | |
| 1. Жидкий чугун | 30, 00 | Шлак | 13, 409 |
| 2. Чушковый чугун | 0, 00 | Газ | 5, 107 |
| 3. Металлический лом | 90, 00 | ||
| 4. Металлодобавки | 5, 00 | ||
| Всего металлошихты: | 125, 00 | ||
| Твердые окислители | |||
| 1. Агломерат металлургический | 3, 00 | ||
| 2. Железная руда | 1, 00 | ||
| 3. Окатыши | 0, 50 | ||
| 4. Окалина | 0, 20 | ||
| Всего окислителей: | 4, 70 | ||
| Шлакообразующие | |||
| 1. Известь | 6, 20 | ||
| 2. Известняк | 1, 20 | ||
| 3. Плавиковый шпат | 0, 30 | ||
| 4. Кварцит | 0, 50 | ||
| 5. Боксит | 0, 41 | ||
| 6. Доломит | 0, 05 | ||
| Всего шлакообразующих: | 8, 66 | ||
| Науглероживатели | |||
| 1. Графит | 0, 10 | ||
| 2. Орешек коксовый | 0, 20 | ||
| 3. Кокс металлургический | 0, 10 | ||
| 4. Уголь | 0, 10 | ||
| Всего науглероживателей: | 0, 50 | ||
| Дутье | |||
| 1. Технический кислород, кг | 3, 080 | ||
| 2. Прир.газ, кг | 0, 177 | ||
| Всего дутья: | 3, 26 | ||
| ИТОГО: | 141, 117 | ИТОГО: | 141, 117 |
Таблица 11 – Материальный баланс веществ
| Вещество | Исходные | Полученные | ||
| кг | % | кг | % | |
| Fe | 122, 558 | 86, 24% | 122, 642 | 86, 30% |
| С | 2, 109 | 1, 48% | 0, 633 | 0, 45% |
| Mn | 0, 462 | 0, 33% | 0, 253 | 0, 18% |
| Si | 0, 312 | 0, 22% | 0, 014 | 0, 01% |
| S | 0, 056 | 0, 04% | 0, 023 | 0, 02% |
| P | 0, 027 | 0, 02% | 0, 030 | 0, 02% |
| Ni | 0, 000 | 0, 00% | 0, 004 | 0, 00% |
| Ti | 0, 000 | 0, 00% | 0, 001 | 0, 00% |
| V | 0, 000 | 0, 00% | 0, 001 | 0, 00% |
| Cr | 0, 000 | 0, 00% | 0, 001 | 0, 00% |
| FeO | 1, 449 | 1, 02% | 2, 887 | 2, 03% |
| Fe2O3 | 2, 771 | 1, 95% | 1, 053 | 0, 74% |
| CaO | 6, 599 | 4, 64% | 6, 550 | 4, 61% |
| SiO2 | 0, 832 | 0, 59% | 1, 471 | 1, 03% |
| Al2O3 | 0, 503 | 0, 35% | 0, 503 | 0, 35% |
| TiO2 | 0, 011 | 0, 01% | 0, 010 | 0, 01% |
| V2O5 | 0, 014 | 0, 01% | 0, 013 | 0, 01% |
| Cr2O3 | 0, 009 | 0, 01% | 0, 008 | 0, 01% |
| NiO | 0, 009 | 0, 01% | 0, 005 | 0, 00% |
| MgO | 0, 207 | 0, 15% | 0, 207 | 0, 15% |
| MnO | 0, 083 | 0, 06% | 0, 353 | 0, 25% |
| P2O5 | 0, 015 | 0, 01% | 0, 008 | 0, 01% |
| CaF2 | 0, 280 | 0, 20% | 0, 280 | 0, 20% |
| CaS | 0, 000 | 0, 00% | 0, 063 | 0, 04% |
| H2O | 0, 192 | 0, 13% | 0, 590 | 0, 42% |
| СО2 | 0, 362 | 0, 25% | 1, 390 | 0, 98% |
| O2 | 3, 065 | 2, 16% | 0, 001 | 0, 00% |
| CH4 | 0, 177 | 0, 12% | 0, 000 | 0, 00% |
| СO | 0, 000 | 0, 00% | 3, 100 | 2, 18% |
| N2 | 0, 015 | 0, 01% | 0, 015 | 0, 01% |
| H2 | 0, 000 | 0, 00% | 0, 000 | 0, 00% |
| SO2 | 0, 000 | 0, 00% | 0, 011 | 0, 01% |
| Всего: | 142, 117 | 100, 00% | 142, 117 | 100, 00% |
Таблица 12 – Материальный баланс элементов.
| Элемент | Исходные | Полученные | ||
| кг | % | кг | % | |
| Fe | 125, 624 | 88, 39% | 125, 6242 | 88, 39% |
| С | 2, 340 | 1, 65% | 2, 3403 | 1, 65% |
| Mn | 0, 526 | 0, 37% | 0, 5261 | 0, 37% |
| Si | 0, 700 | 0, 49% | 0, 7004 | 0, 49% |
| S | 0, 056 | 0, 04% | 0, 0563 | 0, 04% |
| P | 0, 034 | 0, 02% | 0, 0338 | 0, 02% |
| Al | 0, 266 | 0, 19% | 0, 2661 | 0, 19% |
| Ca | 4, 857 | 3, 42% | 4, 8573 | 3, 42% |
| Mg | 0, 124 | 0, 09% | 0, 1242 | 0, 09% |
| Ni | 0, 007 | 0, 01% | 0, 0072 | 0, 01% |
| Ti | 0, 007 | 0, 00% | 0, 0065 | 0, 00% |
| V | 0, 008 | 0, 01% | 0, 0080 | 0, 01% |
| Cr | 0, 006 | 0, 00% | 0, 0062 | 0, 00% |
| H | 0, 066 | 0, 05% | 0, 0656 | 0, 05% |
| O | 7, 343 | 5, 17% | 7, 3430 | 5, 17% |
| F | 0, 136 | 0, 10% | 0, 1364 | 0, 10% |
| N | 0, 015 | 0, 01% | 0, 0154 | 0, 01% |
| Всего: | 142, 117 | 100, 00% | 142, 117 | 100, 00% |
Как следует из таблиц 10-12, общая масса системы не меняется и составляет 142, 117 кг.