
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Сфера застосування. на державний випускний кваліфікаційний екзамен
|
|
Дипломна робота
на державний випускний кваліфікаційний екзамен
з підготовки робочої професії
лаборант хімічного аналізу
на тему:
«Аналітичний контроль у виробництві нітратної кислоти»
Виконала:
учениця групи №5
Оніщук В. І.
Керівник:
Рівне 2015
Зміст
І. Вступ......................................................................................................................3
ІІ. Основна частина:
1. Технологічний процес виробництва нітратної кислоти........................6
2. Аналізи у виробництві............................................................................15
3. Описання приладу спектрофотометра...................................................................................33
4. Заходи з охорони праці і техніки безпеки............................................36
ІІІ. Висновки...........................................................................................................40
IV. Список літератури............................................................................................41
V.Рецензія...............................................................................................................42
Вступ
ПАТ”орозійно ”представляє хімічне підприємство, розташоване у північно-західній частині України на відстані 15 км від міста Рівне. Це – хімічний гігант України зі своєю історією, наполегливим та працьовитим трудовим колективом, який творить його сьогодення.
Публічне акціонерне товариство „орозійно ” створене 13.11.1995 року на базі орендного підприємства „Азот”, яке до 1994 року мало статус державного підприємства. В 2003 році на підприємстві завершено процес приватизації. Пріоритетним напрямком в його діяльності стало впровадження у виробництво заходів, спрямованих на підвищення ефективності діючих цехів, модернізацію обладнання, поліпшення якості продукції та розширення її асортименту.
Для виготовлення і пакування своєї продукції підприємство використовує сировину і матеріали:
- природний газ;
- бензол;
- сірчану кислоту;
- доломіт;
- ороз;
- соду каустичну;
- вапно будівельне;
- ліламін;
- мішки;
- м'які контейнери типу „біг-бег”;
- каталізатори;
- хімреактиви.
Наша продукція
Мінеральні добрива
1 Селітра аміачна
2 Вапняково-аміачна селітра
3 Аміак рідкий
4 Аміак водний технічний
5 Тукосуміш „Рівне-NРК”
Технологічні процеси на підприємстві
Виробництво аміаку
Виробництво аміачної води
Виробництво неконцентрованої азотної кислоти
Виробництво аміачної селітри..
— Виробництво екстракційної фосфорної кислоти
Виробництво циклогексанолу Виробництво адипінової кислоти
Азотна кислота (HNO3) – безколірна чи жовтувата рідина. Дуже гігроскопічна, „димить” на повітрі, оскільки її пара з вологою повітря утворює краплі туману. Як сильний окисник бурхливо реагує з відновниками. Солома, тирса та інші органічні матеріали, облиті кислотою, загораються, виділяючи при цьому діоксид азоту.
Токсична, може викликати хімічні опіки при потраплянні на шкіру і слизові оболонки, подразнює дихальні шляхи (пара азотної кислоти), може викликати пошкодження зубів, кон’юктивіти. Пари НNO3 на 25% токсичніші, ніж NO2. При важких отруєннях – набряк легень, слабкість, блювота, ядуха, кашель з сильною мокротою, пошкодження зубів, пальців рук. При легких – бронхіт.
При попаданні на шкіру викликає її омертвіння, з’являються водянисті пухирці, які при розривах перетворюються в довго не заживаючі рани.
Використовується для виробництва добрив, органічних барвників, для травлення металів, у виробництві сірчаної кислоти за орозійно методом та для виготовлення целюлозних лаків.
Кислота азотна використовується як окислювач в багатьох хімічних процесах. Пакування і транспортування: кислоту заливають в скляні бутелі, бочки і бідони для нехарчових продуктів, в щільно закриті посудини, виготовлені із орозійно тривкої сталі. Зберігається в упакуванні виробника в критих складських темних приміщеннях окремо від інших реактивів при температурі не вище 300С. Транспортують в залізничних цистернах з написом „Обережно”, „Азотна кислота”. Закупорені і марковані бутелі поміщають у вторинну транспортну
Стадії виробництва
— Підготовка і компримування повітря
— Підготовка газоподібного аміаку
— Підготовка аміачно-повітряної суміші
— Конверсія аміаку та охолодження нітрозного газу
— Абсорбція оксидів азоту
— Селективне очищення хвостових газів від залишкових оксидів азоту
— Рекуперація енергії тиску і теплоти очищених хвостових газів
— Видача та зберігання продукційної кислоти
Технологічний процес виробництва нітратної кислоти
Виробництво неконцентрованої азотної кислоти складається з наступних стадій:
Підготовка і компримування повітря.
Підготовка газоподібного аміаку.
Підготовка аміачно-повітряної суміші.
Конверсія аміаку та охолодження нітрозного газу.
Абсорбція оксидів азоту.
Селективне очищення хвостових газів від залишкових оксидів азоту.
Рекуперація енергії тиску і теплоти очищених хвостових газів.
Видача та зберігання продукційної кислоти.
Підготовка і компримування повітря.
Атмосферне повітря осьовим компресором газотурбінної установки ГТТ-3М всмоктується через повітрозабірну трубу в апарат очищення повітря поз. IX), в якому проходить двоступеневе очищення від пилу і твердих домішок на касетних фільтрах:
грубе очищення - на лавсановому фільтрі елементу Ф-1, 8;
тонке очищення - на фільтрі Петрянова елементу Д-33КЛ;
Із апарату поз. IX повітря надходить в газотурбінну установку ГТТ-3М, де, осьовий компресор поз. Іа стискує повітря до тиску 0, 250 - 0, 293 МПа з підвищенням температури до 175 0С. Потім повітря охолоджується в повітроохолоджувачі поз. Ід до температури не більше 48 0С оборотною водою. Після повітроохолоджувача поз. Ід повітря під тиском 0, 247- 0, 290 МПа надходить в нагнітач поз. Іг, в якому стискується до 0, 80 МПа з підвищенням температури не вище 175 0С.
Після нагнітача основна частина повітря направляється в технологічний цикл безпосередньо на окислення аміаку.
Підготовка газоподібного аміаку.
Газоподібний аміак утворюється в процесі випаровування рідкого аміаку у випарнику поз. 11вузла підготовки аміаку (ВПА).
Рідкий аміак під тиском 1, 3-1, 5 МПа надходить в випарник поз. 11 із мережі підприємства попередньо очистившись від механічних домішок і каталізаторного пилу на магнітному фільтрі, який розміщений на вході рідкого аміаку в цех. Випаровування рідкого аміаку відбувається під тиском 1, 08-1, 20 МПа і температурі 30º С за рахунок теплоти пари, яка надходить в трубний простір випарника з температурою 230-250º С під тиском 1, 5 МПа. В міжтрубному просторі знаходиться рідкий і газоподібний аміак.
Із випарника поз.11газоподібний аміак надходить в фільтр поз.11а, в якому очищується від масла і механічних домішок.
Очищений газоподібний аміак після фільтру надходить в трубний простір підігрівача газоподібного аміаку поз.11г, в якому підігрівається до температури не менше 100-110º С за рахунок теплоти пари, яка надходить в міжтрубний простір з температурою 180-200º С під тиском 0, 6 МПа.
Після підігрівача газоподібного аміаку поз.11ггазоподібний аміак з температурою не менше 100º С направляється в змішувач поз. 2. Частина газоподібного аміаку після вузла підготовки аміаку надходить в реактор селективної очистки поз.5 Конденсат із випарника поз.11 і підігрівача поз.11г окремими загально цеховими колекторами надходить в збірник цехового конденсату поз. 28.
Підготовка аміачно-повітряної суміші (АПС).
Після нагнітача поз. Іг повітря під тиском до 0, 80 МПа з температурою не більше 175º С надходить в змішувач поз.
Аміак надходить в трубки знизу, повітря надходить в міжтрубний простір також знизу. Аміак і повітря змішуються на виході із трубної решітки в завихрювачі, який розміщений над трубною решіткою.
Газоподібний аміак надходить в змішувач під тиском до 0, 80 МПа з температурою не менше 80С. Співвідношення аміак-повітря в АПС підтримується регулятором співвідношення постійним в межах 9, 5-11, 0% об’ємних. Частина газоподібного аміаку, який надходить в змішувач, направляється в реактор селективної очистки поз.
Після змішування аміаку і повітря в змішувачі поз.2, утворена АПС очищується від пилу, механічних домішок, масла на патронних фільтрах, розміщених в верхній частині змішувача..
Конверсія аміаку та охолодження нітрозного газу.
Аміачно-повітряна суміш із змішувача поз.2 з температурою 140-230º С надходить в контактний апарат поз.3, в якому при температурі 850-910º С на каталізаторі відбувається окислення аміаку киснем, який знаходиться в АПС, з утворенням оксиду азоту, водяної пари та елементарного азоту за реакціями:
4NH3 + 5O2 = 4NO + 6H2O + 905, 8 кДж (1)
4NH3 + 4O2 = 2N2O + 6H2O + 1103 кДж (2)
4NH3 + 3O2 = 2N2 + 6H2O + 1267 кДж (3)
Основною є перша реакція. Вихід оксиду азоту від кількості аміаку, який іде на окислення, повинен складати не менше 93, 5 % вагових.
Окислення аміаку відбувається на пакеті платино-родієвих сіток,.
Утворені на каталізаторі нітрозні гази (NOX, N2, H2O) з температурою 850-9100С надходять в котел-утилізатор, де охолоджуються до температури 300-3800С. За рахунок теплоти нітрозних газів в котлі відбувається випаровування деаерованої хімочищеної води з утворенням пари тиском не більше 1, 5 МПа і температурою 230-250º С.
В об’ємі котла частково проходить реакція окислення оксиду азоту в двооксид азоту з виділенням теплоти. Нітрозні гази після котла-утилізатора надходять в підігрівач хвостових газів ІІ ступені поз.1.
В підігрівачі хвостових газів ІІ ступені за рахунок охолодження нітрозних газів від температури 300-380º С до температури 210-260º С хвостові гази підігріваються від температури 110-140º С до температури 240-300º С.
З підігрівача хвостових газів ІІ ступені поз.1 нітрозні гази надходять в підігрівач хвостових газів І ступені поз.6, де за рахунок підігріву хвостових газів охолоджуються до температури 140-190º С.
Абсорбція оксидів азоту.
Після підігрівача хвостових газів І ступені поз.6 нітрозні гази з температурою не більше 197º С надходять в міжтрубний простір холодильників-конденсаторів поз.7, 7а, де охолоджуються до температури 800С оборотною водою, яка подається в трубний простір від абсорбційної колони поз.8. В холодильниках-конденсаторах в міжтрубному просторі відбувається конденсація водяної пари і утворення азотної кислоти з масовою часткою моногідрату 40-50%.
Оборотна вода подається в холодильники-конденсатори після змійовиків абсорбційної колони поз.8. Кислота з холодильників-конденсаторів подається на одну з тарілок абсорбційної колони з відповідною концентрацією.
Нітрозні гази після холодильників-конденсаторів надходять в кубову частину абсорбційної колони під першу тарілку і проходять вверх колони через 47 сітчастих тарілок. На 46 тарілку подається насосами знесолена вода з температурою не більше 35º С.Утворена на верхній тарілці слабка азотна кислота перетікає на нижче розташовані тарілки, рухаючись назустріч нітрозному газу. Масова частка азотної
Процес абсорбції двооксиду азоту - екзотермічний. Для відведення теплоти, яка виділяється в процесі абсорбції, на тарілках розміщено змійовики, по яких проходить оборотна вода. Підведення і відведення оборотної води виконано індивідуально для кожної тарілки.
Після абсорбційної колони оборотна вода з температурою не більше 30º С направляється в холодильники-конденсатори. Далі оборотна вода з температурою не більше 35º С направляється в оборотний цикл.В процесі утворення азотної кислоти в абсорбційній колоні накопичуються хлориди, які посилюють корозію металу. З метою запобігання їх накопичення і зменшення корозійної дії на матеріал колони схемою передбачено відвід хлоридів з тарілок абсорбційної колони в цеховий колектор азотної кислоти.
Допустима масова концентрація хлоридів на тарілках абсорбційної колони становить не більше 500 мг/дм3. З метою підвищення ступеня абсорбції схемою передбачено подачу додаткового повітря для доокислення нітрозних газів в трубопровід нітрозних газів після холодильників-конденсаторів поз.7, 7а. З абсорбційної колони азотна кислота надходить в віддувну колону поз.12, де на тарілках сітчастого типу гарячим повітрям азотна кислота віддувається від оксидів азоту до масової концентрації останніх не більше 0, 1%.
Освітлена азотна кислота після віддувної колони направляється на склад в сховища кислоти або безпосередньо на виробництво адипінової кислоти. Віддуті із віддувної колони гази надходять в трубопровід нітрозних газів перед абсорбційною колоною поз.8 Не абсорбовані хвостові гази після абсорбційної колони з об'ємною часткою оксидів азоту не більше 0, 11% і об'ємною часткою кисню не більше 1, 7-4, 0% надходять в підігрівач хвостових газів І ступені поз.6, де за рахунок теплоти нітрозних газів підігріваються до температури 110-140º С.
Селективне очищення хвостових газів від залишкових оксидів азоту.
Хвостові гази після підігрівача хвостових газів І ступені поз.6 надходять в підігрівач хвостових газів ІІ ступені, де за рахунок охолодження нітрозних газів підігріваються до температури 240-300º С і направляються в реактор селективного очищення.В реакторі на каталізаторі АВК-С)) відбувається відновлення оксидів азоту за реакціями:
6NO + 4NH3 = 5N2 + 6H2O + Q;
6NO2 + 8NH3 = 7N2 + 12H2O + Q;
4NH3 +3O2 = 2N2 + 6H2O + Q;
Газоподібний аміак подається безпосередньо в трубопровід хвостових газів перед реактором поз.5.
Рекуперація енергії тиску і теплоти очищених хвостових газів.
Очищені хвостові гази після реактора селективного очищення поз.5) проходять між зовнішнім і внутрішнім корпусами універсальної камери згоряння турбіни поз. Ів і змішуються з топковими газами, які виходять з камери згоряння турбіни, і з температурою не більше 700º С надходять в газову турбіну.
Сталість температури газової суміші на вході в турбіну забезпечується відповідним режимом роботи камери згоряння турбіни агрегату ГТТ-3М.
Відпрацьовані в турбіні гази з температурою 390-410º С під тиском 0, 006 МПа надходять в котел-утилізатор хвостових газів. В котлі виробляється пара тиском не більше 1, 5 МПа) і температурою 230-250º С за рахунок теплоти хвостових газів.
Хвостові гази після котлів-утилізаторів хвостових газів проходять через економайзер котла-утилізатора нітрозних газів і викидаються в атмосферу через вихлопні труби висотою 151м і 153м.
Зберігання і видача продукційної кислоти.
Освітлена в віддувній колоні азотна кислота з масовою часткою оксиду азоту не більше 0, 1% і масовою часткою моногідрату (МНГ) азотної кислоти не менше 57, 0% по двох колекторах надходить в сховища поз.1021-8 складу Із сховищ азотна кислота насосами подається на виробництво аміачної селітри, на виробництво адипінової кислоти, в цех складних мінеральних добрив. Схемою передбачено подачу азотної кислоти на виробництво АК безпосередньо з віддувних колон.
Крім цього, схемою передбачено наливання азотної кислоти в залізничні цистерни для відправки споживачам.
Оксиди азоту (нітрозний газ) -червоно-бурий газ, в склад якого входять NO, NO2, N2O5.
Токсичний, при вдиханні подразнює верхні дихальні шляхи і слизові оболонки, в великих концентраціях викликає набряк легень. Ознаки отруєння – кашель, подразнення дихальних шляхів, головний біль, блювання, неможливість зробити глибокий вдих, подразнення слизової облонки очей, білуватий наліт на яснах. Через 2-12 годин з’являється відчуття страху, сильної слабкості, зростаючий кашель, лихоманка, піднімається температура, блювота, сильна спрага, біль у діафрагмі. Іноді сильна пітливість.
ГДК – 5 мг/м3.
Перша допомога: необхідно перенести потерпілого на свіже повітря (неприпустимо, щоб потерпілий йшов сам навіть при задовільному стані). Спокій, вдихання кисню, запобігання переохолодження, при зупинці дихання – штучне дихання (спосіб Сильвестра), без стискання грудної клітки. При подразненні дихальних шяхів – содові інгаляції, пити гаряче молоко з содою.
Засоби індивідуального захисту: фільтруючий протигаз з коробкою марки " В" або " М", рукавиці гумові, спецодяг, окуляри герметичні.
Перша допомога: при отруєнні парами - свіже повітря, содові інгаляції, пити молоко з содою. При попаданні на шкіру або слизові оболонки - негайно змити, водою, на шкіру - содові примочки.
Засоби індивідуального захисту: спецодяг з тканини КС, чоботи гумові кислотостійкі, окуляри, фільтруючий протигаз з коробкою марки " М" від парів, гумові рукавиці.
Азотна кислота (НNО3). Безбарвна чи жовтувата рідина. Токсична, може викликати хімічні опіки при потраплянні на шкіру і слизові оболонки, подразнює дихальні шляхи (пара азотної кислоти), може викликати пошкодження зубів, кон’юнктивіти. Пари НNO3 на 25% токсичніші, ніж NO2. При важких отруєннях - набряк легень, слабкість, блювання, ядуха, кашель з сильною мокротою, пошкодження зубів, пальців рук. При легких – бронхіт.
При попаданні на шкіру викликає її омертвіння, з'являються водянисті пухирці, які при розривах перетворюються в довго незагоювані рани.
ГДК: 2мг/м3
Перша допомога: при отруєнні парами - свіже повітря, содові інгаляції, пити молоко з содою. При попаданні на шкіру або слизові оболонки - негайно змити водою, на шкіру - содові примочки.
ЗІЗ: спецодяг з тканини КС, чоботи гумові кислотостійкі, окуляри, фільтруючий протигаз з коробкою марки " М" або ДОТ-600 від парів.
Луги (NаОН, КОН) – білі кристалічні речовини. Застосовуються у вигляді розчинів різних концентрацій. Водний розчин лугу - їдка рідина. Розчини лугу токсичні, діють тим сильніше, чим вища концентрація і температура. При попаданні на шкіру луг викликає тяжко загоюванні опіки, після опіків залишаються рубці. При попаданні на слизові оболонки утворюється м’який струп.
Дуже небезпечне попадання лугу в очі, уражаються глибокі частини очей, що може привести до сліпоти.
ГДК - 0, 5 мг/м3. Клас небезпеки – другий.
Перша допомога: при попаданні на шкіру промити уражену ділянку великою кількістю води під сильним струменем на протязі 10 хв., потім прикласти примочку з 2% розчину оцтової чи борної кислоти. При попаданні в очі - промити їх над фонтанчиком на протязі 10-30хв, потім примочки 5% розчином оцтової або лимонної кислоти. Звернутися в медпункт.
ЗІЗ: спецодяг, захисні окуляри, гумові рукавиці, гумові чоботи, прогумований фартух, індиферентні або гідрофобні мазі.
Аналізи у виробництві
1. Визначення масової частки заліза в нітратній кислоті
Сфера застосування
Цей документ встановлює фотоколориметричну методику виконання вимірювання масової частки заліза в пробах із сховища азотної кислоти (трубопровід А-48) та із трубопроводу подачі азотної кислоти в цех адипінової кислоти в діапазоні від 0, 000020 % до 0, 000400 % (від 0, 20 мг/кг до 4, 00 мг/кг).
Дана методика поширюється на ВАТ “Рівнеазот” в цеху неконцентрованої азотної кислоти і застосовується поза сферою поширення державного метрологічного нагляду.
Час виконання вимірювання 15 хвилин.
Метод вимірювання
Вимірювання за цією методикою виконання вимірювання виконують опосередкованим методом, а саме фотоколориметричним методом, який заснований на випарюванні проби, розчиненні залишку трьохвалентного заліза хлористоводневою кислотою, яке при взаємодії з роданистим амонієм утворює забарвлену сполуку. Інтенсивність забарвлення вимірюють на фотоколориметрі.
Підготовка до виконання вимірювання
При підготовці до виконання вимірювання виконують наступні роботи:
1 Підготовка приладу до роботи
Колориметр фотоелектричний концентраційний КФК-2 включають згідно з інструкцією до приладу [5]. Час виходу приладу на робочий режим 30 хвилин. Вимірювання виконують при довжині хвилі λ =440 нм.
2 Відбір проби
Пробу азотної кислоти відбирають в місцях, які призначені для пробовідбору в чисту склянку з товстостінного скла з притертою пробкою. Перед відбором склянку обполіскують азотною кислотою, яку відбирають. На склянці роблять надпис з зазначенням назви проби, дати, часу та місця відбору.
3 Приготування робочого стандартного розчину з масовою
концентрацією заліза 0, 01 мг/см3
Основний стандартний розчин з масовою концентрацією заліза 1 мг/см3 готують згідно з ГОСТ 4212-76.
Із основного стандартного розчину готують робочий стандартний розчин з масовою концентрацією заліза 0, 01 мг/см3. В мірну колбу місткістю 100 см3 вносять піпеткою місткістю 1 см3 основний стандартний розчин в об’ємі 1 см3, доводять об’єм розчину в колбі до риски розчином сірчаної кислоти з молярною концентрацією c(½ H2SO4)=0, 01 моль/дм3.
4 Побудова градуювального графіка
В мірні колби місткістю 50 см3 послідовно вносять з бюретки місткістю 5 см3 робочий стандартний розчин з масовою концентрацією заліза 0, 01 мг/см3 в об’ємі 0, 5; 1, 0; 1, 5; 2, 0; 2, 5; 3, 0; 3, 5; 4, 0 см3, що відповідає 0, 005; 0, 01; 0, 015; 0, 02; 0, 025; 0, 03; 0, 035; 0, 04 мг заліза.
В кожну колбу циліндром місткістю 25 см3 додають дистильовану воду в об’ємі 25 см3 і піпеткою місткістю 2 см3 вносять розчин хлористоводневої кислоти (конц.) в об’ємі 2 см3, піпеткою місткістю 10 см3 вносять розчин амонію роданистого з масовою часткою 10 % в об’ємі 10 см3. Об’єм розчину в колбах доводять до риски дистильованою водою і ретельно перемішують.
Через 2 хвилини вимірюють оптичну густину кожного розчину на фотоколориметрі при довжині хвилі λ =440 нм в кюветах з товщиною світлопоглинаючого шару ℓ =50 мм. Як розчин порівняння використовується розчин, який містить внесені з тією ж послідовністю всі вище зазначені реактиви, крім стандартного розчину.
За отриманими даними будують градуювальний графік, відкладаючи на осі абсцис введену масу заліза (а) в мг, а на осі ординат відповідні їм значення оптичних густин. Градуювальний графік будують в координатах: а, мг – оптична густина D по середніх значеннях з трьох паралельних вимірювань.
Градуювальний графік перевіряють один раз в 90 днів, а також у випадку заміни реактивів або приладів.
Виконання вимірювання
При виконанні вимірювання масової частки заліза в азотній кислоті виконують наступні операції:
Наважку проби азотної кислоти масою 25, 0 г, зважену на вазі, яка вказана в розд.2, в фарфоровому тиглі випарюють на електроплитці або під інфрачервоною лампою насухо, в охолоджений тигель піпеткою місткістю 2 см3 вносять розчин хлористоводневої кислоти (конц.) в об’ємі 2 см3. Вміст тигля кількісно переносять в мірну колбу місткістю 50 см3, циліндром місткістю 25 см3 додають дистильовану воду в об’ємі 25 см3 і піпеткою місткістю 10 см3 вносять розчин амонію роданистого з масовою часткою 10 % в об’ємі 10 см3. Об’єм розчину в колбі доводять до риски дистильованою водою і ретельно перемішують.
Через 2 хвилини вимірюють оптичну густину розчину на фотоколориметрі так, як вказано при побудові градуювального графіка.
Обчислення результатів вимірювання
Обчислення результатів вимірювання масової частки заліза в азотній кислоті ω в відсотках виконують за формулою:
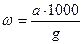 ,
,
де а – маса заліза, знайдена за градуювальним графіком, мг;
g – маса наважки проби, г;
1000– перерахунок г в мг.
Наприклад, 5.04.2012р.:
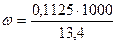 =0, 84%
=0, 84%
2. Метрологія. Знесолена вода. Оборотна вода. Живильна вода.
Хімочищена вода. Конденсат водяної пари. Загальна твердість
Методика виконання вимірювання
Метод вимірювання
Вимірювання за цією методикою виконання вимірювання виконують опосередкованим методом, а саме комплексонометричним методом, який заснований на тому, що сіль динатрієва етилендіамін – N, N, N', N' – тетраоцтової кислоти з іонами кальцію і магнію утворює безбарвну внутрішньо комплексну сполуку.
Титрування проводять в лужному середовищі, водневий показник якого рН 9, 0 – 10, 0, в присутності індикатора кислотного хромтемносинього, який в цьому середовищі при наявності іонів кальцію та магнію забарвлений в винно-червоний колір, а при відсутності їх – синій. Зміна забарвлення розчину при титруванні відбувається тоді, коли трилон Б повністю зв’яже іони кальцію та магнію у комплект.
Підготовка до виконання вимірювання
При підготовці до виконання вимірювання виконують наступні роботи:
1 Відбір проби
Пробу води відбирають з пробовідбірної точки в місцях, призначених для пробовідбору, в склянку місткістю 500 см3 з товстостінного скла з пробкою, яка щільно закривається. Перед відбором склянку обполіскують водою, яку відбирають для аналізу. На склянку наклеюють етикетку із зазначенням назви проби, місця, дати та часу відбору проби.
2 Приготування аміачно-буферного розчину
В мірну колбу місткістю 1000 см3 циліндром місткістю 100 см3 вносять розчин амонію хлористого з масовою часткою 20 % в об’ємі 100 см3 і розчин аміаку з масовою часткою 20 % в об’ємі 100 см3. Доводять об’єм розчину в мірній колбі до риски дистильованою водою і ретельно перемішують. Термін зберігання аміачно-буферого розчину 7 днів.
3 Приготування боратно-буферного розчину
дистильованої води, яку додають циліндром місткістю 1000 см3.
10, 00 г натрію гідроксиду зважують на вазі ВЛКТ-500г-М і розчиняють в 100 см3 дистильованої води, яку додають циліндром місткістю 100 см3.
Обидва розчини змішують і доводять до 1000 см3 цією ж дистильованою водою.
4 Усунення впливу компонентів води, які заважають вимірюванню
Присутність міді і цинку заважає вимірюванню, перехід забарвлення індикатора робиться нечітким. Для усунення впливу цих компонентів до проби, що аналізують, в об’ємі 100 см3 піпеткою місткістю 1 см3 додають розчин натрію сірчистого з масовою часткою 2 % в об’ємі 1 см3 або гідроксиламіну сірчанокислого з масовою часткою 5 % в об’ємі 0, 5 см3. При цьому усувається також вплив марганцю, заліза і алюмінію.
Виконання вимірювання
При виконанні вимірювання загальної твердості вод виконують наступні операції:
1 Вимірювання твердості води в діапазоні понад 0, 015 ммоль/дм3
В конічну колбу місткістю 250 см3 піпеткою місткістю 100 см3 вносять аналізуючу пробу в об’ємі 100 см3, додають піпеткою місткістю 5 см3 аміачно-буферний розчин в об’ємі 5 см3, 8 крапель розчину індикатора кислотного хромтемносинього і повільно титрують розчином трилону Б з відповідною молярною концентрацією С(½ трилон Б) з бюретки відповідної місткості при інтенсивному перемішуванні до зміни забарвлення середовища від винно-червоного до синьо-бузкового.
Рекомендовані параметри бюреток і молярна концентрація трилону Б С(½ трилон Б) в залежності від діапазону вимірювання вказані в таблиці 9.1.1
Таблиця 3.1.1 Рекомендовані параметри бюреток і молярна концентрація трилону Б С(½ трилон Б)
| Діапазон вимірювання, ммоль/дм3 | Молярна концентрація трилону Б С(½ трилон Б), моль/дм3 | Місткість бюретки, см3 |
| Понад 0, 015 до 2, 000 вкл. | 0, 01 | |
| Понад 2, 00 до 20, 00 | 0, 1 |
2 Вимірювання твердості води менше або рівне 0, 015 ммоль/дм3
В конічну колбу місткістю 250 см3 піпеткою місткістю 100 см3 вносять аналізуючу пробу в об’ємі 100 см3, додають піпеткою місткістю 1 см3 боратно-буферний розчин в об’ємі 1 см3, 7 – 8 крапель розчину індикатора кислотного хромтемносинього і повільно титрують розчином трилону Б з молярною концентрацією С(½ трилон Б)=0, 01 моль/дм3 з бюретки місткостю 1 см3 до переходу забарвлення середовища від фіолетового до блакитного. Потім відтитровують надлишок розчину трилону Б розчином сірчанокислого магнію з молярною концентрацією С(½ MgSO4)=0, 01 моль/дм3 до зміни блакитного забарвлення середовища у фіолетовий колір (початкове забарвлення).
Обчислення результатів вимірювання
1. Обчислення результатів вимірювання загальної твердості вод Т в ммоль/дм3 в діапазоні вимірювання понад 0, 015 ммоль/дм3 виконують згідно формули:
 ,
,
де а – об’єм розчину трилонуБ з відповідною молярною концентрацією С(½ трилон Б), що використаний на титрування проби, см3;
С – молярна концентрація розчину трилону Б С(½ трилон Б), моль/дм3;
К – поправочний коефіцієнт для приведення дійсної молярної концентрації розчину трилону Б до номінальної;
V – об’єм проби, взятий для аналізу, см3;
1001– перерахунок моль в ммоль.
2. Обчислення результатів вимірювання загальної твердості вод Т в ммоль/дм3 в діапазоні вимірювання рівне і менше 0, 015 ммоль/дм3 виконують згідно формули:
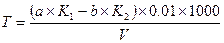 ,
,
де а – об’єм розчину трилону Б з молярною концентрацією c(½ трилон Б)= 0, 01 моль/дм3, що використаний на титрування проби, см3;
К1 – поправочний коефіцієнт для приведення дійсної молярної концентрації розчину трилону Б до номінальної концентрації С(½ трилон Б)= 0, 01 моль/дм3;
b – об’єм розчину магнію сірчанокислого з молярною концентрацією С(½ MgSO4)=0, 01 моль/дм3, що використаний на титрування надлишку розчину трилону Б, см3;
К2 – поправочний коефіцієнт для приведення дійсної молярної концентрації розчину магнію сірчанокислого до номінальної концентрації С(½ MgSO4)=0, 01 моль/дм3;
V – об’єм проби, взятий для аналізу, см3;
0, 01 – молярна концентрація розчину трилону Б С(½ трилон Б), моль/дм3;
1000 – перерахунок моль в ммоль.
Наприклад, 14.03.2012р.:
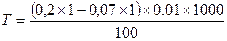 =0, 013ммоль/дм3
=0, 013ммоль/дм3
3. Метрологія. Азотна кислота.
Вміст нітрату амонію.