
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Регуляция биосинтеза белка
|
|
Клетки многоклеточного организма содержат одинаковый набор ДНК, но белки синтезируются разные. Например, соединительная ткань активно синтезирует коллаген, а в мышечных клетках такого белка нет. В эритроцитах содержится Нb, и информация о Нb содержится во всех клетках. С возрастом скорость синтеза изменяется.
Прокариоты.
Теория регуляции биосинтеза у прокариот была разработана в 1961 г. Ф. Жакобом и Ж. Моно. Основные положения теории:
1. неоднородность генетического материала. В геноме имеются:
- структурные гены, которые кодируют синтез структурных белков или ферментов;
- регуляторные гены. Обеспечивают регуляцию считывания информации со структурных генов.
2. регуляция биосинтеза происходит на этапе транскрипции;
3. регуляция осуществляется путем репрессии (подавление транскрипции) и индукции (разрешение транскрипции).
Пр.: работа лактозного оперона.
В клетках микробов имеется фермент лактаза, участвующий в расщеплении лактозы до галактозы и глюкозы. Этот фермент в их клетках вырабатывается только при наличии субстрата – лактозы. Регуляция осуществляется с помощью лактозного оперона. Так, если в среде нет лактозы, то ген-I кодирует синтез белка-репрессора. Белок-репрессор взаимодействует с оператором и в результате РНК-полимераза не может осуществлять транскрипцию. Этот тип регуляции называется репрессией.
Если в среде присутствует лактоза, то она препятствует взаимодействию белка-репрессора с операторм, РНК-полимераза считывает информацию и образуется мРНК лактазы. Т.о. лактоза является индуктором, т.е. веществом, препятствующим взаимодействию белка-репрессора с оператором, в результате чего усиливается и облегчается транскрипция гена лактазы.
У прокариот первичные транскрипты генов (мРНК) используются в синтезе белка еще до завершения процесса транскрипции. У них нет ядерной мембраны.
Эукариоты.
Основные уровни регуляции биосинтеза:
1. на уровне транскрипции. Варианты:
- групповая репрессия генов белками – гистонами;
- амплификация генов - увеличение числа копий заданного участка ДНК или гена. Достигается в результате многократного синтеза ДНК в одном и том же репликативном пузыре. В этом случае транскрипция будет возможна сразу с нескольких копий гена, что увеличивается скорость транскрипции. Эта регуляция изучается у опухолевых клеток, которые способны к амлификации;
- регуляция сигналами-усилителями. Сигналы-усилители - энхансеры - выступающий участок ДНК, который может быть значительно удален от промотора. Под действием энхансера наблюдается более чем 200-кратное увеличение скорости транскрипции. Действует неспецифично, усиливая транскрипцию многих генов.
Пр.: действие гормонов коры надпочечников: глюкокортикоиды проникают внутрь клетки, где взаимодействуют с рецептором, посредством чего проникают в ядро, где присоединяются к ДНК и превращают участок ДНК в энхансер. При этом запускается синтез ферментов, характерных для действия глюкокортикоидов. Данный механизм работает только у эукариот.
2. регуляция на уровне процессинга иРНК:
- разрешение или запрещение процессинга. Так, не все пре-иРНК превращаются в зрелые иРНК: пре-иРНК ®иРНК;
- дифференциальный (альтернативный) процессинг. В клетках эукариот возможен многовариантный процессинг, поэтому утверждение 1 ген®1 белок для них не всегда справедливо. Это происходит в результате потери некоторых экзонов.
Пр.: С-клетки щитовидной железы и нейроны имеют одинаковый ген, который в С-клетках кодирует выработку кальцитонина (регулирует уровень Са2+), а в нейронах дифференцирует процессинг белка CGRP-пептид (регулирует АД).
3. на уровне стабильности и активности иРНК. Чем больше иРНК находится в стабильном состоянии в цитоплазме, тем большее количество молекул белка на ней может быть синтезировано. Поэтому в цитоплазме иРНК консервируются путем взаимодействия с белками-информатионами, образуя комплексы - информосомы.
4. регуляция на уровне трансляции:
- тотальная репрессия или активация трансляции при изменении активности и количества белковых факторов (ФИ и ФЭ);
- избирательная дискриминация иРНК, например, при инфицировании клетки вирусом транслируется вирусная РНК, а РНК хозяина дискриминируется.
- механизм повышения эффективности трансляции включает образование полисом - это комплекс нескольких рибосом с одной иРНК. Расстояние между соседними рибосомами составляет 80 нуклеотидов.
Нарушения матричных биосинтезов
ДНК человека содержит около 3 млрд. нуклеотидов. Точность их копирования зависит от точности: а) репликации, б) транскрипции, в) трансляции.
Факторы нарушения структуры ДНК: УФО, ионизация, химические агенты, спонтанные изменения (при фоновых излучениях).
Чаще всего происходит депуринизация (50'000 нуклеотидов за 70 лет жизни) – 40% всех пуриновых нуклеотидов (за 70 лет). Реже – дезаминирование и депиримидирование.
Этим процессам препятствуют процессы репарации ДНК. Т.о., постоянство информации поддерживается с помощью репликации и репарации.
Изменчивость генотипа наблюдается в результате мутаций. Их молекулярной основой является нерепаративное изменение первичной структуры ДНК. Напр., при действии азотной к-ты изменяются Ц→ У, Ц→ Г, У→ А – эти изменения репаративная система " не замечает".
Система репарации ДНК
Репаративная система состоит из трех ферментов: (1) эндонуклеаза, (2) экзонуклеаза, (3) ДНК-полимераза (репарирующая).
Механизм репарации ДНК:
1. ДНК-эндонуклеаза обнаруживает участок повреждения и вызывает в этом месте разрыв фосфодиэфирных связей.
2. ДНК-экзонуклеаза отщепляет с образовавшихся концов нуклеотиды, в том числе и поврежденные.
3. ДНК-полимераза репарирующая восстанавливает нуклеотиды по принципу комплементарности.
Генные мутации
Они затрагивают небольшие участки ДНК (на уровне генов). Виды генных мутаций:
1. Замена нуклеотидов или кодонов. Замена одного нуклеотида – точечная мутация.
1.1. Замена нуклеотида без изменения смысла кодона. Напр., ААА (лиз)→ ААГ (лиз)
1.2. Замена нуклеотида с изменением смысла кодона. Напр., ААГ (лиз)→ ГАГ (глу). Это миссенс-мутация.
1.3. Замена с образованием терминирующего кодона. Напр., ААА (лиз)→ УАА (обрыв транскрипции). Это нонсенс-мутация.
2. Вставка.
2.1. Вставка одного или нескольких кодонов (т.е. триплетов), при этом не происходит сдвига рамки считывания. Напр., ААА ГЦА ГГА ЦЦА → ААА ГАГ ГЦА ГГА ЦЦА. В белке появляется одна или несколько " лишних" АК.
2.2. Вставка 1, 2 и др., но не кратного трем кол-ва нуклеотидов. Происходит сдвиг рамки считывания. Напр., ААА ГЦА ГГА ЦЦА → ААА ГА Г ЦАГ ГАЦ ЦА… Получается пептид со случайной аминокислотной последовательностью.
3.Делеция.
3.1. Выпадение одного или нескольких кодонов. Нет сдвига рамки считывания. Образуется белок, укороченный на одну или несколько АК.
3.2. Выпадение нуклеотидов 1, 2, но не кратного трем кол-ва. Сдвиг рамки считывания. Синтезируется пептид со случайной последовательностью АК.
Мутации, возникающие в половых клетках, передаются по наследству. Мутации соматических клеток могут приводить к раковому преобразованию клетки.
По биологическим последствиям мутации:
ü молчающие – не проявляются в обычных физиологических условиях, а проявляются в экстремальных условиях.
ü нейтральные – формируется нормальный белок (напр., при замене ГЛУ на АСП).
ü вредные (патогенные) – приводят к заболеванию (напр., при замене в гемоглобине в 6-м положении АК ГЛУ на ВАЛ развивается серповидно-клеточная анемия.
ü полезные – способствуют лучшей адаптации.
Ингибиторы матричных биосинтезов (Антибиотики)
а) ингибиторы, модифицирующие матрицы,
б) модифицирующие рибосомы,
в) инактивирующие ферменты.
Ингибиторы трансляции применяются против прокариот (это антибактериальные препараты). К ингибиторам транскрипции и репликации чувствительны и прокариоты, и эукариоты – они используются для подавления злокачественного роста. Напр., флеомицин, связываясь с ДНК, подавляет репликацию; актиномицин Д ингибирует транскрипцию; митомицин образует ковалентные связи с ДНК (нарушает и транскрипцию, и репликацию). Они подавляют биосинтез во всех клетках.
Антибактериальные
Стрептомицин нарушает структуру рибосом.
Тетрациклин нарушает связывание аминоацил-тРНК с рибосомами.
Эритромицин нарушает образование пептидных связей, нарушает конформацию 50S-субъединицы рибосом.
Биохимический полиморфизм
В результате мутаций возникают различные варианты генов. Если эти варианты не летальны, то они наследуются. Так формируется генотипическая неоднородность (гетерогенность). Это ведет к фенотипической неоднородности. Следствием генотипической неоднородности является полиморфизм белков – это существование разных форм белка, выполняющих одинаковые функции, но отличающихся по физико-химическим свойствам (и по первичной структуре).
Это изобелки, в т.ч. изоферменты.
Так, известно более 300 вариантов гемоглобина, 30 вариантов глюкозо-6-фосфат-ДГ, 14 вариантов альфа1-антитрипсина, 30 вариантов А, В-белков групп крови, 10 вариантов алкоголь-ДГ и ацетальдегид-ДГ.
Биохимический полиморфизм настолько велик, что в настоящее время говорят о биохимической индивидуальности.
Биохимический полиморфизм лежит в основе предрасположенности к заболеваниям (напр., атеросклерозу, алкоголизму, сахарному диабету), непереносимости некоторых пищевых компонентов (напр., лактозы – 15% европейцев, 80% азиатов), непереносимости лекарственных препаратов (напр., непереносимости препарата дитилина при сниженной активности холинэстеразы – дитилин используют при бронхиальной астме).
Биологические последствия обратной транскрипции
В молекулярной биологии принят основной постулат: ДНК → мРНК → белок. Однако, в 1970-е гг. Тёмин открыл фермент обратную транскриптазу ( или ревертазу), катализирующую процесс обратной транскрипции (мРНК → кДНК - комплементарная ДНК). Этот процесс характерен для РНК-содержащих вирусов (ретровирусов), в которых имеется ревертаза, напр., для ВИЧ.
Обратная транскрипция заключается в синтезе короткого фрагмента ДНК, используя мРНК в качестве матрицы. Эта вирусная ДНК внедряется в ДНК хозяина (интеграция), что может приводить к образованию новых вирусных частиц. Интеграция беспорядочна и может привести (1) к мутациям, (2) к образованию онкогенов, (3) к усиленной работе эмбриональных генов (которые в норме во взрослом организме не функционируют).
Теломеры и теломеразы
Метод культуры клеток in vitro широко распространен. Если в эти условия поставить опухолевые клетки, то они делятся бесконечно долго – иммортализованные клетки. Нормальные клетки делятся ограниченное количество раз (это установил Л.Хэйфлик), есть предел деления – лимит Хэйфлика.
Напр., клетка новорожденного может делиться митозом 80-90 раз, взрослого – 60-70 раз, стариков – 20-30 раз, затем репликация нарушается и клетка гибнет.
В 1998 г. американские ученые смогли заставить нормальные клетки делить в 2 раза больше лимита Хэйфлика. В этом участвовали вещества теломеры и ферменты теломеразы.
Теломеры – это специализированные концевые районы хромосомной ДНК, состоящие из многократно повторяющихся коротких нуклеотидных последовательностей. Предполагалось, что эти вещества состоят из 6-8 нуклеотидов: TTAGGG – этот блок повторяется многократно, в результате длина их составляет 2-20 тысяч пар оснований.
Во время репликации в структуре ДНК имеется праймер – короткий РНК-олигонуклеотид, к которому присоединяется ДНК-полимераза. С этого места начинается репликация. Затем происходит удаление праймера и 5'-конец оказывается короче 3'-конца. Возникает эффект недорепликации (Оловников). Образовавшиеся нити ДНК наращиваются с помощью теломеразы. Теломераза синтезирует теломеры. Теломераза – РНК-содержащий фермент, она синтезирует по принципу обратной транскрипции концевой участок, а ДНК-полимераза наращивает другую цепь.
Т.к. теломераза синтезирует теломеры, то она повышает длительность жизни клетки. Повышенная активность теломераз делает клетку бессмертной. Активность теломеразы в различных клетках различна. По активности теломераз выделяют:
1. Соматические клетки. Теломеры их содержат 10-12 тысяч пар нуклеотидов и отсутствует теломеразная активность. Но в макрофагах и лейкоцитах теломераза активна.
2. Половые клетки. Теломеразная активность высокая, теломеры содержат больше – 15-20 тысяч –пар нуклеотидов. То же и в стволовых клетках.
3. Раковые клетки. Длина теломер не очень большая (8-10 тысяч пар нуклеотидов), но высокая теломеразная активность (у 80% раковых клеток).
Т.о., современная биохимия имеет задачей:
а) увеличение теломеразной активности в отдельных клетках, напр., в клетках кожи для восстановления ее после ожогов;
б) снижение теломеразной активности в раковых клетках.
Патология белкового обмена
Нарушения обмена белков могут наблюдаться на различных этапах:
1. На этапе поступления питательных белков в организм. В сутки человеку требуется около 100 г белка. Т.к. белки содержат незаменимые АК, то недостаточное поступление их ведет к снижению или даже к отсутствию синтеза белков в организме.
Напр., недостаток:
ЛИЗ – тошнота, головокружение, повышенная чувствительность к шуму; недостаток
ТРИ – снижение массы тела, гипопротеинемия;
ГИС – снижение гемоглобина в крови;
МЕТ – развитие жирового перерождения печени и почек.
Общее снижение кол-ва белка → белковая недостаточность → отрицательный азотистый баланс, гипопротеинемия.
Тяжелая форма белковой недостаточности – квашиоркор. Сначала снижается общий белок, снижение альбумина ведет к отекам (из-за изменения онкотического давления), снижение гемоглобина ведет к анемии, а само снижение синтеза белка приводит к гипераминоацидемии (повышение АК в крови) и к аминоацидурии. Также снижается синтез ферментов поджелудочной железой (трипсин, химотрипсин, полипептидазы – тоже белки), что ведет к снижению усвоения белка в кишечнике.
2. Нарушение на этапе пищеварения.
2.1. В желудке. Возможна гипоацидитас и анацидитас – ахлоргидрия (снижение и отсутствие кислотности в желудке соответственно). При ахлоргидрии начинается гниение белков.
Гиперацидитас – усвоение белка не нарушается, но может быть поражение слизистой желудка, переходящее в язву.
2.2. В тонкой кишке. Нарушение усвоения белка при панкреатитах, снижении секреции трипсина, химотрипсина.
2.3. В толстой кишке. Повышение процессов гниения белка, напр., при запорах, непроходимости кишечника.
3. Нарушение обмена белков в тканях, т.е. на уровне межуточного обмена. Может быть связано нарушением обмена АК.
3.1. Приобретенные нарушения обмена связаны с дефицитом витаминов; особенно В 6 – нарушение процессов переаминирования и дезаминирования АК, развивается аминоацидурия. Либо связаны с гормональными нарушениями обмена АК.
3.2. Наследственные нарушения обмена АК.
Пример 1: в норме фенилаланин (ФЕН) под действием фенилаланингидроксилазы (ФАГ) окисляется кислородом до тирозина (ТИР).
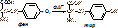
При наследственной патологии (нарушении образования ФАГ) ФЕН накапливается в тканях и затем превращается в фенилпируват, который может превращаться в фениллактат или в фенилацетат. Они накапливаются в тканях и выделяются с мочой (фенилкетонурия). Эти соединения токсичны для ткани мозга, их накопление вызывает нарушения физического и умственного развития. При дефиците ФАГ развивается фенилпировиноградная олигофрения. Если она развилась по гомозиготному типу, то ребенок умственно отсталый и нуждается в помещение в специализированное учреждение. Необходима ранняя диагностика фенилкетонурии (первые 7-10 дней после рождения). Если ребенку ставится этот диагноз, то ему назначается диета, обедненная фенилаланином. Диета сохраняется до 16-18 лет (средний уровень развития).
Пример 2: Генетические нарушения обмена тирозина (ТИР). В организме ТИР образуется из ФЕН (катализируется ФАГ). Затем ТИР может превращаться: (1) в меланин, (2) в тиреоидные гормоны, (3) в ДОФА, а затем в адреналин, (4) в гомогентизиновую к-ту, а затем в конечные продукты (в мочу). Если нарушается блок " ТИР → меланин" (катализируется тирозиназой), то наблюдается альбинизм (отсутствие пигмента кожи меланина). Если блок " гомогентизиновая к-та → конечные продукты" (катализируется оксидазой в присутствии аскорбиновой к-ты), то наблюдается алкаптонурия: моча приобретает темно-бурую окраску, вплоть до черной). Также алкаптонурия может быть приобретенной – при авитаминозе С.
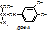
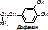
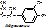
Пример 3: Гистидинемия – повышение ГИС в крови. В норме ГИС под действием гистидазы превращается в уроканиновую к-ту (5-формиминотетрагидрофолиевую к-ту). Накапливающийся ГИС приводит к нарушению умственного и физического развития.
4. Нарушения на стадии биосинтеза белка. Чаще всего наблюдается усиленный синтез белка к.-л. клеткой (злокачественное новообразование).