
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Биогеохимический цикл углерода.
|
|
Циклические процессы массообмена углерода имеют особо важное значение для биосферы. Распределение масс этого элемента следующее. В атмосфере по уточненным данным (Г.В. Войткевич, 1986) находится 2450*109 т углерода. Ежегодная нетто-биопродукция экосферы по С составляет ~ 60 Гт. Такое же количество освобождается в процессах дыхания и деструкции. Период обновления углерода в биосфере 60 лет (для биомассы 10 лет). В океане углерод (помимо его содержания в живых организмах) присутствует в двух главных формах: в составе органического вещества (растворенного в воде и отчасти находящегося в виде взвешенных дисперстных частиц) и в составе взаимосвязанных ионов НСО-3, СО2-3 и СО2.
С углеродом тесно связан весь процесс возникновения и развития биосферы, т.к. именно углерод является основой белковой жизни на нашей планете, т.е. углерод является важнейшим химическим компонентом живого вещества. Именно этот химический элемент, благодаря своей способности образовывать прочные связи между своими атомами, является основой всех органических соединений.
Из атмосферы углерод усваивается автотрофными организмами-продуцентами (растениями, бактериями, цианобионтами) в процессе фотосинтеза, в результате которого, на основе взаимодействия с водой, формируются органические соединения – углеводы. Далее, в результате процессов метаболизма, с участием веществ, поступающих с водными растворами, в организмах синтезируются и более сложные органические вещества. Они не только используются для формирования растительных тканей, но также служат источником питания для организмов, занимающих очередные звенья трофической пирамиды – консументов. Таким образом, по трофическим цепям, углерод переходит в организмы различных животных.
Возвращение углерода в окружающую среду происходит двумя путями. Во-первых – в процессе дыхания. Суть процессов дыхания заключается в использовании организмами окислительных химических реакций, дающих энергию для физиологических процессов. Окисление органических соединений, для которого используется атмосферный или растворённый в воде кислород, имеет результатом разложение сложных органических соединений с образованием СО2 и Н2О. В итоге углерод в составе СО2 возвращается в атмосферу, и одна ветвь круговорота замыкается.
Второй путь возвращения углерода – разложение органического вещества. В условиях биосферы процесс этот в основном протекает в кислородной среде, и конечными продуктами разложения являются те же СО2 и Н2О. Но большая часть углекислого газа при этом не поступает прямо в атмосферу. Углерод, высвобождающийся при разложении органического вещества, в основном остаётся в растворённой форме в почвенных, грунтовых и поверхностных водах. Или в виде растворённого углекислого газа, или же в составе растворённых карбонатных соединений – в форме ионов НСО3- или СО32-. Он может после более или менее продолжительной миграции частично возвращаться в атмосферу, но большая или меньшая его доля всегда осаждается в виде карбонатных солей и связывается в составе литосферы.
Часть атмосферного углерода непосредственно поступает из атмосферы в гидросферу, растворяясь в воде. Главным образом, углекислый газ поглощается из атмосферы, растворяясь в водах Мирового Океана. Сюда же поступает и часть углерода, в тех или иных формах растворённого в водах суши. СО2, растворённый в морской воде, используется морскими организмами на создание карбонатного скелета (раковины, коралловые постройки, панцири иглокожих и т.д.). Он входит в состав пластов карбонатных пород биогенного происхождения, и на более или менее продолжительное время «выпадает» из биосферного круговорота.
В бескислородных средах разложение органического вещества также идёт с формированием в качестве конечного продукта углекислого газа. Здесь окисление протекает за счёт кислорода, заимствуемого из минеральных веществ бактериями-хемосинтетиками. Но процесс в этих условиях идёт медленнее, и разложение органического вещества обычно является неполным. В результате существенная часть углерода остаётся в составе не до конца разложившегося органического вещества и накапливается в толще земной коры в битуминозных илах, торфяниках, углях.
Хранители углерода – это живая биомасса, гумус, известняки и каустобиолиты. Естественными источниками углекислого газа, кроме вулканических эксгаляций, являются процессы разложения органичесекого вещества, дыхание животных и растений, окисление органических веществ в почве и других природных средах. Техногенная углекислота составляет 20х109 т, что пока намного меньше, чем естественное ее поступление в атмосферу. За миллиарды лет с момента появления жизни на Земле весь углерод атмосферы и гидросферы неоднократно прошел через живые организмы. В течение всего 304 лет живые организмы усваивают столько углерода, сколько его содержится в атмосфере. Следовательно, всего за 4 года может полностью обновиться углеродный состав атмосферы, и условно можно считать, что углерод атмосферы за этот срок завершает свой цикл. Цикл углерода, входящего в состав гумуса почв оценивается в 300-400 лет.
Вмешательство человека в круговорот углерода резко возрастает, особенно начиная с 1950-х годов, в результате быстрого роста населения и использования ресурсов, и происходит оно в основном двумя способами:
· сведение лесов и другой растительности без достаточных лесовосстановительных работ, в связи с чем, уменьшается общее количество растительности, способной поглощать углекислый газ.
· сжигание углеродсодержащих ископаемых видов топлива и древесины. Образующийся при этом углекислый газ попадает в атмосферу, постепенное возрастание содержания которого, вызывает так называемый «парниковый эффект».
Биогеохимический цикл азота.
Главным постановщиком азота в биосферу являются недра Земли, основным накопителем – атмосфера, точнее – тропосфера. Наряду с N2 в атмосферу систематически поступают другие газообразные соединения азота: NН3-, N2О, NО-, NО2-. Наряду с оксидами азота в атмосфере присутствует восстановленное соединение азота – аммиак. В кислородсодержащей атмосфере он реагирует с оксидами серы и образует кислый сульфат аммония NH4HSO4. Это соединение, так же как нитраты и нитриты, легко вымываются атмосферными осадками.
Основная часть этого элемента, находящаяся в атмосфере в химически неактивной форме N2, недоступна для главных продуцентов - зеленых растений суши. Но химическая неактивность молекулярного азота не означает его геохимической стабильности. Существуют некоторые виды бактерий, способные активизировать молекулярный азот и связывать его в химические соединения. Этот процесс получил название Фиксации азота. Промышленная фиксация азота идет в присутствии катализаторов при t~500°С и давлении ~300 атм.
В организмах большая часть азота присутствует в форме соединений, в состав которых входит аминогруппа NН2-, или в виде аммония. В процессе биохимической фиксации расщепляется молекула N2 и атомы аммиака. Этот процесс протекает с помощью фермента нитрогеназы. Аммиак и ион NH4+, могут поглощаться корнями растений и как уже отмечено, входить в состав аминокислот. Фиксацию азота осуществляют отдельные специализированные бактерии семейства Azotobacteracea и в определенных условиях синезеленые водоросли. Наиболее продуктивны азотофиксирующие клубеньковые бактерии, образующие симбиозы с бобовыми растениями. Массам азота, фиксируемая из воздуха почвенными бактериями до начала хозяйственной деятельности человека, оценивается разными авторами от 30-40 до 200*106 т/год. В настоящее время к этому добавляется искусственная биологическая фиксация, получаемая при помощи бобовых сельскохозяйственных растений (около 20*109 т/год), а также промышленная фиксация азота из воздуха превысила 60-90*106 т/год.
Цикл – фиксация молекулярного азота – аммонификация мертвого органического вещества – нитрификация – денитрификация имеет наиболее важное значение для глобального массообмена азота, так как этот цикл обеспечивает основной поток азота из его главного резерва – атмосферы.
Часть азота выводится из биологического круговорота и аккумулируется в мертвом органическом веществе. Этот своеобразный запас азота в лесных подстилках, торфе и почвенном гумусе постоянно поддерживается в педосфере и свидетельствует о некоторой заторможенности биологического круговорота.
Промышленная фиксация атмосферного азота – наиболее сильное вмешательство человечества в систему природных глобальных циклов массообмена химических элементов в биосфере. Кроме того, значительное количество азота (около 40*106 т/год) в форме оксидов поступает в атмосферу с выбросами промышленных предприятий и транспорта, образующимися при сжигании минерального топлива, а также в гидросферу с бытовыми и промышленными стоками.
Схема биогеохимического цикла азота представлена на рис. 2.3.
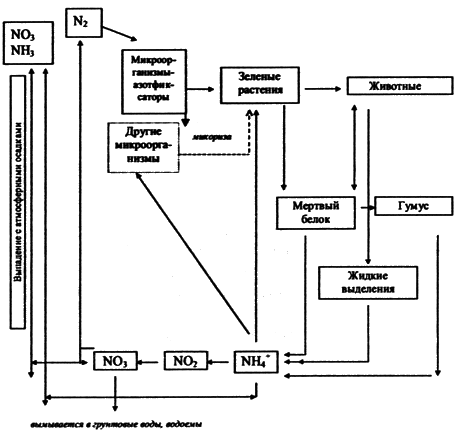
Рис. 2.3 Схема биогеохимического цикла азота
Вмешательство человека в круговорот азота состоит в следующем:
· при сжигании ископаемого топлива в атмосферу выбрасываются большие количества оксида азота (NO-). Оксид азота затем соединяется в атмосфере с кислородом и образуется диоксид азота (NO2-), который при взаимодействии с водяным паром может образовывать азотную кислоту (HNO3). Эта кислота становится компонентом кислотных осадков.
· использование удобрений приводит к выделению в атмосферу «парникового газа» закиси азота (N2O)
· увеличение количества нитратов и ионов аммония в водных экосистемах при смыве с удобрений с полей. Избыток питательных веществ приводит к быстрому росту водорослей, при разложении которых расходуется растворенный кислород, что приводит к массовым морам рыб.
Биогеохимический цикл кислорода
Как Вы помните, кислород – самый распространенный элемент не только земной коры (его кларк 47), но и гидросферы (85, 7%), а также живого вещества (70%). Существенную роль этот элемент играет и в составе атмосферы (более 20%). Благодаря исключительно высокой химической активности, кислород играет особо важную роль в биосфере. Он определяет окислительно-восстановительные и щелочно-кислотные условия растворов и расплавов. Для него характерна как ионная, так и неионная форма миграции в растворах.
Эволюция геохимических процессов на Земле сопровождается неуклонным увеличением содержания кислорода. В настоящее время количество кислорода в атмосфере составляет 1, 2х1015 тонн. Масштабы продуцирования кислорода зелеными растениями таковы, что это количество могло быть удвоено за 4000 лет. Но этого не происходит, так как в течение года разлагается примерно такое же количество органического вещества, которое образуется в результате фотосинтеза. При этом поглощается почти весь выделившийся кислород. Но благодаря незамкнутости биогеохимического круговорота в связи с тем, что часть органического вещества сохраняется и свободный кислород постепенно накапливается в атмосфере.
Главная «фабрика» по производству кислорода на нашей планете – зеленые растения, хотя в земной коре также протекают разнообразные химические реакциив результате которых выделяется свободный кислород.
Еще один миграционный цикл свободного кислорода связан с массобменом в системе природные воды – тропосфера. В воде океана находится от 3х109 до 10х109 м3 растворенного кислорода. Холодная вода высоких широт поглощает кислород, а, поступая с океаническими течениями в тропики – выделяет его в атмосферу. Поглощение и выделение кислорода происходит и при смене сезонов года, сопровождающихся изменением температуры воды.
Кислород расходуется в громадном количестве окислительных реакций, большинство из которых имеет биохимическую природу. В этих реакциях высвобождается энергия, поглощенная в ходе фотосинтеза. В почвах, илах, водоносных горизонтах развиваются микроорганизмы, использующие кислород для окисления органических соединений. Запасы кислорода на нашей планете огромны. Он входит в состав кристаллических решеток минералов и высвобождается из них живым веществом.
Таким образом, общая схема круговорота кислорода в биосфере складывается из двух ветвей:
· образование свободного кислорода при фотосинтезе;
· поглощение кислорода в окислительных реакциях
Согласно расчетам Дж. Уолкера (1980) выделение кислорода растительностью мировой суши составляет 150х1015 тонн в год; выделение фотосинтезирующими организмами океана – 120х1015 тонн в год; поглощение в процессах аэробного дыхания – 210х1015 тонн в год; биологическая нитрификация и другие процессы разложения органического вещества – 70х1015 тонн в год.
В биогеохимическом круговороте можно выделить потоки кислорода между отдельными компонентами биосферы (рис. 2.4).

Рис. 2.4 Схема биогеохимического цикла кислорода
В современных условиях установившиеся в биосфере потоки кислорода нарушаются техногенными миграциями. Многие химические соединения, сбрасываемые промышленными предприятиями в природные воды, связывают растворенный в воде кислород. В атмосферу выбрасывается все большее количество углекислого газа и различных аэрозолей. Загрязнение почв и, особенно, вырубка лесов, а также опустынивание земель на огромных территориях уменьшают производство кислорода растениями суши. Огромное количество атмосферного кислорода расходуется при сжигании топлива. В некоторых промышленно развитых странах кислорода сжигают больше, чем образуется его за счет фотосинтеза.
Биогеохимический цикл фосфора.
Для большинства химических элементов и соединений, которые обычно связаны с литосферой, а не с атмосферой, характерны осадочные циклы. Циркуляция таких элементов осуществляется путем эрозии почв, осадкообразования, горообразования, вулканической деятельности и переноса веществ организмами. Твердые вещества, переносимые по воздуху как пыль, выпадают на землю в виде сухих осадков или с дождем. Осадочные циклы имеют общую направленность «вниз».
Живым сообществам доступны в основном те химические элементы, которые входят в состав пород, расположенных на поверхности Земли. Важным для биосферы элементом, недостаток которого на поверхности ограничивает рост растений, является фосфор.
Человек так изменяет движение многих веществ, участвующих в осадочных циклах, что круговороты их теряют цикличность. В результате в одних местах возникает недостаток, а в других - избыток некоторых веществ. Механизмы, обеспечивающие возвращение химических элементов в круговорот, основаны главным образом на биологических процессах минерализации органических веществ.
Из осадочных циклов наибольшее значение в биосфере имеет круговорот фосфора
Круговорот фосфора в природе сильно отличается от биогеохимических циклов углерода, кислорода, азота и серы, так как газовая форма соединений фосфора (например РН3) практически не участвует в биогеохимическом цикле фосфора. То есть фосфор к накоплению в атмосфере вообще не способен. Поэтому роль «резервуара» фосфора, из которого этот элемент извлекается и используется в биологическом круговороте играет литосфера.
Фосфор в литосфере содержится в форме фосфатных соединений (солей фосфорной кислоты). Основная доля среди них приходится на фосфат кальция – апатит. Это полигенный минерал, образующийся в различных природных процессах – как в глубинных, так и в гипергенных (в том числе и биогенных). Фосфатные соединения способны растворяться в воде, и фосфор в составе иона РО43- может мигрировать в водных растворах. Из них фосфор и усваивается растениями.
Индекс биогенного обогащения почв по отношению к земной коре, а растений по отношению к почвам составляет для фосфора, так же, как и для азота 1000 и 10000 соответственно (Ковда, 1985). Для растений наиболее доступным является фосфор неспецифических органических соединений и гумуса и именно он играет главную роль в малом (локальном) биологическом цикле фосфора.
Животные являются еще большими концентраторами фосфора, чем растения. Многие из них накапливают фосфор в составе тканей мозга, скелета, панцирей.. Есть несколько способов усвоения фосфора организмами-консументами. Во-первых, прямое усвоение из растений в процессе питания. Во-вторых, водные организмы-фильтраторы извлекают фосфор из органических взвесей. В-третьих, органические соединения фосфора усваиваются организмами-илоедами при переработке ими биогенных илов.
Возврат фосфора в окружающую среду происходит при разложении органического вещества. Но возврат этот оказывается далеко не полным. В целом для соединений фосфора характерна тенденция выноса в форме водных растворов и взвесей в конечные водоёмы стока, в наибольшей мере – в Мировой Океан, где он и накапливается в составе осадочных отложений различного генезиса. Вновь вернуться в экзогенный круговорот эта часть фосфора может только в результате тектонических процессов, растягивающихся на сотни миллионов лет. В естественных условиях сохранение баланса обеспечивается сравнительно слабой подвижностью соединений фосфора, в результате которой фосфор, извлечённый растениями из почвы, большей частью возвращается в неё в результате разложения органического вещества. В почвах и породах фосфор достаточно легко фиксируется. Фиксаторами фосфора являются гидроксиды железа, марганца, алюминия, глинистые минералы (особенно, минералы группы каолинита). Однако, фиксированный фосфор может быть на 40-50% десорбирован и использован растениями. Этот процесс зависит от рН и Eh условий среды. Повышенная кислотность, образование угольной кислоты, способствуют десорбции фосфора, усилению миграции фосфорных соединений.
В восстановительной среде образуются соединения фосфора с двухвалентным железом, что тоже способствует выносу фосфора из почвы.
Миграция фосфора возможна и за счет водной и ветровой эрозии. Поэтому биогеохимический цикл фосфора значительно менее замкнут и менее обратим, чем циклы углерода и азота, а загрязнение фосфором окружающей среды особенно опасно (рис. 2.5).

Рис. 2.5. Схема биогеохимического цикла фосфора
Основными особенностями круговорота фосфора, таким образом, являются:
· отсутствие атмосферного переноса;
· наличие единственного источника – литосферы;
· тенденция к накоплению в конечных водоёмах стока.
При интенсивной сельскохозяйственной эксплуатации земель потери фосфора в ландшафте становятся практически необратимыми. Компенсация возможна только за счёт применения фосфорных удобрений. Известно, что фосфорные удобрения являются важным и необходимым звеном в получении высоких урожаев сельскохозяйственных культур. Однако, все известные запасы месторождений фосфатов ограничены и по предсказаниям ученых могут истощиться уже в ближайшие 75-100 лет. В то же время, вредные соединения фосфатов в последнее время становятся одним из важнейших факторов загрязнения речных и озерных вод.
Таким образом, в последе время общая картина распределения им миграции фосфора в биосфере резко нарушена человеком. Вот слагаемые этого явления: во-первых, мобилизация фосфора из агроруд и шлаков, производство и применение фосфорных удобрений, во-вторых производство фосфорсодержащих препаратов и их использование в быту; в-третьих – производство фосфорсодержащих ресурсов продовольствия и кормов, вывоз и потребление их в зонах концентрации населения; в-четвертых – развитие рыбного промысла, добыча морских моллюсков и водорослей, что влечет за собой перераспределение фосфора из океана на сушу. В итоге наблюдается процесс фосфатизации суши, но процесс этот проявляется крайне неравномерно. Увеличивается содержание фосфора в окружающей среде больших городов. Напротив, страны, активно экспортирующие органические продукты и не применяющие фосфорных удобрений, теряют запасы фосфора в своих почвах.
Вмешательство человека в круговорот фосфора сводится в основном к двум вариантам:
· добыча больших количеств фосфатных руд для производства минеральных удобрений и моющих средств;
· увеличение избытка фосфат-ионов в водных экосистемах при попадании в них загрязненных стоков с животноводческих ферм, смытых с полей фосфатных удобрений, а также очищенных и неочищенных коммунально-бытовых стоков. Избыток этих элементов способствует «взрывному» росту сине-зеленых водорослей и других водных растений, что нарушает жизненное равновесие в водных экосистемах.
Биогеохимический цикл серы
Сера также является одним из элементов, играющих чрезвычайно важную роль в круговороте веществ биосферы. Она относится к числу химических элементов, наиболее необходимых для живых организмов. В частности, она является компонентом аминокислот. Она предопределяет важные биохимические процессы живой клетки, является незаменимым компонентом питания растений и микрофлоры. Соединения серы участвуют в формировании химического состава почв, в значительных количествах присутствуют в подземных водах, что играет решающую роль в процессах засоления почв.
Содержание серы в земной коре составляет 4, 7х10-2%, в почве – 8, 5х10-2%, в океане – 8, 8х10-2% (Виноградов, 1962). Однако, в засоленных почвах содержание серы может достигать значений, измеряемых целыми процентами. Таким образом, основным резервуаром, из которого она черпается живыми организмами, является литосфера. Это обусловлено тем, что устойчивое существование сернистых соединений в условиях современной атмосферы Земли, содержащей свободный кислород и пары Н2О, невозможно. Сероводород (H2S) в кислородной среде окисляется, а кислородные соединения серы, реагируя с Н2О, образуют серную кислоту H2SO4, которая выпадает на поверхность Земли в составе кислотных дождей. Поэтому оксиды серы SOх, хотя и могут усваиваться растениями непосредственно из атмосферы, существенной роли в круговороте серы этот процесс не играет.
Сера имеет несколько изотопов, из которых в природных соединениях наиболее распространены S32 (> 95%) и S34 (4, 18%). В результате биологических и биогеохимических процессов происходит изменение в соотношении этих изотопов в сторону увеличения содержаний более легкого изотопа в верхних гумусовых горизонтах почв.
Изотопный состав серы подземных, почвенно-грунтовых вод и водорастворимых сульфатов из горизонта С сульфатно-содовых солончаков является сходным.
В составе земной коры соединения серы существуют, в основном, в двух минеральных формах: сульфидной (соли сероводородной кислоты) и сульфатной (соли серной кислоты). Редко встречается самородная сера, которая неустойчива и склонна, в зависимости, от значений окислительно-восстановительного потенциала среды, формировать или кислородные, или водородные соединения.
Первичной, глубинной по происхождению, минеральной формой нахождения серы в земной коре, является сульфидная. Сульфидные соединения в условиях биосферы практически нерастворимы, и потому сульфидная сера растениями не усваивается. Но, в то же время, сульфиды в кислородной среде неустойчивы. Поэтому сульфиды на земной поверхности, как правило, окисляются, и в результате этого сера входит в состав сульфатных соединений. Сульфатные соли обладают достаточно хорошей растворимостью, и сера в географической оболочке активно мигрирует в водных растворах в составе сульфат-иона SO42-.
Именно в этой, сульфатной форме сера, в составе водных растворов, эффективно усваивается растениями, а далее – животными организмами. Усвоению способствует то, что сульфатные соединения серы способны накапливаться в почвах, участвуя в процессах обменной сорбции и входя при этом в состав почвенного поглощающего комплекса (ППК).
Разложение органического вещества в кислородной среде приводит к возвращению серы в почву и природные воды. Сульфатная сера мигрирует в водных растворах, и может снова использоваться растениями. Если же разложение идёт в бескислородной среде, ведущую роль играет деятельность серобактерий, которые восстанавливают SO42- до H2S. Сероводород выделяется в атмосферу, где окисляется и возвращается в другие компоненты биосферы в сульфатной форме. Часть серы в восстановительной обстановке может связываться в сульфидных соединениях, которые, при возобновлении доступа кислорода, снова окисляются и переходят в сульфатную форму.
Биогеохимический цикл серы состоит из 4 стадий (рис. 2.6):
1. усвоение соединений серы живыми организмами (растениями и бактериями) и включение серы в состав белков и аминокислот.
2. Превращение органической серы живыми организмами (животными и бактериями) в конечный продукт – сероводород.
3. Окисление минеральной серы живыми организмами (серобактериями, тионовыми бактериями) в процессе сульфатредукции. На этой стадии происходит окисление сероводорода, элементарной серы, ее тио- и тетрасоединений.
4. Восстановление минеральной серы живыми организмами (бактериями) в процессе десульфофикации до сероводорода. Таким образом, важнейшим звеном всего биогеохимического цикла серы в биосфере является биогенное образование сероводорода.
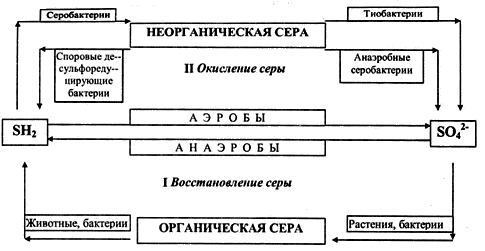
Рис. 2.6. Схема биогеохимического цикла серы
Изъятие серы из биосферного круговорота происходит в результате накопления сульфатных отложений (в основном гипсовых), слои и линзы которых становятся компонентами литосферы. Компенсируются потери во-первых, в процессах вулканизма (поступление H2S и SOx в атмосферу, а оттуда, с атмосферными осадками – на поверхность Земли). А во-вторых, в результате деятельности термальных вод, с которыми в верхние горизонты земной коры и на дно Мирового океана поступают сульфидные соединения.
Таким образом, к характерным особенностям круговорота серы можно отнести второстепенную роль процессов атмосферной миграции, а также многообразие форм нахождения, обусловленное переходом её из сульфидных форм в сульфатные и обратно, в зависимости от изменения окислительно-восстановительных условий.
Промышленные процессы выносят в атмосферу большое количество серы. В отдельных случаях значительная концентрация соединений серы в воздухе служит причиной нарушений в окружающей среде, в том числе, кислотных дождей. Присутствие в воздухе двуокиси серы негативно влияет как на высшие растения, так и на лишайники, причем эпифитные лишайники могут служить индикаторами повышенных содержаний серы в воздухе. Лишайники поглощают влагу из атмосферы всем слоевищем, поэтому концентрация серы в них быстро достигает предельно допустимого уровня, что ведет к гибели организмов.
Поступление серы в общий круговорот по данным Дж. П. Френда (1976) следующее:
При дегазации земной коры – 12х1012 г/год; при выветривании осадочных пород – 42х1012 г/год,; антропогенные поступления в виде сернистого газа – 65х1012 г/год, что в сумме составляет 119х1012 г/год. Значительные количества серы ежегодно консервируются в виде сульфидов и сульфатов – 100х1012 г/год и, таким образом., временно выводятся из общего биогеохимического круговорота.
Таким образом, антропогенное поступление серы в биосферу существенно изменяет круговорот этого элемента, а приход серы в биосферу превышает ее расход, в результате чего, должно происходить постепенное ее накопление.
КОНТРОЛЬНЫЕ ВОПРОСЫ
1. Какой русский ученый внес наибольший вклад в изучение биосферы?
2. Как называется совокупность живых организмов по Вернадскому?
3. Что такое ноосфера?
4. Каким образом атмосферный азот становится частью живой материи?
5. Как по Вернадскому называется материя, образованная без участия живых организмов?
6. Чем различаются большой и малый круговороты вещест?
7. Какова основная особенность круговорота воды?
8. Как влияет человек на круговорот воды?
9. В чем различие газообразных и осадочных биогеохимических циклов?
10. Как влияет человек на круговорот углерода?
11. Как влияет человек на круговорот азота?
12. Как влияет человек на круговорот фосфора?