
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Теоретична частина
|
|
Оксидами називаються сполуки елементів з Оксигеном, в яких він має ступінь окиснення -2.
За хімічними властивостями оксиди поділяють на несолетворні і солетворні. Оксиди, які не утворюють гідратних сполук і солей, називаються несолетворними (N2O, NO, CO, SiO).
Оксиди, які під час хімічних реакцій утворюють солі, є солетворними. За хімічними властивостями вони поділяються на основні, кислотні та амфотерні.
Основними називають оксиди, гідрати яких є основними. До основних належать оксиди активних металів – лужних (Li, Na, K, Rb, Cs), лужноземельних (Ca, Sr, Ba, Ra), Магнію, Лантану, а також перехідних металів (Mn, Cr, Ni, Fe, Cu) в нижчих ступенях окиснення (+1, +2). Основні оксиди реагують з кислотними оксидами та їх гідратами (кислотами) з утворенням солей:




Оксиди лужних і лужноземельних металів розчиняються у воді, утворюючи при цьому їх гідрати – розчинні у воді основи (луги):

Кислотними оксидами або ангідридами називають оксиди, гідрати яких є кислотами. До них належать оксиди неметалів (CO2, B2O3, N2O5, P2O5, SO3, SO2, N2O3), а також оксиди перехідних металів у вищому (+6, +7) ступені окиснення (CrO3, MnO3, Mn2O7). Кислотні оксиди реагують з основними оксидами і їх гідратами (основами) з утворенням солей:




Майже всі кислотні оксиди, окрім SiO2 і деяких інших розчиняються у воді, утворюючи при цьому їх гідрати – кислоти:
 - сульфітна кислота,
- сульфітна кислота,
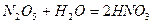 - нітратна кислота,
- нітратна кислота,
 - манганатна(VІІ) кислота,
- манганатна(VІІ) кислота,
 - манганатна(VІ) кислота.
- манганатна(VІ) кислота.
Ангідридами кислот називають кислотні оксиди, які одержані шляхом дегідратації (відбирання води) від відповідних оксигеновмісних кислот:
 - нітратний ангідрид,
- нітратний ангідрид,
 - сульфатний ангідрид.
- сульфатний ангідрид.
Амфотерними оксидами називають оксиди, які мають слабко виражені і кислотні і основні властивості, тобто здатні реагувати і з сильними кислотами і з сильними основами (лугами) з утворенням солей. До них належать оксиди деяких малоактивних металів головних підгруп (ВеО, А12О3), а також оксиди багатьох перехідних металів у проміжному ступені окиснення (ZnO, Cr2O3, MnO2, SnO2, Fe2O3, TiO2).
У перехідних металів із змінною валентністю з підвищенням ступеня окиснення хімічний характер оксидів змінюється від основного через амфотерний до кислотного:
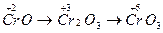 .
.
основний амфотерний кислотний
Амфотерні оксиди реагують з кислотними оксидами та кислотами, проявляючи слабко виражені основні властивості, з утворенням солей:


Проявляючи слабко виражені кислотні властивості, амфотерні оксиди реагують з оксидами, гідроксидами або карбонатами лужних та лужноземельних металів з утворенням солей. Ці реакції відбуваються під час сплавлення:
 ,
,
натрій цинкат
 ,
,
натрій метаалюмінат
 ,
,
натрій ортоалюмінат
 .
.
Одержані солі приєднують воду за звичайних умов, утворюючи комплексні солі:
 - натрій тетрагідроксоалюмінат,
- натрій тетрагідроксоалюмінат,
 - натрій гексагідроксоалюмінат.
- натрій гексагідроксоалюмінат.
При безпосередній взаємодії амфотерних оксидів з концентрованими розчинами лугів утворюються комплексні солі:

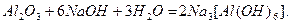
Основами називають сполуки, які у водних розчинах дисоціюють на катіони основних залишків та гідроксид-аніони ОН-.
Найважливіша хімічна властивість основ – здатність реагувати з кислотами та кислотними оксидами (ангідридами) з утворенням солей:


Основи є продуктами гідратації основних оксидів. Розчинні у воді основи (луги) утворюються в результаті прямої гідратації розчинних у воді основних оксидів:
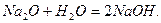
Нерозчинні у воді основи утворюються в результаті непрямої гідратації основних оксидів:


Амфотерні гідроксиди – це продукти непрямої гідратації амфотерних оксидів. Як і амфотерні оксиди, вони реагують як з кислотами, так і з лугами з утворенням солей. При взаємодії з кислотами вони поводять себе як слабкі основи, а при взаємодії з лугами – як слабкі кислоти:


натрій цинкат
 натрій
натрій
тетрагідроксоцинкат