
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Расчет поверхности теплообмена
|
|
Операция выделения гидрата диацетон -2-кето-L- гулоновая кислоты
Для нейтрализации используется 21% соляная кислота Реакция нейтрализации щелочи
NaOH + HCl = NaCl + H2O (реакция №3)
М.М=40 36, 5 58, 5 18
а) Определяем количество соляной кислоты из пропорции:
40 NaOH - 36, 5 HCl
1187, 61NaOH — Х кг HCl
х = 1083, 69 кг
б) содержание воды в 21% соляная кислота 1083, 69 *100/21 = 5160, 43 кг
5160, 43 - 1083, 69 = 4076, 74
в) количество гидрата диацетон- 2-кето-L- гулоновая кислоты полученное в результате реакции
C12H17 O9Na+HCl+H2O→ C 12H20O8 +H2O +NaCl (Реакция№4)
Натривая соль ДКГК
296 кг натриевая соль - диацетон-2-кето-L- гулоновой кислоты - 292 кг
гидрат 7872, 37 кг - х кг гидрат
х = 7765, 99 кг
с учетом выхода = 0.974 (технологический регламент)
7765, 99 * 0, 974 = 7564, 07 кг
Остаток натриевая соль диацетон-2-кето-L- гулоновой кислоты составит
7765, 99 - 7564, 07 = 201, 92 кг
г) Определяем количество NaCl образовавшейся при нейтрализации:
по реакции №3
40 NaOH - 58, 5 NaCl
1187, 61 NaOH — х NaCl
х =1736, 88 кг
по реакции №4
292 гидрат — 58, 5 NaCl
7564, 07 гидрат - х кг NaCl
х = 1515, 4 кг
Всего NaCl:
1736, 88 + 1515, 4 = 3252, 28 кг
д) Количество воды образовавшееся при нейтрализации щелочи (реакция № 3)
40 NaOH — 18 H2O
1187, 61NaOH - х H2O
х = 534, 42 кг
Количество воды в реакционной массе
14220, 41- (7564, 07+201, 92+3252, 28+534, 42) = 2667, 72 кг
Таблица материального баланса Таблица 4.2
| Приход | Расход | ||
| Вещества | кг | Вещества | кг |
| 1.Натриевая соль Д2ККГ кислоты | 7872, 37 | 1. Гидрата диацетон -2- кето-L- гулоновая кислоты | 7564, 07 |
| 2 Щелочь | 1187, 61 | 2.2КТ кислоты | 201, 92 |
| 3.Соляная кислота 21% | 5160, 43 | 3. NaCl | 3252, 28 |
| 4.Вода с продуктами расложения. | 2667, 72 | ||
| Итого | 14220, 41 | 14220, 41 |
4.2 Технологический расчет основного аппарата.
Реактор-гидрататор предназначен для реакции получения натриевой соли диацетон-2-кето-L-гулоновой кислоты в жидкой среде. Принимаем стальной эмалированный аппарат с механическим перемешиванием.
Согласно каталога эмалированного емкостного оборудования Фастовского Завода Химического Машиностроения «Красный октябрь» объемом (4м3 площадь поверхности теплообмена F — 8, 57 м2 (каталог эмалированного оборудования).
Реактор представляет собой емкостной вертикальный аппарат с механическим перемешивающим. Реактор оснащен пропеллерной мешалкой, число оборотов 170 об/мин. Для отведения тепла реакции аппарат снабжен рубашкой, охлаждающим агентом является рассол.
Расчет поверхности теплообмена
Определяем поверхность теплообмена
F = Q/K*Δ tcр*τ
Где: Q — общая тепловая нагрузка (из теплового баланса)
К — коэффициент теплопередачи принимаем равным
Δ tср - средняя разность температур (средний температурный напор) при противотоке.
Для расчета реакторов с мешалкой и поверхностью теплообмена применяется формула Критерия Нуссельта
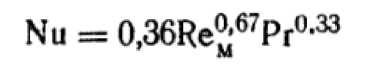 [№ 3, 390]
[№ 3, 390]
Данные для расчета:
Принимаем диаметр реактора D=1, 6 м
Диаметр мешалки d = 0, 4 м
Для реакционной массы:
Коэффициент теплопроводности X = 0, 17 Вт/м*К
Плотность раствора р= 810 кг/м3
Удельная теплоемкости с = 2, 17 кДж/кг*К = 2, 17*103Дж/кг*К
Вязкость µ = 0, 396 -10-3 н*сек/м2
Число оборотов мешалки n =170 об/мин = 2, 85 об/сек