
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
гидрокарбонатная, гемоглобиновая/ окигемоглобиновая, гидрофосфатная, белковая.
|
|
Все эти системы имеются в крови, где с их помощью особенно строго поддерживается рН = 7, 35-7, 45, несмотря на поступление в нее из кишечника и тканей значительного количества кислот и небольшой – оснований.
Гидрокарбонатная буферная система наиболее важна в поддержании постоянства рН крови. Емкость этого буфера составляет более половины всей буферной емкости крови. Составные части этого буфера – угольная кислота (Н2СО3) и ионы бикарбоната (НСО3‑ ).
В этой системе донором протона является угольная кислота Н2СО3, а акцептором протона - гидрокарбонат – ион НСО3‑ .
Уравнение Гендерсона – Хассельбаха для гидрокарбонатной буферной системы можно записать следующим образом
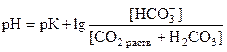
Механизм действия гидрокарбонатной буферной системы
Н+ + НСО3- ® Н2СО3 ОН‑ + Н2СО3 ® НСО3‑ + Н2О
Главное назначение гидрокарбонатного буфера заключается в нейтрализации кислот.
Гидрофосфатная буферная система содержится как в крови, так и во внутриклеточной жидкости других тканей, особенно почек. В клетках она представлена К2НРО4 и КН2РО4, а в плазме крови и межклеточной жидкости Nа2НРО4 и NаН2РО4. Роль донора протона в этой системе играет ион Н2РО4‑ , а акцептора протона - ион НРО42-. Работа гидрофосфатной буферной системы описывается уравнением буферного действия:
рН =рК + lg(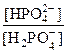 )
)
Механизм действия гидрофосфатной буферной системы
ОН‑ + H2PO4– ® НPО42– + Н2О Н+ + НPО42– ® H2PO4–
Гемоглобиновая буферная система является сложной буферной системой эритроцитов, которая включает в качества донора протона две слабые кислоты: гемоглобин ННb и оксигемоглобин ННbО2. Роль акцептора протона играют сопряженные этим кислотам основания, т.е. их анионы Нb- и НbО2-.
Механизм буферного действия гемоглобиновой системы:
Н+ + Нb-«ННb ОН- + ННb «Нb- + Н2О
Механизм буферного действия оксигемоглобиновой системы:
Н+ + НbО2- «ННbО2 ОН- + ННbО2 «НbО2- + Н2О
Белковые (протеиновые) буферные системы находятся в крови.
Механизм буферного действия белковой системы:
NН2 - Рrot –СООН + Н+ Û NН3+ - Рrot –СООН
NН2 - Рrot –СООН + ОН- Û NН2 - Рrot –СОО- + Н2О