
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Стадии 2,3. Конверсия метана
|
|
Конверсию метана водяным паром проводят в 2 стадии (ступени) в газовой фазе на никелевом катализаторе. Первая ступень конверсии проводится в трубчатом каталитическом реакторе (рис.2), а вторая – в адиабатическом шахтном реакторе (рис.3). На каждой из двух стадий конверсии возможны реакции:
1) СН4+Н2О↔ 3Н2+СО (Q = –206 кДж/моль)
2) СО+Н2О↔ Н2+СО2 (Q = 41 кДж/моль)
Равновесие в эндотермической реакции 1 при низком давлении и высокой температуре смещено вправо, а в реакции 2 при тех же условиях – влево. Вначале необходимо обеспечить максимальное превращение в реакции (1), поэтому оптимальными являются низкое давление и высокая температура, однако для синтеза в целом низкое давление невыгодно. Расчет показывает, что Ропт=40 атм.
Соотношение реагентов. Из реакций 1, 2 видно, что стехиометрическое соотношение СН4 : Н2О составляет 1: 2. Но термодинамические расчеты показывают, что при этом соотношении под давлением 40 атм даже при 10300С полное превращение метана не достигается. Двойной избыток пара (СН4: Н2О=1: 4) повышает равновесный выход до 99%.
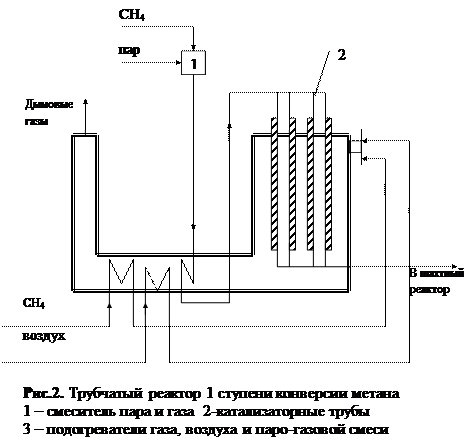 Температура Для проведения реакции 1 нужна высокая температура, что обусловлено как термодинамикой, так и кинетикой реакции. Никелевый катализатор конверсии активен при высокой температуре. Реакцию проводят в трубчатой печи, катализатор находится в трубках, а в межтрубном пространстве сжигают природный газ. Материал труб конвертора выдерживает нагрев до 9300, при этом максимальная температура в слое катализатора будет ниже 8000. Степень превращения при этом составит всего 75%. Следовательно, нужна 2-я ступень конверсии.
Температура Для проведения реакции 1 нужна высокая температура, что обусловлено как термодинамикой, так и кинетикой реакции. Никелевый катализатор конверсии активен при высокой температуре. Реакцию проводят в трубчатой печи, катализатор находится в трубках, а в межтрубном пространстве сжигают природный газ. Материал труб конвертора выдерживает нагрев до 9300, при этом максимальная температура в слое катализатора будет ниже 8000. Степень превращения при этом составит всего 75%. Следовательно, нужна 2-я ступень конверсии.

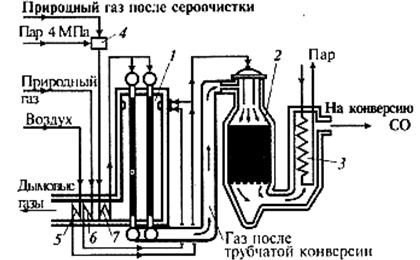 Вторую стадию конверсии метана проводят в адиабатическом шахтном реакторе с фильтрующим (неподвижным) слоем Ni катализатора. В реактор подают воздух, служащий источником азота для синтеза аммиака. Его количество рассчитывают так, чтобы в АВС соотношение N2: Н2 составило 1: 3. Реакционная смесь содержит Н2, а также другие горючие газы – метан, СО, которые сгорают, окисляясь кислородом, поступающим с воздухом. Весь кислород воздуха расходуется на горение. В результате температура в реакторе повышается до 1000оС. Давление в шахтном реакторе снижается до 33 атм из-за потерь на гидравлические сопротивления реакторов и слоев катализатора, к тому же смесь разбавляется инертным газом – азотом. Эти факторы смещают равновесие в реакции 1, и степень превращения достигает 99, 5%. Теплота реакции используется в котлах-утилизаторах для получения пара.
Вторую стадию конверсии метана проводят в адиабатическом шахтном реакторе с фильтрующим (неподвижным) слоем Ni катализатора. В реактор подают воздух, служащий источником азота для синтеза аммиака. Его количество рассчитывают так, чтобы в АВС соотношение N2: Н2 составило 1: 3. Реакционная смесь содержит Н2, а также другие горючие газы – метан, СО, которые сгорают, окисляясь кислородом, поступающим с воздухом. Весь кислород воздуха расходуется на горение. В результате температура в реакторе повышается до 1000оС. Давление в шахтном реакторе снижается до 33 атм из-за потерь на гидравлические сопротивления реакторов и слоев катализатора, к тому же смесь разбавляется инертным газом – азотом. Эти факторы смещают равновесие в реакции 1, и степень превращения достигает 99, 5%. Теплота реакции используется в котлах-утилизаторах для получения пара.