
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Кинетика и катализ. 1. При определении скорости химической реакции концентрация веществ измеряется в:
|
|
1. При определении скорости химической реакции концентрация веществ измеряется в:
а)  б)
б)  в)
в)  г)
г) 
2. По какой формуле можно вычислить среднее значение скорости реакции:
а) V=+ 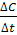 б) V= -
б) V= - 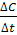 в)
в) 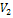 =
=  · γ г) V=k ·
· γ г) V=k · 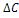
3. Для реакции  +
+  2AB укажите кинетическое управление прямого процесса:
2AB укажите кинетическое управление прямого процесса:
а) V=k 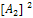 б) V=k
б) V=k 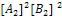 в) V=k[
в) V=k[ 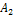 ][
][ 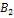 ] г) V=k[AB]
] г) V=k[AB]
4. Назовите автора принципа смещения химического равновесия:
а) Лавуазье б) Ле-Шателье в) Ломоносов г) Бекетов
5. Как повлияет на состояние равновесия реакции 2  +
+ 
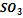 +198 кДж
+198 кДж
понижение температуры:
а) сместиться влево б) сместиться вправо
в) равновесие не сместиться
г) скорость обратной реакции уменьшиться, а прямой – нет
6. Какие факторы сместят вправо равновесие реакции FeO + Н2 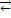 Fe + Н2О + Q:
Fe + Н2О + Q:
а) повышение температуры б) понижение температуры
в) повышение давления г) уменьшение концентрации водяных паров
7. Какие реакции называют реакциями замещения? Приведите пример данной реакции.
8. Среди данных реакций укажите реакции замещения:
а)  б)
б) 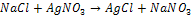
в)  г)
г) 
9. Как измениться скорость реакции 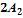 +
+  =2
=2  В при уменьшении концентрации вещества А в 2 раза:
В при уменьшении концентрации вещества А в 2 раза:
а) уменьшится в 4 раза б) уменьшится в 2 раза
в) не изменится г) увеличится в 4 раза
10. Какие реакции называют реакциями разложения? Приведите пример данной реакции.
11. Во сколько раз изменится скорость реакции, если температуру реакции понизить с 90 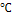 до 60
до 60 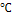 ? Температурный коэффициент равен 3. Приведите ход решения задачи.
? Температурный коэффициент равен 3. Приведите ход решения задачи.
12. При взаимодействии 13г Zn с хлоридной кислотой выделяется 40 кДж теплоты. Запишите термохимическое уравнение данного процесса. Приведите ход решения задачи.