
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Особенности кинетики гетерогенных реакций
|
|
В отличие от гомогенных реакций, гетерогенные протекают на поверхности раздела между реагентами, поэтому скорость гетерогенных реакций зависит, кроме рассмотренных уже для гомогенных реакций факторов, еще от величины поверхности раздела, а также скоростей диффузии реагентов в зону реакции и продуктов реакции из этой зоны. В кинетическое уравнение для гетерогенной реакции записываются только концентрации веществ, находящихся в жидком или газообразном состоянии. Концентрация твердого компонента и величина его поверхности (остающиеся практически неизменными при определении истинной скорости) учитываются величиной константы скорости гетерогенной реакции. Для реакции
аА(т) + bB(г) → dD(г)
кинетическое уравнение имеет вид:
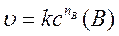
где k - константа скорости гетерогенной реакции; nB - порядок реакции по газообразному или растворенному компоненту.
Гетерогенный химический процесс всегда включает диффузионные стадии (подвод реагентов и отвод продуктов реакции) и кинетические (адсорбция реагентов, собственно химическое взаимодействие и десорбция продуктов), следовательно, его скорость может определяться как скоростью кинетических стадий (кинетический режим), так и скоростью диффузионных стадий (диффузионный режим). Кинетический режим наиболее вероятен при невысокой температуре, а при высоких температурах скорость реакции возрастает быстрее, чем скорость диффузии, поэтому течение гетерогенной реакции переходит в диффузионный режим.