
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Используя метод стационарных концентраций, определите, каков порядок этой реакции по пероксиду водорода.
|
|
Решение. Согласно методу стационарных концентраций
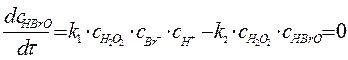 |
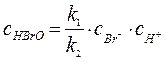 |
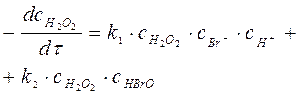 |
Скорость реакции по пероксиду водорода может быть выражена следующим образом:
После подстановки с НВrО в полученное уравнение имеем:
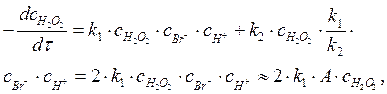 |
где А = const, т. к. концентрация ионов брома, как катализатора не должна существенно изменяться, как и концентрация ионов водорода в кислой среде.
Таким образом, порядок этой реакции по пероксиду водорода равен единице (показатель степени при концентрации Н2О2 в кинетическом уравнении).
10. При исследовании кинетики реакции распада диметилового эфира были
получены следующие данные:
| Время, с (t) | ¥ | ||||
| Повышение давления, Па (D р × 10-4) | 1, 28 | 2, 35 | 3, 33 | 6, 23 | 8, 25 |
Начальное давление диметилового эфира 4, 16× 104 Па. Рассчитайте порядок реакции и константу скорости распада диметилового эфира.
Решение. Предположим, что реакция имеет первый порядок:
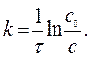
Вместо концентраций используем давления, тогда получим
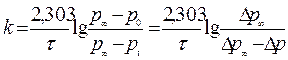 |
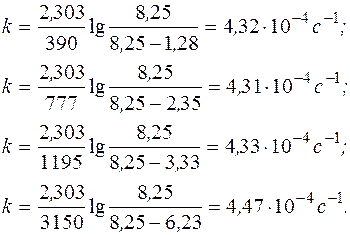 |
Подставляя соответствующие значения изменения давления со временем в полученное уравнение, рассчитаем константу скорости:
Константа скорости постоянна в пределах погрешности эксперимента, следовательно, предположение, что реакция является реакцией I-го порядка, верно.
Отсюда k ср = 4, 36× 10-4 с-1.