Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Нитрование алканов азотной кислотой (Коновалов, Хэсс)
|
|
Концентрированная азотная кислота или смесь азотной и серной кислот окисляют алканы. Нитрование протекает только под действием разбавленной азотной кислоты (уд.вес 1, 036) в жидкой фазе при температуре 120-130°С в запаянных трубках (М.И. Коновалов, 1893г.):
R-H + HO-NO2 → R-NO2 + H2O
Для нитрования Коновалов М.И. впервые использовал нонафтен
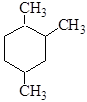
Было установлено, что легкость замещения водородного атома нитрогруппой растет в ряду:
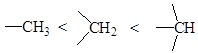
Основными факторами, влияющими на скорость реакции нитрования и выход нитросоединений, являются концентрация кислоты, температура и продолжительность процесса. Так, например, нитрование гексана проводят азотной кислотой (d 1, 075) при температуре 140°С:
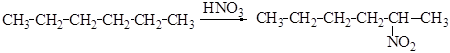
Реакция сопровождается образованием полинитросоединений и продуктов окисления.
Практическое значение получил метод парофазного нитрования алканов (Хэсс, 1936 г.). Нитрование проводят при температуре 420°С и непродолжительном пребывании углеводорода в реакционной зоне (0, 22-2, 9 сек). Нитрование алканов по Хэссу приводит к образованию смеси нитропарафинов:
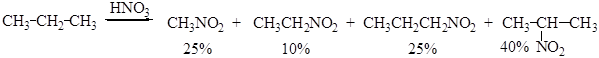
Образование нитрометана и этана происходит в результате крекинга углеводородной цепи.
Реакция нитрования алканов протекает по свободнорадикальному механизму, причем азотная кислота не является нитрующим агентом, а служит источником окислов азота NO2: