
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Взаимосвязь иммунной, эндокринной и нервной систем регуляции
|
|
Министерство сельского хозяйства
Федеральное государственное бюджетное образовательное учреждение
Высшего и профессионального образования
«Оренбургский государственный аграрный университет»
Кафедра микробиологии
И.В. Савина
Взаимосвязь иммунной, эндокринной и нервной систем регуляции
Методические указания для студентов, обучающихся по специальности «Микробиология», «Ветеринария»
Оренбург
Автор: И.В. Савина.
Методическое указание к теме, предназначенной для самостоятельного изучение: «Взаимосвязь иммунной, эндокринной и нервной систем регуляции»
Рецензент: доцент кафедры эпизоотологии и паразитологии О.В. Филлипова
Методические указания обсуждены на заседании методической комиссии факультета Ветеринарной медицины ОГАУ и рекомендованы к опубликованию (протокол № от «» «» 2011г.)
ВВЕДЕНИЕ
В ходе иммунного ответа запуск в работу многочисленного ряда только внутрисистемных факторов регуляции нередко оказывается недостаточным для поддержания гомеостаза. Следом, иногда очень быстро, в регуляторный каскад событий включаются практически все гомеостатические системы регуляции, в том числе эндокринная и нервная. Нервная и эндокринная системы участвуют в регуляции обмена веществ, защите организма от химических, физических и других факторов. Иммунная система направлена главным образом против чужеродных биологических агентов, к которым нет рецепторов у нервной и эндокринной систем. Нервная, эндокринная и иммунная системы регуляции выступают, с одной стороны, как самостоятельные, а с другой — как тесно взаимосвязанные системы (рис. 45). От того как станут взаимодействовать эти регулирующие механизмы, в значительной мере будет зависеть и величина конкретного ответа иммунной системы на конкретный антиген: ответ будет нормальным или сниженным (при иммунодефиците), или даже повышенным (перед развитием аллергии.
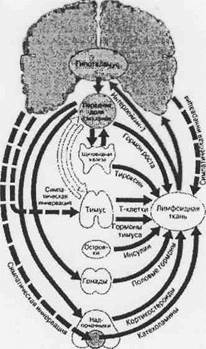
Рис. 1. Взаимодействие между нейроэидокрннной и иммунной системами
Некоторые из возможных связей между эндокринной, нервной и иммунной системами. Черными стрелками показана симпатическая иннервация, серыми — воздействие гормонов, белыми — предполагаемые связи, эффекторные молекулы для которых не установлены (А.Ройт и др., 2000)
Имеются многочисленные факты, свидетельствующие о существовании взаимосвязи трех главных систем регуляции. Прежде всего это наличие хорошо развитой симпатической и парасимпатической иннервации центральных и периферических лимфоидных органов и рецепторов к нейромедиаторам и гормонам как в лимфоидных органах, так и на отдельных иммунных лимфоцитах (к катехоламинам, холинэргическим веществам, нейро- и миелопептидам). Известно, что не только воздействие со стороны нейроэндокринной системы влияет на развитие иммунного ответа, но и изменение функциональной активности иммунной системы (сенсибилизация, стимуляция выработки лим-фокинов, монокинов) приводит к характерным сдвигам электрофизиологических показаний нейрональной активности.
В центральной нервной системе и в железах внутренней секреции имеются рецепторы к интерлейкинам, миелопептидам, гормонам тимуса пептидной природы и другим медиаторам иммунной системы, обладающим нейротроп-ным действием. О существовании тесных функциональных взаимоотношений между нервной, эндокринной и иммунной системами говорит обнаружение в них общих гормонов и медиаторов. Например, в функционировании нервной системы существенная роль принадлежит нейропептидам — эндорфинам и энкефалинам, секретируемым некоторыми нейронами головного мозга. Эти же пептиды являются составной частью, действующим началом лейкоцитарного интерферона, миелопептидов костного мозга, тимозина, некоторых медиаторов Т-хелперов. Ацетилхолин, норадреналин, серотонин образуются в нервных клетках и в лимфоцитах, соматотропин — в гипофизе и лимфоцитах. Интсрлейкин-1 продуцируется преимущественно мононуклеарными фагоцитами. Его продуцентами также являются нейтрофилы, В-лимфоциты, нормальные киллеры, клетки нейроглии, нейроны головного мозга, периферические симпатические нейроны, мозговое вещество надпочечников.
В связи с общностью структуры многих медиаторов и рецепторов к ним в различных системах регуляции, антиген в организме вызывает активацию не только иммунной системы, но и нервной и эндокринной систем, которые по принципу обратной связи могут усилить или ослабить иммунный ответ. Характер реактивности зависит от природы, иммуногенности реагентов (различных белков).
Следует, однако, подчеркнуть, что нейроэндокринные факторы могут изменить лишь интенсивность ответной реакции (усиление или ослабление), но не могут изменить специфичность иммунного ответа. Модулирующее влияние на иммунную систему возможно через холин- и адренергические волокна и окончания в лимфоидных органах, а также через функциональные специализированные рецепторы к медиаторам и гормонам на лимфоидных клетках, т. е. это влияние возможно как в индуктивную (за счет увеличения количества антителообразующих клеток), так и в продуктивную (за счет увеличения синтеза антител без увеличения количества антителообразующих клеток) стадии иммунного ответа. В частности, холинотропные препараты резко увеличивают образование антител без увеличения количества плазматических клеток, а атропин снимает этот эффект.
Комплекс нейроэндокринных факторов потенцирует иммунный ответ в адаптационную стадию стресса. При длительном же действии стрессора как специфический, так и неспецифический иммунные ответы угнетаются. При глубоком стрессе, а также при применении высоких доз гормонов, обладающих иммуносупрессорным действием (гидрокортизон и др.), при различных заболеваниях, пересадке органов и тканей резко уменьшается популяция Т-киллеров, что в десятки и сотни раз повышает риск возникновения злокачественных опухолей.
Имеются наблюдения (В. В. Абрамов, 1988) о том, что под влиянием неблагоприятных факторов внешней среды (химических, биологических и физических) возможно истощение компенсаторных, адаптационных возможностей нервной системы, в том числе \ при длительном, чрезмерном поступлении информации от иммунной системы. Это может способствовать нарушению нервной регуляции иммунологических функций и, как следствие усилению «автономности» иммунной системы, нарушению ее функций иммунологического контроля, регулирования пролиферации и дифференцировки клеток различных тканей, повышению риска опухолевого роста в этих тканях и восприимчивости к инфекционным заболеваниям, нарушению процессов оплодотворения.
Приведенные выше факты указывают на то, что нормальное функционирование иммунной системы возможно лишь при нормальном функционировании нервной и эндокринной систем регуляции и при тесном их взаимодействии с иммунной системой.
Формирование нейроэндокринноиммунных взаимодействий закладывается уже в раннем онтогенезе. Большинство млекопитающих рождаются примерно с одинаковой степенью зрелости иммунной и нервной систем. Центральным звеном, координирующим нейроэндокринноиммунное взаимодействие, является гипоталамо-гипофизарная система, осуществляющая в пренатальном онтогенезе не только регуляторную, но и морфогенетичес-кую функцию, контролируя созревание иммунной системы и включение ее в регуляцию иммунологических функций. В частности, выраженность эндокринной функции гипофиза плода коррелирует с массой тимуса и созреванием в нем лимфоцитов (Л.А.Захаров, М. В. Угрюмов, 1998).
В постнатальный период завершается формирование нейроэндокринно-иммунных взаимодействий. Для сохранения динамического гомеостаза (в том числе иммунного) в организме животных нервная, иммунная и эндокринная системы объединяются в общую нейроиммунно-эндокринную систему. В этой системе они взаимодействуют по принципу взаимной регуляции, осуществляемой нейромедиаторами, неиропептидами, трофическими факторами, гормонами, цитокинами через соответствующий рецепторный аппарат.
Уникальность иммунной системы состоит в том, что она может участвовать во взаимной регуляции не только за счет продуцирования молекул цито-кинов, гормонов и антител, но и путем непрерывной циркуляции подвижных элементов этой системы — иммунокомпетентных лимфоцитов и вспомогательных (макрофаги и др.) клеток. Клетки иммунной системы могут одновременно выполнять рецепторные, секреторные и эффекторные функции и, обладая подвижностью, мобильно осуществлять свою цензорную, регуляторную и защитную роль в то время и в том месте организма, когда, где и с какой интенсивностью это требуется. Интенсивность и продолжительность иммунного ответа определяются как иммунной, так и другими системами регуляции.
У взрослых животных в реакцию организма на внедрение антигена вовлекаются гипоталамус, гиппокамп, миндальное ядро, холинергические, норадренергические, серотонинергические, дофаминергические нейроны некоторых других отделов мозга. Высшие отделы центральной нервной системы также способны влиять на состояние иммунной системы, в частности, показана возможность условно-рефлекторной стимуляции или угнетения иммунного ответа.
Ключевым звеном аппарата нервной регуляции иммунной системы является гипоталамус, а влияние других отделов мозга опосредуется гипоталамусом. Гипоталамус получает информацию о нарушении антигенного гомеостаза сразу же после внедрения иммуногена в организм от рецепторно-го аппарата иммунокомпетентных клеток через различные нейротрансмит-терные и нейрогормональные системы. Эти системы взаимосвязаны и дублируют активирующие и тормозящие нейрорегуляторные влияния на функции иммунологической защиты, что повышает надежность иммунорегуля-торного аппарата и обеспечивает возможность компенсации нарушений отдельных его звеньев (Г. Н. Кржыжановский, С. В. Мачаева, С. В. Макаров, 1997).
Гипоталамус участвует в регуляции иммунного ответа через симпатическую и парасимпатическую иннервации органов иммунной системы, а также посредством продукции нейрогормонов (либеринов и статинов), стимулирующих или ингибирующих синтез гормонов в аденогипофизе. Известны следующие регуляторные «оси»:
гипоталамус —> гипофиз —> тимус;
гипоталамус —> гипофиз -> щитовидная железа;
гипоталамус —> гипофиз —> кора надпочечников;
гипоталамус —> гипофиз —> половые железы.
Через эти «оси» гипоталамус влияет на синтез гормонов соответствующих желез, а через них — на иммунную систему.
Центральные и периферические органы иммунной системы иннерви-руются холинергическими, норадренергическими, серотонинергическими проводящими путями и пептидергическими волокнами, содержащими ме-тэнкефалин, субстанцию Р и другие нейропептиды.
Нервные окончания в тимусе, костном мозге, селезенке, лимфатических узлах и других лимфоидных органах приближаются к лимфоцитам на расстояния, сравнимые с таковыми для их контактов с мышечными и сосудистыми клетками. Лимфоциты и макрофаги вступают в непосредственный контакт с нервными волокнами и своими собственными рецепторами воспринимают нейрорегуляторные влияния (А. А. Ярилин, 1999).
Регуляторные факторы могут проникать в лимфоидные органы и гуморальным путем. Т-, В-лимфоциты, макрофаги и их предшественники могут вступать в контакт и с гуморальными регуляторными факторами, так как имеют рецепторы ко многим нейромедиаторам, нейропептидам, нейрогормонам и гормонам эндокринных желез. Так, например, известно, что Т- и В-лимфоциты имеют рецепторы к норадреналину, адреналину, ацетилхолину, серотони-ну, вазопрессину, глюкокортикоидам, b-эндорфину, фактору роста нервов, тиротропину; ЕК-клетки — к γ -эндорфину, норадреналину; макрофаги — к норадреналину, адреналину, субстанции Р, b-эндорфину, глюкокортикоидам. Количество рецепторов, экспрессированных на поверхности лимфоцитов и макрофагов, резко повышается при активации лимфоцитов антигеном. Например, у стимулированных антигеном макрофагов экспрессируется до 40 тыс. рецепторов, связывающих кортикостероиды.
Присоединение соответствующего лиганда к рецепторам стимулирует в клетках иммунной системы комплекс циклазных ферментов, которые включают последующие, характерные для каждого типа клеток внутриклеточные процессы.
Для функционирования иммунной системы исключительно важное значение имеет уровень секреции пептидных гормонов (тимозин, тимолин, Т-акти-вин и др.) эпителиальными клетками тимуса: их уменьшение в крови снижает способность Т-лимфоцитов к активации (в частности, к выработке ИЛ-2) и, как следствие, к снижению интенсивности иммунного ответа. Секрецию тимусных гормонов стимулируют прогестерон, соматотропин, пролактин, подавляют— глюкокортикоиды, андрогены, эстрогены. Ацетилхолин и холинергические стимулы в тимусе способствуют пролиферации и миграции тимоцитов, а сигналы, принимаемые b-адренорецепторами, подавляют пролиферацию лимфоцитов и повышают их дифференцировку.
Медиаторы вегетативной нервной системы и гормоны могут оказывать действие, подобное действию на тимус, на иммунную систему в целом, а именно: холинергические стимулы активизируют, а адренергические угнетают иммунную систему. Тироксин усиливает пролиферацию и дифферецировку лимфоцитов; инсулин — пролиферацию Т-клеток; а-эндорфин стимулирует гуморальный иммунный ответ, р-эндорфин — клеточный, но подавляет гуморальный. Кортикостероиды индуцируют апоптоз тимоцитов и других покоящихся лимфоцитов, особенно в стадии отрицательной селекции, снижают секрецию цитокинов и гормонов тимуса; кортикотропин снижает количество лимфоцитов циркулирующей крови и их функциональную активность; катехоламины (адреналин и норадреналин) подавляют пролиферацию и усиливают дифференцировку лимфоцитов (особенно Т-хелперов) и их миграцию в лимфатические узлы.
Гормоны и цитокины, образующиеся в тимусе и в отдельных клетках иммунной системы, в свою очередь, могут влиять на активность эндокринной и нервной систем. Изменения электрической активности гипоталамических структур, наступающие при поступлении антигена в организм, сохраняются на протяжении всего периода индуктивной и продуктивной фаз иммунного ответа, с изменением ультраструктуры нейронов, синапсов, астроцитов, уровня окситоцина, вазопрессина, дофамина, норадреналина, серотонина в различных отделах мозга. Гормоны тимуса — тимопоэтин и ИЛ-1, продуцируемые фагоцитами, В-лимфоцитами, ЕК-клетками, усиливают секрецию глюкокортикоидов, тем самым ограничивая (подавляя) иммунный ответ.
В осуществлении взаимосвязи нервной, эндокринной и иммунной систем регуляции по поддержанию динамического, в том числе иммунного, го-меостаза важная роль принадлежит опиоидным пептидам, в секреции которых участвуют клетки всех трех основных систем регуляции.
Нейроны, иммунокомпетентные клетки, клетки гипофиза и некоторых других эндокринных желез не только синтезируют идентичные физиологически активные вещества, но и имеют идентичные к ним рецепторы. Так, например, в костном мозге, тимусе, селезенке, стимулированных Т-лимфоцитах (в том числе в Т-хелперах), в макрофагах обнаружены регулируемый ген про-опиокортина, идентичный гену некоторых секреторных клеток гипофиза, а также м-РНК, отражающая его структуру. Из проопиокортина, состоящего из 134 аминокислотных остатков, при ограниченном протеолизе образуется кортикотропин (АКТГ), в состав которого входят 39 аминокислотных остатков и |3-липотропин, насчитывающий у свиньи и овцы 91 аминокислотный остаток (Т. Т. Березов, Б. Ф. Коровкин, 1998). У свиньи и овцы молекулы (3-ли-потропина имеют одинаковое количество аминокислотных остатков, но существенно различаются в последовательности аминокислот. Однако последовательности аминокислот с 61 по 91 у всех исследованных видов животных и у человека одинаковы, и при специфическом протеолизе липотропина из них образуются (в ткани мозга, аденогипофизе, иммунокомпетентных клетках и макрофагах) биологически активные пептиды, обладающие опиотоподобным действием: метэнкефалин (61 — 65), a-эндорфин (61 — 76), γ -эндорфин (61—77), d-эндорфин (61-79), b-эн-дорфин (61 —91). Все они принимают участие (как медиаторы) в нейроэндокринноиммунных взаимодействиях и, подобно морфину, снимают болевые ощущения.
Суммарная активность синтезируемых в лимфоидной системе опиоидов сравнима с активностью наиболее интенсивного их продуцента — гипофиза, причем процессинг проопиокортина в гипофизе и лимфоцитах осуществляется одинаково.
Эффект от взаимодействия какого-либо из опиоидных пептидов с рецепторами различных клеток может быть различным в зависимости от того, на какой ответ запрограммирована та или иная клетка при активации данного рецептора. Например, b-эндорфин нейронального, костномозгового, лимфо-цитарного происхождения (т.е. независимо от происхождения), связавшись с опиоидными рецепторами центральной нервной системы, оказывает анальгетический эффект, а воздействуя на лимфоциты, вызывает (в зависимости от дозы) изменение величины иммунного ответа, активирует ЕК-клетки, повышает синтез ИЛ-2 и его экспрессию на Т-лимфоцитах, а также стимулирует хемотаксис макрофагов и других лейкоцитов. В свою очередь, ИЛ-1 и ИЛ-2 повышают экспрессию генов проопиокортина в клетках гипофиза и секрецию ими эндорфина (Г. Н. Кржыжановский и др., 1997).
Помимо опиоидных пептидов в осуществлении нейроэндокринно-иммунных взаимодействий участвуют и другие биологически активные вещества, в том числе ацетилхолин, норадреналин, серотонин, дофамин, гипоталамические либерины, соматотропин, кортикотропин, нейротензин, вазопрессин. интерлейкины и пр. Гормон тимуса (тимозин) воспринимается нейрональными структурами, вызывая у животных изменение поведенческих реакций, стимулирует активность регуляторных систем гипоталамус — гипофиз — кора надпочечников, гипоталамус — гипофиз — гонады, в гипофизе стимулирует секрецию эндорфинов, в иммунной системе — иммунный ответ.
Таким образом, нервная, эндокринная и иммунная системы работают по принципу взаиморегуляции, которая обеспечивается комплексом связанных между собой механизмов, в том числе участием дублирующих факторов регуляции. Эти механизмы регуляции действуют на клеточном, системном и межсистемном уровнях, обеспечивая высокую степень надежности нейро- эндокринно-иммунологических процессов регуляции.
В то же время высокий уровень реактивности всех систем регуляции и сложность организации их аппарата являются факторами риска развития иммунологических, неврологических и эндокринных расстройств, так как при патологии одной системы повышается риск расстройства других систем. В частности, нарушения нейроэндокринных механизмов регуляции могут играть важную роль в патогенезе иммунологических расстройств, а иммунологические механизмы могут участвовать в патогенезе нервных и эндокринных болезней. При срыве компенсаторных механизмов может возникнуть сочетанная патология нервной, эндокринной и иммунной систем независимо от первичной локализации патологического процесса в той или иной системе (Г. Н. Кржыжановский и др., 1997).
Вопросы для самоконтроля:
1. Перечислите факты, свидетельствующие о существовании взаимосвязи трех главных систем регуляции.
2. Как действуют на иммунную систему эндокринные факторы?
3. Как происходит формирование нейроэндокриноиммунных взаимодействий в онтогенезе?
4. В чем состоит уникальность иммунной системы?
5. Каково значение уровня секреции пептидных гормонов для функционирования иммунной системы?
6. К чему приводит высокий уровень реактивности всех систем регуляции?
Список использованной литературы:
1. Балаболкин М.И. Эндокринология, - Универсум паблишинг. - М., 1998 – 584 с.
2. Воронин Е.С. Иммунология. – М.: Колос-Пресс, 2002.- 408 с.
3. Иммунология: Учеб. для студентов вузов/В.Г. Галактионов.- 3-е изд., испр. и доп. – М.: Издательский центр «Академия», 2004. – 528 с.
4. Сапин М.Р., Этинген Л.Е. Иммунная система человека. – М.: Медицина, 1996. – 304с.
|