
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Дата: 08.05.13
|
|
Пропись № 1 Rp.: Sol. Аtropini sulfatis 0, 1 %-10 ml
D. S. По 5 - 8 капель внутрь 2 - 3 раза в день перед едой.
Состав: Атропина сульфата 0, 1
Натрия хлорида 0, 08
Воды очищенной 10 мл
Описание: на анализ поступила бесцветная прозрачная жидкость без запаха и механических включений в прозрачном бесцветном флаконе.
ОПРЕДЛЕНИЕ ПОДЛИННОСТИ:
Натрия хлорид: см пропись №1 за 24.04.13г.
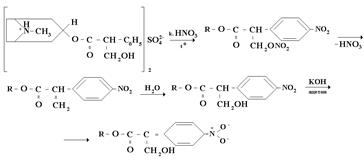 Атропина сульфат:
Атропина сульфат:
1)
2) [атропин]2 SO42- + BaCl2 =Ba2SO4 +[атропин] +2HCl
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ:
Атропина сульфат алкалиметрия.
[атропин]2 SO42- + NaOH =Na2SO4 +[атропин] +H2O f=1
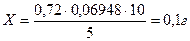 T = 0, 1*694, 8/1000 = 0, 06948 г/мл
T = 0, 1*694, 8/1000 = 0, 06948 г/мл
0, 1 – 10 мл
х - 5мл; аф=0, 05
Vтеор. = аф / T = 0, 05/0, 06948 = 0, 72мл
Vпр=0, 72
Расчет отклонения:
Относит.ошибка: 0% (по П №305 допустимо 15%).
Натрия хлорид (аргентометрически методом Мора). Метод основан на способности натрия хлорида реагировать с серебра нитратом с образованием серебра хлорида.
1 мл ЛФ прибавляют титруют 0, 1 моль/л раствором серебра нитрата до оранжево-желтого цвета.
NaCl + AgNO3 → AgCl↓ бел. + NaNO3 f=1
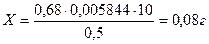 T = 0, 1*58, 44/1000 = 0, 005844
T = 0, 1*58, 44/1000 = 0, 005844
0, 08 – 10мл
х - 0, 5мл; аф=0, 004
Vтеор. = аф / T = 0, 004/0, 005844 = 0, 68
Vпр=0, 68
Расчет отклонения:
Относит.ошибка: 0% (по П №305 допустимо 15%).
Заключение: Данная лекарственная форма приготовлена удовлетворительно
Пропись № 2 Sol. Hydrogenii peroxydi 3% - 50 ml
Раствор перекиси водорода 3%-50мл
Описание: Представляет собой бесцветную, прозрачную жидкость со слабым своеобразным запахом. Общий объем 50мл.
ОПРЕДЛЕНИЕ ПОДЛИННОСТИ:
3) К 1 мл исследуемого раствора прибавляют 2 капли разведенной серной кислоты и по каплям раствор калия перманганата. Раствор калия перманганата обесцвечивается.
5H2O2 + 2KMnO4 + 3H2SO4 → 5O2 +K2SO4 + 2MnSO4 + 8 H2O
4) 1 мл препарата подкисляют 4 каплями разведенной серной кислоты, прибавляют 2 мл эфира и 4 капли раствора бихромата калия и взбалтывают, эфирный слой окрашивается в синий цвет.
K2Cr2O7 + H2SO4 → H2Cr2O7 + K2SO4
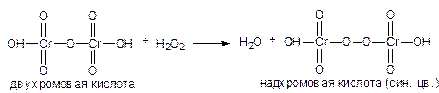
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ:
Перманганатометрический метод – основан на восстановительных свойствах перекиси водорода.
К 0, 1 мл ЛФ прибавляют 5 мл разведенной серной кислоты и титруют 0, 1 моль/л раствором калия перманганата до слабо розового окрашивания.
5H2O2 + 2KMnO4 + 3H2SO4 → 5O2 +K2SO4 + 2MnSO4 + 8 H2O
f = ½
Mmэкв. = 34, 02*1/2 = 17, 01
T = 0, 1*17, 01/1000 = 0, 001701г/мл
Vтеор. = 0, 003/0, 001701= 1, 76мл
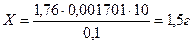 (по ГФ X допустимо отклонение 5, 7-6, 3%).
(по ГФ X допустимо отклонение 5, 7-6, 3%).
Заключение: Данная лекарственная форма приготовлена удовлетворительно.