
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Теория метода. Федеральное агентство по образованию Российской Федерации
|
|
Федеральное агентство по образованию Российской Федерации
Филиал «Севмашвтуз» государственного образовательного учреждения высшего профессионального образования «Санкт – Петербургский государственный морской технический университет»
В г. Северодвинске
Факультет: № 4
Кафедра: № 12
Лабораторная работа
ОПРЕДЕЛЕНИЕ МОЛЕКУЛЯРНОЙ МАССЫ И ПЛОТНОСТИ ГАЗА
МЕТОДОМ ОТКАЧКИ
Северодвинск
Лабораторная работа ФПТ 1-12
ОПРЕДЕЛЕНИЕ МОЛЕКУЛЯРНОЙ МАССЫ И ПЛОТНОСТИ ГАЗА
МЕТОДОМ ОТКАЧКИ
ЦЕЛЬ И МЕТОД РАБОТЫ
С помощью метода взвешивания колбы, наполненной воздухом под разными давлениями, при неизменных температуре и объеме определить молекулярную массу и плотность газа.
ТЕОРИЯ МЕТОДА
Молекулярной (молярной) массой называется масса одного моля вещества. В единицах СИ эта величина измеряется в килограммах на моль. Молем какого-либо вещества называется количество этого вещества, содержащее столько же структурных элементов (молекул, атомов и т.д.), сколько атомов содержится в 0, 012 кг изотопа углерода 12С. Молекулярную массу газа можно определить из уравнения газового состояния.
При не очень высоких давлениях, но достаточно высоких температурах газ можно считать идеальным. Состояние такого газа описывается уравнением Менделеева-Клаперона:
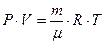 (1)
(1)
где Р - давление газа; V - объем газа, m - масса газа; 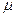 - молярная масса газа, R = 8, 31 Дж/(мольК) — универсальная газовая постоянная; Т — абсолютная температура газа.
- молярная масса газа, R = 8, 31 Дж/(мольК) — универсальная газовая постоянная; Т — абсолютная температура газа.
Из уравнения (1) можно получить формулу для молярной массы газа:
 (2)
(2)
Если измерение давления Р, объема V, температуры Т газа, то есть параметров газа, входящих в формулу (2) не вызывает особенных трудностей, то определение массы газа выполнить практически невозможно, так как взвешивание газа возможно только вместе с колбой. в которой он находится. Поэтому для определения 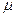 необходимо исключить массу сосуда. Это можно сделать, рассмотрев уравнение состояния двух масс m1 и m2 одного и того же газа при неизменных температуре Т и объеме V.
необходимо исключить массу сосуда. Это можно сделать, рассмотрев уравнение состояния двух масс m1 и m2 одного и того же газа при неизменных температуре Т и объеме V.
Пусть в колбе объемом V находится газ массой m1 при давлении Р, и температуре Т. Уравнение состояния (1) для этого газа имеет вид
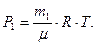 (3)
(3)
Откачаем часть газа из колбы, не изменяя его температуры. После откачки масса газа, что оставалась в колбе, и его давление уменьшились. Обозначим их соответственно m1 и Р и снова запишем уравнение состояния

 (4)
(4)
Из уравнений (12.3) и (12.4) получим:

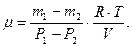
 (5)
(5)
Полученная формула (12.5) дает возможность определить 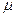 , если известно изменение массы газа (но не сама масса), а также изменение давления, температура и объем газа.
, если известно изменение массы газа (но не сама масса), а также изменение давления, температура и объем газа.
В данной работе исследуемым газом является воздух, который представляет собой смесь азота, кислорода, аргона и других газов.
Формула (5) пригодна и для определения 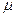 смеси газов. Найденное в этом случае значение и представляет собой некоторую среднюю или эффективную молярную массу смеси газов. Молярная масса смеси газов может быть рас считана и теоретически, если известно процентное содержание и молярная масса каждого из газов, входящих в состав смеси, по формуле
смеси газов. Найденное в этом случае значение и представляет собой некоторую среднюю или эффективную молярную массу смеси газов. Молярная масса смеси газов может быть рас считана и теоретически, если известно процентное содержание и молярная масса каждого из газов, входящих в состав смеси, по формуле
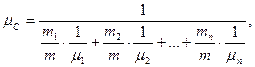 (6)
(6)
где  - относительное содержание каждого газа:
- относительное содержание каждого газа: 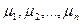 - молекулярные массы газов.
- молекулярные массы газов.
Если известна молярная масса газа, то можно легко определить еще одну важную характеристику газа - его плотность 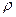 . Плотность газа - это масса единицы объема газа:
. Плотность газа - это масса единицы объема газа:
 (7)
(7)
Определив 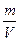 из уравнения Менделеева-Клаперона, получим
из уравнения Менделеева-Клаперона, получим
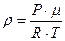 (8)
(8)
Плотность смеси газов можно вычислить по формуле (8), подразумевая под 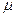 эффективную молярную массу смеси.
эффективную молярную массу смеси.