
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Реакции переаминирования (трансаминирование). Связан с ферментами аминотрансферазами.
|
|
РЕАКЦИИ ДЕКАРБОКСИЛИРОВАНИЯ АК.
НЕВИТАМИНЫЕ КОФРМЕНТЫ:
Не содержат в своём составе витаминов, но участвуют в каталитических превращениях.
1.НУКЛЕОТИДЫ: АТФ, ЦТФ (синтез ФОСФОЛИПИДОВ); УДФ, УТФ, ГТФ (синтез
ГЛИКОГЕНА).
2.ПРОИЗВОДНЫЕ ПОРФИРИНА: ГЕМ, ЦИТОХРОМЫ, КАТАЛАЗА.
3.ПЕПТИДЫ:
ГЛУТАТИОН - ТРИПЕПТИД, содержащий ГЛУ-ЦИС-ГЛИ. Он связан с ферментами ОКСИДОРЕДУКТАЗАМИ. Участвует в окислительно-восстановительных реакциях.
ИОНЫ РАЗЛИЧНЫХ МЕТАЛЛОВ.
Лекция № 4.
ФЕРМЕНТЫ (продолжение).
СВОЙСТВА ФЕРМЕНТОВ.
МЕХАНИЗМ ДЕЙСТВИЯ ФЕРМЕНТОВ.
З.МОЛЕКУЛЯРНЫЕ ЭФФЕКТЫ ФЕРМЕНТАТИВНЫХ РЕАКЦИЙ.
СВОЙСТВА ФЕРМЕНТОВ.
Высокая каталитическая активность. УРЕАЗА повышает скорость реакции в 10 раз.
Ферменты, являясь белками, проявляют ТЕРМОЛАБИЛЬНЫЕ свойства - чувствительность к изменению температуры.
При повышении температуры на каждые 10 градусов, скорость ферментативных реакций повышает в 1, 5-2 раза (правило ВАНТ - ГОФФА). Это правило применимо для ферментов в очень узком интервале температуры, т.к. уже при 50-60 градусах наблюдается денатурация, а при 100 гр. - полная денатурация с потерей активности. При 1-3 гр. Активность фермента также понижается, но при понижении температуры структура его сохраняется, поэтому при последующем повышении Т. активность восстанавливается. Это свойство используется в клинической практике при проведении оперативных вмешательств. Температура, при которой фермент проявляет максимальную активность, называется ОПТИМАЛЬНОЙ.
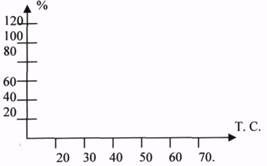
3.Ферменты чувствительны к изменениям РН среды. Для большинства ферментов оптимальные значения РН лежат в нейтральной среде (для КАТАЛАЗЫ РН=7).
Есть ферменты, для которых оптимальные значения РН лежат в кислой среде (пепсин РН=1, 5-2, 5). Некоторые ферменты проявляют активность в щелочной среде (АРГИНАЗА РН=10-11). Изменения РН приводит к изменению степени ионизации кислых и основных групп в активном центре фермента, т.к. эти группы участвуют в связывании субстрата и его превращении. Изменение РН приводит к конформационной перестройке не только активного центра фермента, но и всей молекулы фермента. Это может сопровождаться нарушением третичной структуры фермента. При оптимальном значении РН функциональные группы активного центра находятся в наиболее реакционно-способном состоянии, и это обеспечивает образование фермент-субстратного комплекса.
4.Специфичность действия ферментов. В основе специфичности действия ферментов лежит КОНФОРМАЦИОННОЕ соответствие его активного центра молекуле субстрата. Различают следующие виды специфичности: