
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Обработка результатов измерений. 1. Вычислите значения давлений по формулам
|
|
1. Вычислите значения давлений по формулам
 ,
,  ,
, 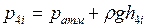 ,
,
где ρ =103 кг/м 3 – плотность воды (жидкости в манометре)
g =9, 8· м/с 2 – ускорение свободного падения.
Полученные значения занесите в таблицу.
2. При установившемся состоянии 2 имеют место равенства 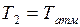 и
и 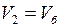 , а при установившимся состоянии 4 –
, а при установившимся состоянии 4 –  и
и 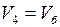 . Учитывая, что для воздуха i =5, из уравнения (10.17) получим формулы для определения изменения энтропии при изохорическом охлаждении:
. Учитывая, что для воздуха i =5, из уравнения (10.17) получим формулы для определения изменения энтропии при изохорическом охлаждении:
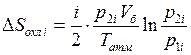 ,
,
и при изохорическом нагревании:
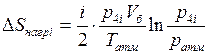 .
.
По полученным формулам рассчитайте для каждого опыта изменение энтропии и данные занесите в таблицу.
3. Для изменения энтропии при охлаждении и нагревании определите соответствующие средние значения 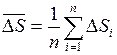 . Оцените абсолютную
. Оцените абсолютную 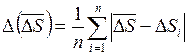 и относительную
и относительную 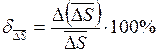 погрешность расчетов.
погрешность расчетов.
4. Окончательный результат запишите в виде
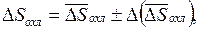
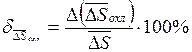 ;
;
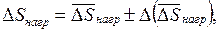
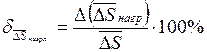 .
.
Контрольные вопросы
1. Сформулируйте первое начало термодинамики.
2. Что называется параметрами системы? Какой процесс называется равновесным?
3. Что называется энтропией системы и каковы ее свойства?
4. Микро и макро состояния. Что называется статистическим весом макросостояния и его связь с энтропией?
5. Сформулируйте второе начало термодинамики.
[1] Числом степеней свободы механической системы называется количество независимых величин, с помощью которых однозначно задается положение системы в пространстве.
[2] Разница в написании бесконечно малого изменения внутренней энергии dU и бесконечно малого количества теплоты dQ, сообщенного системе, или работы dА, совершенной системой, объясняется тем, что энергия – функция состояния, ее изменение при переходе из одного состояния в другое однозначно (не зависит от промежуточных состояний), а количество теплоты и работа – функции процесса, их значения при переходе между заданными состояниями могут быть различны.
[3] Величины, входящие в это выражение, могут быть и положительными, и отрицательными. Если в данном процессе внутренняя энергия уменьшилась, то dU < 0. Если система отдала некоторое количество теплоты, то dQ < 0. Если, наконец, над системой была извне совершена некоторая работа, то dА < 0.
[4] adiabatos (греч.) – непереходимый.
[5] Разница в написании бесконечно малого изменения внутренней энергии dU и бесконечно малого количества теплоты dQ, сообщенного системе, или работы dА, совершенной системой, объясняется тем, что энергия – функция состояния, ее изменение при переходе из одного состояния в другое однозначно (не зависит от промежуточных состояний), а количество теплоты и работа – функции процесса, их значения при переходе между заданными состояниями могут быть различны.