Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Характерные особенности химических соединений
|
|
1. Кристаллическая решетка отличается от решеток компонентов, образующих соединение;
2. В соединении всегда сохраняется простое кратное соотношение компонентов. Это позволяет выразить их состав простой формулой АnВm, где А и В – соответствующие элементы, m и n - простые числа;
3. Свойства соединения резко отличаются от свойств образующих его компонентов;
4. Температура плавления (диссоциации) постоянная;
5. Образование химического соединения сопровождается значительным тепловым эффектом.
Примеры химических соединений: цементит – Fe3C, оксиды металлов WC, TiO2…
Механические смеси образуются, когда из жидкого расплава одновременно выпадают кристаллы составляющих его компонентов. При образовании механической смеси кристаллические решетки фаз не меняются.
Под структурой понимают форму, размеры и характер взаимного расположения фаз в сплаве. Для описания структуры используют понятие структурных составляющих.
Структурная составляющая – часть сплава, имеющая при рассмотрении под микроскопом однообразное строение. Структурные составляющие могут быть однофазными и двухфазными.
| 
| 
|
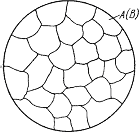
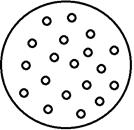
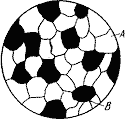
| 1 фаза, 1 структурная составляющая | 2 фазы, 1 структурная составляющая | 2 фазы, 2 структурные составляющие |
Диаграммы и способы их построения
Курс металловедения тесно связан с изучением диаграмм состояния.
Диаграмма состояния сплава представляет собой графическое изображение состояния сплава и показывает превращения, протекающие в сплавах в зависимости от температуры и концентрации элементов (в условиях минимальной свободной энергии).
Без знания диаграмм состояния нельзя научно обоснованно выбирать сплавы с заданными свойствами и выбирать режимы литья, термической обработки и обработки давлением. Диаграммы состояния строятся для определения количества фаз в сплаве и их состава.
Диаграммы состояния, как правило, строят экспериментально (на основании кривых охлаждения). Для их построения обычно используется термический метод, с помощью которого получают кривые затвердевания и охлаждения сплавов.
Готовят ряд сплавов с различным содержанием компонентов А и В, расплавляют и начинают медленно охлаждать, фиксируя их температуру через равные промежутки времени. По этим данным строят кривые охлаждения для всех сплавов.
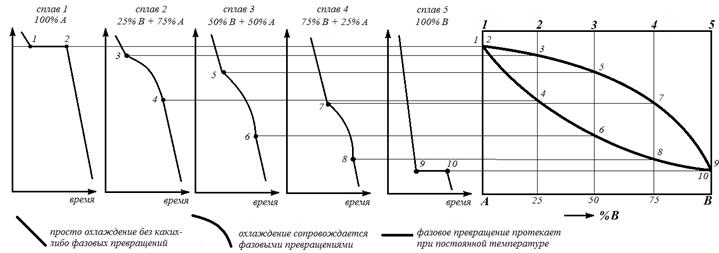
По остановкам и перегибам на этих кривых, обусловленных тепловыми эффектами превращений, определяют температуры превращений.
Фиксируют эти температуры и переносят на поле диаграммы состояния. Затем точки с одинаковым физико-химическим смыслом (начало кристаллизации, конец кристаллизации, образование химического соединения, и т.д.) соединяют между собой.
Кривая, замыкающая критические точки начала кристаллизации a-твердого раствора (линия 1-3-5-7-9) называется линией ликвидус («ликва» – жидкость, лат.).
Семейство критических точек, соответствующих температуре окончания кристаллизационных процессов (линия 2-4-6-8-10), образует линию солидус (solid, «солид» – твердый, лат.).
Выше линии 1-3-5-7-9 сплавы находятся в жидком состоянии. Ниже линии 2-4-6-8-10 сплавы находятся в твердом состоянии.
Точки перегиба (3–8) или остановки (1, 2, 9, 10) на кривых охлаждения называют критическими точками. Они соответствуют температурам, при которых в сплавах начинаются, заканчиваются или полностью протекают какие-либо превращения.
Правило отрезков
А В
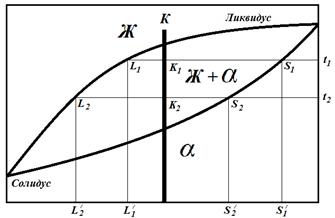
С помощью правила отрезков на диаграмме определяют:
1. Состав фаз сплава заданного состава при определенной температуре.
Пусть имеем сплав К определенной концентрации. Проводим горизонтальную линию, соответствующую данной температуре t 1, до пересечения с линиями ликвидус (l 1) и солидус(s 1). Проекции точек пересечения на ось концентраций (l/ 1 и s/ 1) показывают состав фаз. При охлаждении состав жидкой фазы в соответствии с правилом отрезков меняется по линии ликвидус, а состав твердой фазы – по линии солидус.
2. Относительное количество каждой фазы при определенной температуре.
Отрезки горизонтальной линии между точкой К и точками, определяющими составы фаз, обратно пропорциональны количествам этих фаз:
| температура | количество жидкой фазы | количество твердой фазы |
| t 1 | 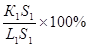
| 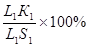
|
| t 2 | 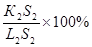
| 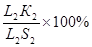
|
Существует большое количество диаграмм различных типов. Свойства сплавов зависят от их положения на диаграмме:
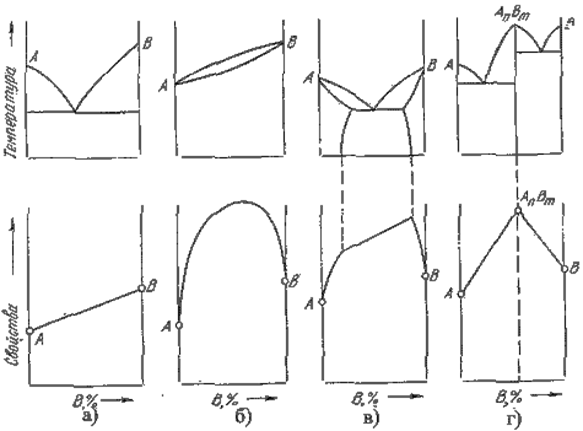
Диаграмма состояния ЖЕЛЕЗО-УГЛЕРОД
Железо и его сплавы – важнейшие конструкционные материалы в технике, и в особенности в машиностроении. Разнообразие фазовых и структурных составляющих в системе железо-углерод способствует получению сталей и чугунов с заданными механическими свойствами.
В виду того, что в машиностроении нельзя использовать сплавы с содержанием углерода свыше 6, 67 % С ввиду их очень высокой хрупкости, то диаграмму состояния обычно изображают для соединения Fe3C – цементита, содержащего 6, 67 % углерода.
Диаграмма состояния железо-цементит