
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Жалпы сипаттама.
|
|
ДӘ РІС 6
Дә ріс тақ ырыбы: VІІІ А тобы элементтері.
Дә ріс жоспары:
1. Жалпы сипаттама.
2. Алынуы. Жай заттар.
3. Химиялық қ асиеттері.
4. Бинарлы қ осылыстары.
5. Гидроксидтер жә не олардың туындылары.
Дә ріс тексті
Жалпы сипаттама.
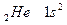
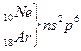
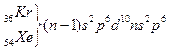
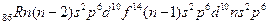
Системаның барлық периодтары VIII А тобының элементтерімен аяқ талады. Бұ л элементтерде (гелийден басқ а, онда 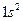 ) толық аяқ талғ ан электрондық қ абат -
) толық аяқ талғ ан электрондық қ абат - 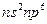 . Электрондық қ ұ рылысы тұ рғ ысынан неонды жә не ауыр асыл газдарды VIII А тобына орналастыру табиғ и нә рсе, ө йткені олардың сыртқ ы қ абатында 8 электрон бар жә не
. Электрондық қ ұ рылысы тұ рғ ысынан неонды жә не ауыр асыл газдарды VIII А тобына орналастыру табиғ и нә рсе, ө йткені олардың сыртқ ы қ абатында 8 электрон бар жә не  - элементтер болып табылады. Бұ л тұ рғ ыдан гелий
- элементтер болып табылады. Бұ л тұ рғ ыдан гелий 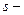 элементтерге жатады (сутек сияқ ты) жә не формальды тү рде ІІ А тобын бастау керек сияқ ты. Бірақ гелийде электрон беріп жіберу (қ озғ ан кү йде, бос орбиталь болса) мү мкіндігі жоқ, сондық тан ол химиялық инертті. Сол себептен оны VIII А тобы ө кілдерімен бірге орналастырады. Сол сияқ ты неонның электрондық конфигурациясының ерекшелігі (
элементтерге жатады (сутек сияқ ты) жә не формальды тү рде ІІ А тобын бастау керек сияқ ты. Бірақ гелийде электрон беріп жіберу (қ озғ ан кү йде, бос орбиталь болса) мү мкіндігі жоқ, сондық тан ол химиялық инертті. Сол себептен оны VIII А тобы ө кілдерімен бірге орналастырады. Сол сияқ ты неонның электрондық конфигурациясының ерекшелігі (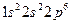 жә не
жә не 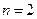 болғ анда бос
болғ анда бос  орбитальдың болмауы) оның химиялық инерттілігін кө рсетеді. Одан басқ а
орбитальдың болмауы) оның химиялық инерттілігін кө рсетеді. Одан басқ а 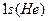 жә не
жә не 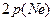 орбитальдардың кайносимметриялы болуы – бұ л элементтердің инертті болуының тағ ы бір себебі. VIII А тобының басқ а ө кілдерінде, аргоннан бастап, сыртқ ы электрон қ абатына сә йкес келетін бас квант санының мә ніндей бос
орбитальдардың кайносимметриялы болуы – бұ л элементтердің инертті болуының тағ ы бір себебі. VIII А тобының басқ а ө кілдерінде, аргоннан бастап, сыртқ ы электрон қ абатына сә йкес келетін бас квант санының мә ніндей бос  орбитальдары
орбитальдары  бар. Сондық тан олар электрондардың ажырауы (распаривание) есебінен валентті-химиялық қ осылыстар тү зуге қ абілетті. Олардың электрондық қ ұ рылысындағ ы осы ө згешелікті ескере отырып, гелий мен неонды инертті газдар, ал аргонды жә не VIII А тобының ауырырақ газдарын асыл газдар деп атағ ан жө н.
бар. Сондық тан олар электрондардың ажырауы (распаривание) есебінен валентті-химиялық қ осылыстар тү зуге қ абілетті. Олардың электрондық қ ұ рылысындағ ы осы ө згешелікті ескере отырып, гелий мен неонды инертті газдар, ал аргонды жә не VIII А тобының ауырырақ газдарын асыл газдар деп атағ ан жө н.
Инертті жә не асыл газдардың атомдары ө з периодтарында эктремальді қ асиеттерімен сипатталады: ең аз атомдық радиустармен жә не ең кө п иондану потенциалымен, оғ ан қ оса VIII А тобында бұ л шамалар біркелкі ө згермейді
Кайносимметриялы 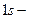 орбиталь
орбиталь 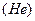 жә не
жә не 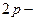 орбиталь
орбиталь 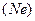 болгандық тан, олардың атомдық радиустары айтарлық тай аз, ал иондану птенциалдары асыл газдарғ а қ арағ анда анағ ұ рлым жоғ ары. Аргондағ ы бос
болгандық тан, олардың атомдық радиустары айтарлық тай аз, ал иондану птенциалдары асыл газдарғ а қ арағ анда анағ ұ рлым жоғ ары. Аргондағ ы бос 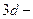 орбиталі де кайносимметриялы болғ андық тан, ол да басқ а асыл газдардан ерекшеленеді. Бұ л жағ дай, басқ а асыл газдарда белгілі болғ андай, аргонда валентті қ осылыстардың болмауының бір себебі болады.
орбиталі де кайносимметриялы болғ андық тан, ол да басқ а асыл газдардан ерекшеленеді. Бұ л жағ дай, басқ а асыл газдарда белгілі болғ андай, аргонда валентті қ осылыстардың болмауының бір себебі болады.
2. Алынуы. Жай заттар.
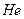 ,
, 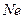 ,
, 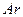 ,
, 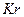 ,
, 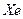 - сұ йық ауаны ректификациялаудағ ы қ осымша ө німдер ретінде алынады.
- сұ йық ауаны ректификациялаудағ ы қ осымша ө німдер ретінде алынады.
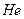 - табиғ и газдарды терең салқ ындату ә дісімен алынады.
- табиғ и газдарды терең салқ ындату ә дісімен алынады. 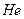 - ден басқ а газдар-қ оспа, олар сұ йытылады;
- ден басқ а газдар-қ оспа, олар сұ йытылады; 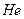 - ең тө мен қ айнайтын зат ретінде газ кү йінде қ алады, тек жоғ ары қ ысымда ғ ана сұ йылады.
- ең тө мен қ айнайтын зат ретінде газ кү йінде қ алады, тек жоғ ары қ ысымда ғ ана сұ йылады.
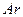 - аммиак
- аммиак  синтездеудегі қ осымша ө нім.
синтездеудегі қ осымша ө нім.
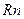 - радийдің радиоактивті ыдырауынан алады:
- радийдің радиоактивті ыдырауынан алады:
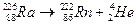
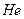 ,
, 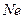 жә не
жә не 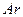 - типтік элементтер,
- типтік элементтер, 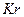 ,
, 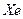 ,
, 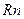 - толық электрондық аналогтар.
- толық электрондық аналогтар. 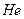 жә не
жә не 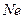 инертті газдар, олар химиялық қ осылыстар тү збейді, ал қ алғ андары –
инертті газдар, олар химиялық қ осылыстар тү збейді, ал қ алғ андары – 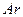 ,
, 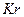 ,
, 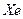 ,
, 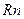 бағ алы газдарғ а жатады, ө йткені олар белгілібір активтілік кө рсетеді.
бағ алы газдарғ а жатады, ө йткені олар белгілібір активтілік кө рсетеді.
Қ атты тү рінде 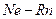 қ ырлы-центрленген кубтық тор (атомды-молекулалық тор) болады.
қ ырлы-центрленген кубтық тор (атомды-молекулалық тор) болады.
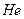 жә не
жә не 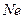 атомдық радиустары қ алғ ан бағ алы газдарғ а қ арағ анда анағ ұ рлым аз, нә тижесінде
атомдық радиустары қ алғ ан бағ алы газдарғ а қ арағ анда анағ ұ рлым аз, нә тижесінде 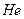 жә не
жә не 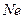 иондану энергиясы басқ а газдарғ а қ арағ анда анағ ұ рлым жоғ ары, бұ л олардың инерттілігінің себебі болады. Топшада жоғ арыдан тө мен орбиталь радиустың ұ лғ аюымен иондану энергиясы кемиді, бұ л бағ ытта атомдардың поляризациялануы, бір-бірімен дисперсиялық, ван-дер-ваальстік ә рекеттесулері артады, олар қ айнау жә не балқ у энтальпияларының, қ айнау жә не балқ у температураларының, тығ ыздығ ының жә не суда еруінің жоғ арлауына ә келеді.
иондану энергиясы басқ а газдарғ а қ арағ анда анағ ұ рлым жоғ ары, бұ л олардың инерттілігінің себебі болады. Топшада жоғ арыдан тө мен орбиталь радиустың ұ лғ аюымен иондану энергиясы кемиді, бұ л бағ ытта атомдардың поляризациялануы, бір-бірімен дисперсиялық, ван-дер-ваальстік ә рекеттесулері артады, олар қ айнау жә не балқ у энтальпияларының, қ айнау жә не балқ у температураларының, тығ ыздығ ының жә не суда еруінің жоғ арлауына ә келеді.
Мә селен, 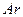 ,
, 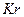 ,
, 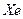 - кристаллогидраттар
- кристаллогидраттар 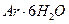 ,
, 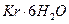 ,
, 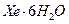 тү зеді.
тү зеді. 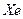 ү шін осы тә різдес басқ а қ осылыстары
ү шін осы тә різдес басқ а қ осылыстары 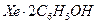 ,
, 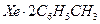 белгілі. Бұ лар комплексті қ осылыстар емес, олар ену молекулалық қ осылыстары.
белгілі. Бұ лар комплексті қ осылыстар емес, олар ену молекулалық қ осылыстары.