
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Изменению каких функций состояния равны тепловые эффекты изобарного и изохорного процессов.
|
|
Первый закон термодинамики устанавливает связь между количеством теплоты, полученным или отданным в процессе химической реакции, работой, совершенной системой, и изменением внутренней энергии.
В соответствии с первым законом термодинамики  ,
,  ⇒
⇒ 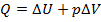 (1)
(1)
1) При p = const (изобарный процесс) уравнение (1) можно записать как 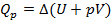 , где
, где 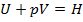 (энтальпия)
(энтальпия)
Энтальпия -это функция состояния термодинамической системы, изменение которой при постоянном давлении равно количеству теплоты, подведенной к системе, поэтому энтальпия называется часто тепловой функцией или теплосодержанием.
Отсюда следует, что 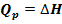
2) При V = const (изохорный процесс)  ⇒
⇒  , где U - внутренняя энергия.
, где U - внутренняя энергия.
Внутренняя энергия - это энергия физической системы, зависящая от её внутреннего состояния. Она включает энергию хаотического (теплового) движения всех микрочастиц системы (молекул, атомов, ионов и т. д.) и энергию взаимодействия этих частиц.