
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Основные проявления интоксикации. Действуя в дозах выше среднелетальных, вещество поражает все жизненно важные органы (печень, почки, лёгкие)
|
|
Действуя в дозах выше среднелетальных, вещество поражает все жизненно важные органы (печень, почки, лёгкие). Развиваются: ожог слизистой желудочно-кишечного тракта, диарея, повреждение паренхиматозных органов и острый токсический альвеолит. Характерна отсроченная гибель отравленных через несколько дней или недель от нарастающего фиброза лёгких.
Поражение лёгких при интоксикации паракватом протекает в две фазы. В первую – деструктивную (1-3 сутки) – наблюдается гибель и десквамация альвеолоцитов 1-го и 2-го типов, что становится причиной острого альвеолита, токсического отёка лёгких. Во второй фазе – пролиферативной – происходит замещение альвеолоцитов кубовидными клетками, постепенное разрастание фиброзной ткани.
|
Предотвратить накопление параквата в лёгких после его приёма на практике не удается. Субстраты-конкуренты яда (цистамин, путресцин и т.д.) могут оказать эффект лишь в ранние сроки от начала интоксикации (первые 8-12 часов).
При отравлениях паракватом абсолютно противопоказана оксигенотерапия. Данное мероприятие достоверно ускоряет гибель отравленных. Только в случаях угрожающей жизни гипоксемии (РО2 в артериальной крови менее 40 мм Hg) возможна ингаляция кислорода.
Треххлористый фосфор (РС1з) – бесцветная жидкость с температурой кипения +74, 8°С. Удельный вес 1, 57. Хорошо растворим в органических растворителях. Энергично реагирует с водой. Сильно раздражает слизистую оболочку верхних дыхательных путей. При попадании на кожу вызывает ожоги. Для нейтрализации необходимо большое количество воды. LD = 550 мг/кг.
Пятифтористая сера – бесцветная жидкость. Температура кипения +29°С. Летучее соединение, пары токсичнее фосгена. ПДК 0.025 мг/м3.
Изоцианаты – это жидкости и кристаллические вещества, которые, попадая в организм ингаляционным путём способны вызывать поражение органов дыхания с развитием токсического отёка лёгких. Наибольшую опасность представляет метилизоцианат. Метилизоцианат – бесцветная жидкость с едким запахом. Температура кипения около +45°С. По токсичности близок к синильной кислоте. Как все изоцианаты обладает выраженным раздражающим действием на конъюнктиву глаз и дыхательные пути. Уже при однократной экспозиции может развиться состояние повышенной чувствительности к токсиканту, проявляющееся синдромом реактивной дисфункции дыхательных путей (СРДП) – состояние, напоминающее приступ бронхиальной астмы.
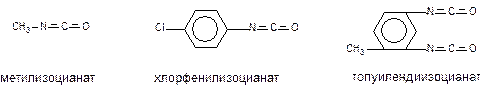
Аммиак (NНз) – бесцветный газ с резким запахом и щелочным вкусом. Легче воздуха. Легко растворяется в воде. При охлаждении и под давлением сгущается в прозрачную бесцветную жидкость, кипящую при температуре +33°С. Обладает как местным так и резорбтивным действием. В концентрации 0, 3-0, 5 г/м3 вызывает раздражение; 7-14 г/м3 – эритематозный, 21 г/м3 – буллёзный дерматит. Возможны химические ожоги глаз. В концентрации более 1, 5 г/м3 и часовой экспозиции вызывает развитие токсического отёка лёгких.
Удушающим действием обладают такие вещества, которые при ингаляционном поступлении в организм вызывают токсический отёк лёгких (ТОЛ) с развитием кислородного голодания. К данной группе отравляющих веществ (ОВ) относятся фосген, дифосген, трифосген, обладающие высокой летучестью и при вдыхании которых специфически поражается лёгочная ткань и возникает отёк лёгких. Помимо этих ОВ удушающим действием обладают хлор, хлорпикрин, аммиак, гидразин, окислы азота и др.
Согласно современной химической классификации фосген и дифосген относятся к производным угольной кислоты.
Фосген. Фосген впервые получен в 1811 году английским химиком Дж. Дэви, при реакции хлора с окисью углерода на солнечном свету. Отсюда и произошло название (фосген от греч.-" светорождённый"). Фосген впервые применен немцами как ОВ 19 декабря 1915 года (германские войска осуществили газобаллонные пуски против английских войск). Всего за первую мировую войну было произведено 40 тыс. т. фосгена. В 1935 году применялся итальянской армией в Эфиопии, японцами во время войны с Китаем (1937-1945г.г.).
Фосген и его производные являются важным исходным продуктом синтеза пластмасс, синтетических волокон, красителей, пестицидов. Поэтому производство этого вещества во всех странах с развитой химической промышленностью неуклонно возрастает.
Фосген является одним из токсичных продуктов термической деструкции хлорорганических соединений (фреоны, поливинилхлоридный пластик, тефлон, четырёххлористый углерод), что также необходимо учитывать при организации оказания помощи в очагах аварий и катастроф.
Фосген (дихлорангидрид угольной кислоты) – бесцветный газ с запахом прелого сена или гнилых яблок, плотность которого в 3, 48 раза выше плотности воздуха. Температура кипения +8, 2оС, что обусловливает высокую летучесть. Максимальная концентрация при температуре –20оС. составляет 1400 мг/л, а при температуре +20оС – 6370 мг/л. Застывает в белую кристаллическую массу при –118оС. Фосген является липидотропным веществом, ограниченно растворяется в воде (0, 9%), хорошо в органических растворителях, в жирах, липидах и других ОВ. Фосген, растворённый в воде, быстро гидролизуется с образованием угольной и соляной кислот (при температуре 0оС в 100 г воды за 20 сек. разлагается 1 г ОВ). В щелочной среде и при нагревании гидролиз ускоряется. При взаимодействии с аммиаком образуются нетоксичные мочевина и хлористый аммоний, что используется для дегазации. При реакции с уротропином образуются продукты присоединения, что лежало в основе защитного действия " влажного противогаза".
Токсикокинетика. Фосген действует только ингаляционно, оказывает специфическое «удушающее» действие: отёк лёгких. В момент контакта раздражающим действием практически не обладает (немой контакт).
Во внутренние среды фосген не проникает, разрушаясь в крови малого круга.
Фосген обладает кумулятивным свойством. Запах фосгена ощущается при концентрации 0, 004 мг/л. Вдыхание данной концентрации в течение 1 часа влияет на вкусовые ощущения (отвращение к табачному дыму и запаху). При пребывании в атмосфере с концентрацией свыше 5 мг/л, смерть может наступить в течение 1 минуты. Условно-смертельная концентрация 3, 2 мг/л мин. Концентрация 0, 3 мг/л вызывает смерть при экспозиции 15 мин.
Дифосген. Дифосген впервые получен в 1847 г. О.Кауром (Франция). 16 мая 1916 года немцы обстреляли позиции французских войск артиллерийскими снарядами и минами, содержащими дифосген. А всего за годы первой мировой войны было произведено около 20 тыс.т. дифосгена.
Дифосген (трихлорметиловый эфир хлоругольной кислоты) – бесцветная легкоподвижная жидкость с запахом как у фосгена. Температура кипения +128оС, но летучесть его в 2, 5 раза превосходит летучесть воды, замерзает при –97оС. Максимальная концентрация при температуре +20оС – 120 мг/л. Химические свойства аналогичны фосгену.
Порог раздражающего действия дифосгена на глаза 0, 005 мг/л, непереносимая концентрация 0, 075 мг/л мин., смертельная 0, 5-0, 7 мг/л при 15 минутной и 1 мг/л – при минутной экспозиции. Условно-смертельная концентрация 3, 4 мг/л мин.
Из 100.000 человек, погибших в 1 мировую войну от химического оружия, 80.000 погибли от фосгена и дифосгена.
Фосген и дифосген способствуют возникновению очагов поражения нестойкими ОВ замедленного действия. Санитарные потери в таком очаге формируются в течение 1-6 часов.
Клинические формы поражений, степень тяжести их проявлений зависят от токсических концентраций фосгена и дифосгена, а также от ингаляционной токсодозы. Так, в интервале ингаляционных доз 0, 05-0, 5 мг мин/л возникают лёгкие формы поражения, которые проявляются в форме токсических катаров ВДП и кератоконъюнктивитов; при токсических концентрациях от 0, 5 до 3 мг мин/л возникают поражения средней тяжести, которые диагностируются как первичная токсическая бронхопневмония. При воздействии более высоких концентраций (3–10 мг мин/л) возникает тяжёлая форма поражения – токсический отёк лёгких. Концентрации на порядок выше (10-100 мг мин/л) вызывают тяжелейший ожог лёгочной ткани. Сверхвысокие концентрации могут вызвать смерть от рефлекторного спазма голосовой щели.
Ожог лёгочной ткани и рефлекторное удушье следует рассматривать как крайне тяжёлую степень поражения. Однако прогностически указанные два состояния отличаются друг от друга. При ожоге лёгочная ткань становится ломкой и сухой. Она полностью утрачивает свои функциональные свойства. При рефлекторном спазме лёгкие могут сохранить свою функцию, если пострадавшему своевременно надеть противогаз, произвести искусственное дыхание и вынести из заражённой атмосферы.
2. ПАТОГЕНЕЗ ИНТОКСИКАЦИИ ОВ УДУШАЮЩЕГО ДЕЙСТВИЯ.
Патогенез поражения ОВ удушающего действия является сложным. Он не может быть уложен ни в одну схему резорбтивного действия яда, ни в представление о превалирующем местном действии ОВ.
Первое опровергается нестойкостью молекулы ОВ – доказано, что яд в свободном состоянии циркулирует в организме не больше, чем в течение одного-двух полных кругооборотов крови. При этом также исключается действие соляной кислоты, как основного продукта гидролиза (ди-)фосгена, ибо последней, при смертельном отравлении образуется примерно в 2400 раз меньше той дозы, которая при введении в организм могла бы привести к летальному исходу.
Объяснить же патогенез поражения за счёт местного действия яда не представляется возможным потому, что интоксикация ОВ не ограничивается изменениями со стороны органов дыхания.
Токсикодинамика (механизм токсического действия): вызывает отёк лёгких «медленного» типа. Фосген не задерживается в дыхательных путях вследствие низкой гидрофильности.
При рассмотрении патогенеза поражения ОВ удушающего действия следует учитывать следующие моменты:
1. Возникновение токсического отёка лёгких.
2. Развивающееся кислородное голодание.
3. Расстройство сердечно-сосудистой системы.
4. Нарушение тканевого метаболизма.
К сожалению, законченной теории патогенеза токсического отёка лёгких не существует до сих пор. В патогенезе поражения имеют значение как местные факторы, связанные с непосредственным действием ОВ на ткань лёгких, так и общие, являющиеся следствием глубоких сдвигов, наступающих в организме под действием ОВ.
Отёк лёгких – патологическое состояние, при котором транссудация сосудистой жидкости не уравновешивается её резорбцией, и сосудистая жидкость изливается в альвеолы. Токсическим он называется потому, что возникает в результате действия токсического вещества. В основе токсического отёка лёгких лежит повышение проницаемости капиллярной и альвеолярной стенок, что приводит к пропотеванию не только жидкой части крови, но и протеинов.
Проницаемость капиллярной и альвеолярной стенок нарушается не одновременно. Вначале становятся проницаемыми капиллярные мембраны, и сосудистая жидкость пропотевает в интерстиций, где временно накапливается. Такую фазу развития отёка называют интерстициальной, она характеризуется постепенным развитием (отсутствие клинических симптомов отёка лёгких). Во время этой фазы происходит компенсаторное ускорение лимфотока примерно в 10 раз. Но эта приспособительная реакция оказывается недостаточной, и внесосудистая жидкость, переполнив интерстиций, прорывается в полость альвеол через их деструктивно измененные стенки. Это приводит к развитию альвеолярной фазы, характеризующейся внезапностью развития и клиническими признаками отёка лёгких. Причины нарушения проницаемости капиллярно-альвеолярной мембраны многочисленны, но наибольшее значение имеют увеличение внутрисосудистого давления в малом круге кровообращения и повреждающее мембраны действие.
Лёгочная гипертензия возникает благодаря увеличению содержания в крови вазоактивных веществ, гипоксии и угнетению скорости лимфотока.
Вазоактивные вещества способны оказывать влияние непосредственно на гладкие мышцы сосудов и бронхов и повышать тонус сосудов малого круга, вызывая лёгочную гипертензию.
Гипоксия и регуляция уровней вазоактивных веществ (норадреналина, ацетилхолина, гистамина, кининов и т.д.) связаны между собой. Обнаружено, что при гипоксии нарушается инактивация в лёгких конкретных вазоактивных веществ – норадреналина, серотонина и брадикинина, что также вызывает лёгочную гипертензию.
Местное повреждающее мембраны действие является обязательным условием развития токсического отёка лёгких. Об этом говорит невозможность развития токсического отёка лёгких при воздействии фосгеном неигаляционным путём. Структурная целостность альвеолярно-капиллярного комплекса поддерживается благодаря определённым биохимическим процессам, происходящим в нём. Наиболее интенсивно в лёгочной ткани протекают окислительно-восстановительные процессы, что подтверждается присутствием сульфгидрильных и дисульфидных групп, а также аскорбиновой кислоты. Под действием токсических веществ происходит блокада SH- групп (перевод их в дисульфидные) структурных белков альвеолярно-капиллярной мембраны. Их инактивация приводит к нарушению связи белков с липидами, что вызывает разрыхление лёгочной мембраны и облегчает ток жидкости через неё.
При воздействии ОВ в тканях лёгкого увеличивается содержание свободного гистамина. Гистамин активирует гиалуронидазу, являющуюся фактором тканевой проницаемости.
К местным нарушениям следует отнести повреждение поверхностно активного вещества (лёгочного сурфактанта). Лёгочный сурфактант обеспечивает стабилизацию лёгочной мембраны, предупреждая полное спадение лёгких при выдохе. При токсическом отёке лёгких содержание сурфактанта в альвеолах снижается. Это приводит к снижению поверхностного натяжения отёчного экссудата и созданию дополнительного препятствия внешнему дыханию.
Местные биохимические изменения в лёгочной ткани, возникающие под действием фосгена: пары фосгена образуют комплекс с сурфактантом, который раздражает рецепторы тучных клеток Эрлиха в лёгочной ткани. Клетки начинают испытывать энергетический голод. Они перестают удерживать в себе запасы гистамина, серотонина и других активных веществ. Эти вещества активируют гиалуронидазу лёгочной ткани, являющуюся фактором тканевой проницаемости, и сосудистая мембрана из полупроницаемой становится проницаемой. В лёгочную ткань устремляются из крови вещества, богатые энергией. Энергетический голод устраняется ценой повреждения сосудистой мембраны и развития токсического отёка лёгких.
Большую роль в развитии токсического отёка лёгких играет нервная система. Впервые в опытах А.В. Тонких и В.Д. Белогорского (1946г) выявлена пусковая роль нервно–рефлекторных механизмов в патогенезе токсического отёка лёгких. У кошек атравматично перерезались шейные симпатические узлы. Последующая затравка животных в камере с дифосгеном показала, что у таких животных по сравнению с контрольными (неоперированными) не возникает токсический отёк лёгких. Следовательно, симпатические нервы несут к лёгким (эфферентно) чрезвычайную импульсацию, которая вызывает развитие патологического процесса. Афферентным звеном рефлекторной дуги являются рецепторы n.vagus в нижнем отделе дыхательных путей, которые подвергаются прямому воздействию паров фосгена и дифосгена. Достигая центра n.vagus, возбуждение иррадиирует на гипоталамус, на высшие центры симпатической регуляции. Выброс катехоламинов в лёгочные сосуды увеличивает гидростатическое давление крови, нарушает трофические процессы в лёгочной ткани, что подтверждается экспериментально. Внутривенное введение животным избыточного количества адреналина вызывает у них развитие отёка лёгких. Нейрогенным путем может быть угнетён и лимфоток, что ведет к гипертензии.
Нарушение проницаемости альвеолярно-капиллярной мембраны вызывает воздействие токсических веществ на рецепторы дыхательных путей и паренхимы лёгких, на хеморецепторы малого круга кровообращения (в этих образованиях имеются структуры содержащие SH- группы).
Кислородное голодание – основная причина, приводящая к расстройству многих функций организма при отравлении ОВ удушающего действия. Гипоксия возникает уже в скрытом периоде. Повышается возбудимость блуждающего нерва, а это приводит к тому, что меньшее по сравнению с обычным растяжение альвеол при вдохе служит сигналом к прекращению вдоха и началу выдоха. Снижение альвеолярной вентиляции, уменьшает поступление кислорода в кровь и вызывает гипоксию, обязанную своим происхождением рефлексу с блуждающего нерва и называется, поэтому, рефлекторной.
Гипоксия с развитием отёка нарастает, неоднократно меняется по глубине и приводит к дальнейшему нарушению многих функций. Вслед за гипоксемией рефлекторного происхождения выделяют синюю гипоксию, характеризующуюся более глубокими расстройствами дыхания, но выраженных расстройств гемодинамики при этом не наблюдается. Содержание кислорода в крови снижается, а углекислого газа увеличивается (гиперкапния), что приводит к стимуляции дыхательного центра и нарастанию одышки.
Гипоксемия вызывает нарушение метаболических процессов и появление в крови недоокисленных продуктов обмена (молочная, ацетоуксусная и b-оксимасляная кислоты, ацетон), что способствует ещё большему нарушению дыхания и изменению кислотно-щелочного равновесия. Иногда ацидоз бывает и более выраженным. Все это приводит к увеличению проницаемости мембран и нарастанию отёка.
Гипоксия и сгущение крови вызывает замедление тока крови и её перераспределение. Расстройство гемодинамики приводит к появлению циркуляторной гипоксии. При этом выявляются клинические признаки коллапса. Такая стадия гипоксии носит название серой гипоксии. Снижается содержание кислорода в крови и углекислого газа (гипокапния). Возникновение гипокапнии можно объяснить нарушением метаболических процессов в условиях гипоксии, снижением выработки углекислого газа и способностью его легко диффундировать через отёчную жидкость.
Сердечно-сосудистая система претерпевает наиболее тяжёлые изменения. Это происходит вследствие гипоксии миокарда, увеличения вязкости крови и отёка лёгких. Уже в скрытом периоде, как ответная реакция на раздражение блуждающего нерва, отмечается брадикардия, которая сопровождается учащённым дыханием (характерно для дифосгена), нарушением коронарного кровообращения, снижением артериального давления. По нарастанию гипоксемии и гиперкапнии как реакция компенсации, развивается тахикардия и повышается тонус периферических сосудистых образований. Но с нарастанием гипоксии и ацидоза паралитически расширяются капилляры, и в них депонируется кровь. Одновременно увеличивается проницаемость сосудистой стенки, что благоприятствует развитию отёка ткани.