
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Литературный обзор
|
|
Курсовая работа
Тема: “ Синтез 1- (фенилазо) – нафтол – 2 (судан 1)”
Выполнила: Студентка Григорьева А.С.
Гр 15451
Руководитель: Таратайко А.И.
Новосибирск
Содержание
1 Введение………………………………………………………….3-4
2 Литературный обзор…………………………………………….4-8
3 Реакция азосочетания…………………………………………..9-10
4 Экспирементальна часть ………………………………………..10-13
5 Выводы……………………………………………………………14
6 Список литературы………………………………………………15
Введение
Судан — группа нейтральных жирорастворимых красителей
Существует несколько типов с разными заместителями: Судан I, Судан II, Судан III, Судан IV, Sudan Para Red (Пара Ред), Судан Чёрный и другие. В сферах экономики используются при производстве дизельного топлива, в легкой промышленности для окрашивания тканей, а также при проведении биохимических исследований для окрашивания препаратов, и относятся к непищевым красителям. Часто используются при фальсификации специй и пряностей, а также продуктов их переработки, БАД к пище, изготовленных с использованием специй и пряностей, и других пищевых продуктов, в состав которых входят специи и пряности, с целью придания им более интенсивной окраски. В химии и медицине используется для качественного определения жиров и покраске гистологических проб.
Судан I — краситель жёлтого цвета — C16H12N2O

Цель работы: синтезировать данное вещество в соответствии с приведенными инструкциями, узнать физические и химические свойства данного соединения, исследовать механизмы реакций азосочетания.
Литературный обзор
Реакция азосочетания - это наиболее важная в практическом отношении реакция ароматических диазосоединений. Соли диазония реагируют с фенолами и ароматическими аминами с образованием ярко окрашенных азосоединений, в которых два ароматических кольца связаны азогруппой - N = N -.
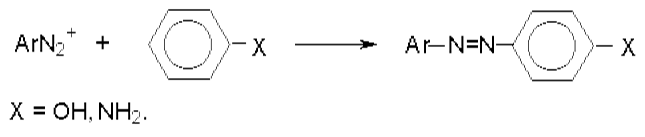
Диазосоединения получили название диазосоставляющих реакции азосочетания, а амины или фенолы — азосоставляющей.
В этой реакции следует различать диазо- (ArN2+) и азо- (ArX)
составляющие. Азосочетание относится к типичным реакциям электрофильного ароматического замещения, скорость которой зависит как от электрофильных свойств катиона диазония, так и от электронодонорных свойств азосоставляющей. Диазосоединеия участвует в р-ции в форме катиона диа-зония. Азосоставляющая имеет нуклеоф. центр, возникающий при ее ионизации или поляризации. Степень поляризации зависит от электронодонорных св-в заместителей. В кач-ве азосоставляюшей обычно используют фенолы, амины, эфиры и анилиды ацетоуксусной и др. кетокислот, производные 5-пиразолона и др.
Катион арендиазония относится к числу слабых электрофильных агентов, так как его положительный заряд делокализован за счет сопряжения с ароматическим кольцом. Как слабый электрофильный агент катион диазония взаимодействует только с такими производными бензола и нафталина, которые содержат сильные электронодонорные заместители.
Реакционная способность азосоставляющей уменьшается в ряду: X = O- > NR2 > NHR > NH2 > OH~OR > > Alk. В реакцию азосочетания вступают фенолы в форме фенолят - ионов, обладающих +М и +I эффектом аниона О-, и амины благодаря сильному +М эффекту аминогруппы. Только в отдельных, исключительных случаях соли арендиазония взаимодействуют с эфирами одно- или многоатомных фенолов.
Активной формой фенола в качестве азосоставляющей является фенолят - анион и сочетание с фенолами проводят в слабоосновной среде. Однако рН раствора в этом случае поддерживают в интервале 8-10, избегая более высокой основности раствора. Это объясняется тем, что единственно активной формой диазосоединений в реакции азосочетания является только катион диазония.
Анти- и син- диазотат - анионы, также как и другие стойкие формы диазосоединений, такие как ковалентные диазосульфонаты, диазоцианиды и триазены, неактивны в этой реакции. Как уже было отмечено ранее, при значениях рН > 12 резко уменьшается концентрация активной формы ArN2+ и растет концентрация нереакционноспособного Ar - N = N - O-. Именно по этой причине сочетание с фенолами проводится в растворах со значением рН от 8 до примерно 10.
С другой стороны, сочетание с ароматическими аминами проводится в слабокислой среде с рН 3 - 5, где катион диазония реагирует со свободным непротонированным амином. Катион арендиазония в слабокислой или нейтральной среде первоначально атакует атом азота первичных или вторичных аминов, как место наиболее высокой электронной плотности.
При этом в результате быстрого кинетически контролируемого процесса образуются диазоаминосоединения (триазены). Эта реакция, однако, обратима и протонированная форма триазена в кислой среде легко разлагается на исходные реагенты.
Более медленная реакция катиона арендиазония по пара-положению ароматического амина приводит к азосоединению, как конечному продукту термодинамически контролируемого процесса. Поскольку образующийся в качестве промежуточного соединения сигма-комплекс обладает большей кислотностью, чем катион диазония, он легко депротонируется даже в слабокислом растворе под действием любого основания, присутствующего в реакционной смеси.

Азосочетание отличается от других реакций электрофильного ароматического замещения чрезвычайно высокой селективностью. Азосочетание с фенолят-ионами и аминами осуществляется в пара-положение к гидроксильной группе или аминогруппе. Доля продукта замещения в орто-положение, как правило, не превышает 1-2 %. И только в том случае, если пара-положение занято, сочетание идет в орто-положение.
Среди фенолов орто- и пара-нитрофенолы не вступают в реакцию азосочетания, но салициловая кислота, содержащая более слабый акцепторный заместитель, уже реагирует с катионом диазония. Резорцин очень легко сочетается в положение 4, а со вторым катионом диазония в положение 2, гидрохинон и пирокатехин окисляются солями диазония до хинонов.
Среди ароматических аминов мета-нитроанилин, мета-хлоранилин, мета-аминобензолсульфокислота и ряд других аминов с электроноакцепторными заместителями не вступают в реакцию азосочетания. Орто- и пара-фенилендиамины, так же как орто- и пара-аминофенолы, окисляются солями диазония до хинонов.
Если в азосоставляющей имеются одновременно амино- и гидроксигруппа, то в зависимости от рН среды сочетание проводится при активирующем влиянии либо амино-, либо гидроксигруппы. Практически в таких случаях первоначально проводят сочетание в слабокислой среде, где ориентацию оказывает аминогруппа.
Так, например, при сочетании солей диазония с 4- амино-5-гидрокси-2, 7-нафталиндисульфокислотой (Аш - кислотой) в кислой среде сочетание идет в положение 3, а в основной - в положение 6.
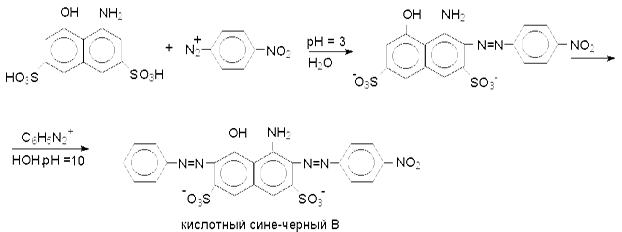
В результате комбинации солей диазония из различных ароматических аминов с различными азосоставляющими и подбора условий могут быть получены самые разнообразные азокрасители. Многие азокрасители в зависимости от рН среды изменяют строение, а следовательно и окраску. Такие азокрасители находят применение в качестве индикаторов (метилоранж, метаниловый желтый, метиловый красный, конго красный и др.).
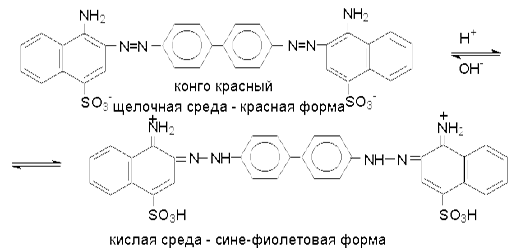
Азокрасители используются для окрашивания тканей. Ниже приведены некоторые примеры азокрасителей, используемых при крашении естественных волокон - шерсти и хлопка.

Механизм реакции (общий)
Установлено, что реакция азосочетания протекает по механизму электрофильного замещения, в котором атакующим агентом выступает ион диазония (Аг—N=N), а субстратом — ароматические системы, содержащие в п- или о-положении заместители NH2, NHAlk, NHAr, N(Alk)2, NHSO3H, NHNO2, ОН и в некоторых случаях OAlk:

Вследствие небольшой активности ионов диазония реакция протекает направленно с образованием п- или о-изомеров. Электроноакцепторные заместители в диазониевом ионе повышают его реакционную способность, а электронодонорные группы понижают ее.