
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Cинтетические поверхностно-активные вещества
|
|
Обычные мыла изготавливаются нагреванием с каустической содой. Основной активный компонент такого мыла – стеарат натрия: (СH3–(CH2)16–СO–O)– Na+, легко разлагается в водной среде и представляет опасность для окружающей среды не большую, чем другие легкоокисляемые органические вещества, входящие в состав бытовых сточных вод.
Но с 1950-х г. начали применяться более эффективные синтетические моющие средства (СМС). В таких моющих средствах содержатся активные соединения – сурфактанты (детергенты), обладающие более сильными поверхностно-активными свойствами, чем «натуральное» мыло. Кроме того, СМС или синтетические поверхностно-активные вещества (СПАВ) лучше стирают в жесткой воде, в которой применение обычного мыла, как известно, затруднено.
Обычно такое поверхностно-активное вещество растворено в триполифосфате натрия или в четырехзамещенном трифосфате натрия. Если мыло в воде подвергается полному гидролизу и разлагается до легко усвояемых водной микрофлорой соединений, то СМС обладают многими нежелательными свойствами (вспенивание воды, возникновение кислородного дефицита, токсичность для гидробионтов). Кроме того, входящие в состав СМС фосфатные наполнители вызывают эвтрофирование водоемов. В связи с последней опасностью в настоящее время фосфорсодержащие детергенты в развитых странах заменены сульфатсодержащими веществами, например такими как алкилбензолсульфонат натрия (Эткинс, 1991):
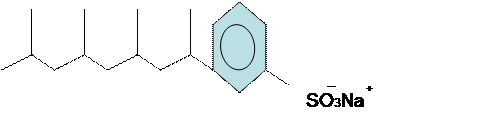
лорилсульфат натрия:
(СH3–(CH2)11–O–SO2–O)– Na+.
Кроме того, они содержат добавочные ингредиенты: ароматизирующие вещества, отбеливающие реагенты (персульфаты, пербораты), токсичные для водных организмов.
В настоящее время, СПАВ – одни из самых распространенных химических загрязнителей водоемов. Они поступают в водные объекты в результате их широкомасштабного применения с бытовыми, промышленными и сельскохозяйственными стоками. В сельском хозяйстве поверхностно-активные вещества используются для эмульгирования пестицидов. В подземные воды поверхностно-активные вещества попадают в результате применения почвенных методов очистки сточных вод, при пополнении запасов подземных вод из открытых водоемов и при загрязнении почвы этими веществами.
Кроме описанных выше ионных детергентов, производятся и неионные детергенты. Примером их может служить полиоксиэтилен (Эткинс, 1991):
СH3–(CH2)11–O–CH2–CH2–OH
Их используют, как правило, для эмульгации нефтяных загрязнений больших масштабов.
Поверхностно-активные вещества – «экологически жесткие» вещества.
На их окисление расходуется много растворенного кислорода, который, таким образом, отвлекается от процессов биологического окисления. Кроме этого косвенного вреда, детергенты оказывают и прямое токсическое действие на водных животных. Они нарушают функции биологических мембран. Это вызывает жаберные кровотечения и удушье у рыб и беспозвоночных животных. Для теплокровных они усиливают токсическое и канцерогенное влияние других загрязняющих веществ. Как было сказано выше поверхностно-активные вещества бытового назначения – анионные детергенты. Обычно они менее токсичны, чем неионные (Андруз, 1999).
***
Рассмотренные материалы свидетельствуют об опасности внесения в биосферу, несвойственных для нее веществ. Синтетические же вещества, попав в биосферу, практически не разлагаются ею, и, накапливаясь в пищевых цепях, как и тяжелые металлы, способны представить опасность для здоровья и жизни человека.
Контрольные вопросы
1. Что называют гидросферой?
2. Дайте объяснение аномальным свойствам воды.
3. Что такое тяжелая вода и где она используется?
4. Каким образом очищают воду с забором из поверхностных источников для получения питьевой воды?
5. Каким образом очищают воду с забором из подземных источников для получения питьевой воды?
6. Охарактеризуйте основные этапы очистки сточных вод.
7. Какие процессы протекают в аэротенках?
8. Какие Вам известны методы обеззараживания сточных вод? Дайте сравнительную характеристику.
9. Что такое эвтрофикация?
10. На какие группы делятся водоёмы по трофности?
11. Какое из питательных веществ чаще всего лимитирует рост растений во многих пресных водоёмах?
12. Какова роль фосфора в эвтрофировании?
13. Каковы хозяйственные последствия эвтрофирования?
14. Как нефтепродукты влияют на водные экосистемы?
15. Какие Вам известны ПАУ? Каким образом они влияют на гидросферу?
16. Назовите основные источники поступления токсичных металлов в водную среду? Какое влияние они оказывают? Приведите примеры.
17. Какие Вам извечтны хлорированные углеводороды? Каким образом они влияют на гидросферу?
18. Каким образом пестициды поступают в гидросферу? Каковы последствия?
19. Какие Вам известны детергены и каким образом они влияют на гидросферу?
Задачи
1. Рассчитать рН насыщенного при комнатной температуре раствора извести, если ПР[30] (Са(ОН)2)=5, 5*10-6. Расчет провести без учета коэффициента активности.
2. Значение коэффициента абсорбции кислорода водой составляет 0, 03. Рассчитать равновесную концентрацию кислорода в воде в мг/л при температуре 22 0С и давлении кислорода 1 амт.
3. Для флюорита СаF2 ПР=4*10-11. Рассчитайте максимальную концентрацию ионов фтора, которая может быть достигнута при растворении СаF2 при комнатной температуре в воде не содержащей ионов кальция.
4. Каковы концентрации ионов в насыщенном растворе доломита СаСО3*MgCO3, если ПР (СаСО3) и ПР (MgСО3) соответственно равны 4, 8*10-9 и 2, 1*10-5?
5. Равновесная концентрации СО2 в дождевой воде составляет 0, 7 мг/л. Константа диссоциации Н2СО3 по первой ступени К1=4, 5*10-7. Рассчитайте значение рН воды.
6. Концентрация Na2SO3 в сточных водах составляет 125 мг/л. При выпуске сточных вод в водоём концентрация Na2SO3 за счет разбавления природной водой уменьшилась в 10 раз. Насколько снизится концентрация растворенного кислорода в воде водоёма за счет его взаимодействия с Na2SO3.
7. Для обеззараживания и умягчения воды использовали пятиминутное кипячение, в результате которого общая жесткость[31] её снизилась с 5, 5 до 3, 1 мг-экв/л. Какое ориентировочное количество накипи образуется в чайнике в течение полугода, если ежедневно подобным образом в нем кипятят 3 л воды? Содержанием соединений магния в воде пренебречь.
8. На предприятии не хватило запаса соды для нейтрализации кислотных отходов, и 3, 15 кг азотной кислоты были вылиты в канализацию, а оттуда попали в пруд емкостью 10000 м3. После этого в пруду погибла вся рыба, даже такая неприхотливая, как плотва. Определите водородный показатель воды, загрязненной азотной кислотой.
9. Самый дешевый щелочной реагент для нейтрализации кислотных промышленных стоков - гашеная известь (гидроксид кальция). Используют как суспензию гидроксида кальция (" известковое молоко"), так и прозрачный раствор (" известковую воду"). Рассчитайте рН 0, 02М раствора Ca(OH)2.
10. Для определения железа в промышленной воде из 100 мл воды после упаривания и обработки о-фенантрамином было получено 25 мл окрашенного раствора. Оптическая плотность этого раствора в кювете с толщиной слоя 1 см оказалась 0, 46. Определить содержание железа в промышленной воде (в мг/л), если молярный коэффициент поглощения этого окрашенного соединения равен 1100.