
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Гидролиз соединений с ковалентной связью.
|
|
Наиболее типичными ковалентными соединениями являются соединения двух, трех и более элементов, мало отличающихся по электроотрицательности.
Особенностью таких соединений является то, что они в большинстве случаев на ионы не распадаются, а при нагревании в присутствии воды подвергаются полному гидролитическому разложению:
B2S2 + 6HOH ® 2H3BO3 + 3H2S
P2S5 + 8HOH ® 2H3PO4 + 5H2S
PCl5 + 4HOH ® H3PO4 + 5HCl
SO2Cl2 + 2HOH ® H2SO4 + 2HCl
SiCl4 + 2HOH ® SiO2¯ + 4HCl
Нитриды металлов гидролизуются с образованием аммиака:
Na3N + 3H2O ® 3NaOH + NH3
AlN + 3H2O ® Al(OH)3¯ + NH3
Карбиды гидролизуются с образованием гидроксида или оксида соответствующего элемента и углеводородов:
Al4C3 + 12H2O 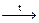 4Al(OH)3¯ + 3CH4
4Al(OH)3¯ + 3CH4
SiC + 2H2O 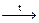 SiO2¯ + CH4
SiO2¯ + CH4
Гидролиз гидридов сопровождается окислительно-восстановительной реакцией: SiH4 + 2H2O 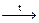 SiO2¯ + 4H2
SiO2¯ + 4H2