
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Ферментативный катализ и его особенности.
|
|
Все биохимические процессы протекают в присутствии катализаторов – ферментов.
Ферменты – это белковые молекулы, которые катализируют химические реакции в живых организмах.
Другое название ферментов – энзимы. В настоящее время известно около 2000 различных ферментов, около 150 ферментов удалось выделить в чистом виде.
Для веществ, участвующих в ферментативных реакциях приняты следующие названия:
· субстрат (S) – вещество, на которое фермент оказывает специфическое каталитическое действие;
· фермент (Е) – вещество, ускоряющее превращение субстрата;
· продукт (Р) – вещество, в которое превращается субстрат в результате ферментативного катализа.
Ферментативный катализ имеет свои особенности, отличающие его от обычного химического катализа:
ü Высокая эффективность. Реакции, катализируемые ферментами, ускоряются в десятки тысяч раз. Объясняется это тем, что при действии фермента на субстрат образуется фермент-субстратный комплекс, энергия активации которого значительно ниже энергии активации некаталитической реакции.
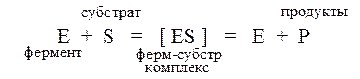
ü Высокая специфичность (избирательность). Каждый фермент катализирует только определенную биохимическую реакцию, т.е. действует только на определенный субстрат. Для объяснения такой высокой специфичности используется теория «ключ-замок» или «рука-перчатка». В.И. Слесарев «Химия. Основы химии живого», стр.117-118.
На активность ферментативного катализа влияют следующие факторы:
§ концентрация фермента
§ концентрация субстрата
§ температура
§ реакция среды (рН)
В.И.Слесарев «Химия. Основы химии живого», стр.116-119.