
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Работа 5. Определение константы скорости реакции окисления йодоводородной кислоты пероксидом водорода
|
|
Окисление йодоводородной кислоты протекает по уравнению:

При большом избытке Н2О2 реакция описывается кинетическим уравнением первого порядка. В этом случае константу скорости реакции можно рассчитать по уравнению.
Электропроводность исходной смеси HI и Н2О2 обусловлена наличием сильного электролита - HI. По мере протекания реакции электропроводность будет уменьшаться пропорционально концентрации электролита в растворе. Коэффициент пропорциональности между удельной электропроводностью и концентрацией электролита при подстановке в уравнение сокращается, поэтому для расчета константы скорости можно использовать следующее уравнение:
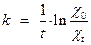 ,
,
где 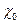 - электропроводность раствора в начальный момент времени, a
- электропроводность раствора в начальный момент времени, a 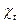 -электропроводность раствора в момент времени t.
-электропроводность раствора в момент времени t.