
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Очистка и обеззараживание питьевой воды
|
|
Подземные глубокие артезианские воды, а также воды родников и ключей, вытекающих часто с большой глубины, санитарном отношении являются наиболее благополучными. Они обладают лучшими физико-химическими свойствами и почти свободны от бактерий. Воды обладают более низкими физико-химическими свойствами и обычно имеют большое бактериальное загрязнение. Поэтому воды открытых водоемов, используемые при центральном водоснабжении, требуют предварительной очистки и обеззараживания.
Очистка улучшает физические свойства воды. Вода становится прозрачной, освобождается от окраски и запахов. При этом из воды удаляется большая часть бактерий, которые при отстаивании воды оседают.
Для очистки воды применяется несколько методов:
а) отстаивание;
б) коагуляция;
в) фильтрация.
ОТСТАИВАНИЕ
Для отстаивания воды устраиваются специальные резервуары-отстойники. Вода в этих отстойниках движется очень медленно и находится в них 6-8 часов, а иногда и больше. За это время из воды успевает осесть большая часть взвешенных в ней веществ, в среднем до 60%. При этом в воде остаются главным образом самые мелкие взвешенные частицы.
КОАГУЛЯЦИЯ ВОДЫ и ФИЛЬТРАЦИЯ
Для того, чтобы при отстаивании удалять мелкие взвешенные частицы, к воде еще до поступления ее в отстойники прибавляют коагулянты-осадители. Чаще всего для этого используется алюминий (глинозем) - Al2(SO4)3. Сернокислый глинозем действует на взвешенные в воде частицы двояким образом. Он имеет положительный электрический заряд, а взвешенные частицы - отрицательный. Разноименно заряженные частицы взаимно притягиваются, укрепляются и оседают. Кроме того, коагулянт образует в воде хлопья, которые оседая, захватывают и увлекают на дно взвешенные частицы. При применении коагулянта вода освобождается от большинства мелких взвешенных частиц, при этом срок отстаивания можно сократить до 3-4 часов. Однако при этом в воде еще остается часть мельчайших взвешенных веществ и бактерий, для удаления которых применяется фильтрация воды через песчаные фильтры. При эксплуатации фильтра на поверхности песка образуется пленка, состоящая из тех же взвешенных частиц и хлопьев коагулянта. Эта пленка задерживает взвешенные частицы и бактерии. Песчаные фильтры в среднем задерживают до 80% 6актерий.
Для того, чтобы освободить воду от остаточной микрофлоры, ее подвергают обеззараживанию.
ХЛОРИРОВАНИЕ ВОДЫ
Имеется несколько методов обеззараживания воды. Наиболее распространенным является метод хлорирования - обеззараживания воды с помощью хлорной извести или газooбpaзнoгo хлора.
Лабораторный контроль за коагуляцией и хлорированием воды имеет большое практическое значение. Прежде всего, необходимо определить дозы коагулянта и хлора, требуемые для очистки и обеззараживания данной воды, т.к. различные воды нуждается в разных количествах этих веществ.
КОАГУЛЯЦИЯ ВОДЫ СЕРНОКИСЛЫМ АЛЮМИНИЕМ
Как мы уже отмечали, наиболее распространенный метод коагуляции воды - обработка ее сернокислым алюминием.
Процесс коагуляции состоит в том, что раствор глинозема при прибавлении в воду вступает в реакцию с двууглекислыми солями кальция и магния (бикарбонатами) и образует с ними гидрат окиси алюминия в виде хлопьев. Реакция протекает по уравнению:
Al2(SO4)3 + 3Ca(HCO3)2 = 2A1(OH)3 + 3CaSO4 + 6С02
Потребная доза коагулянта зависит, в основном, от степени карбонатной (устранимой) жесткости воды. В мягкой воде, имеющей устранимую жёсткость меньше 4-5°, процесс коагуляции протекает плохо, т.к. здесь образуется мало хлопьев гидрата окиси алюминия. В таких случаях приходится добавлять в воду соду или известь (повышать устранимую жесткость), чтобы обеспечить образование достаточного количества хлопьев. Выбор дозы коагулянта имеет большое практическое значение, т.к. при недостаточной дозе коагулянта образуется мало хлопьев или нет хорошего эффекта осветления воды; избыток коагулянта придает воде кислый привкус. Кроме того, возможно последующее помутнение воды вследствие образования хлопьев.
ВЫБОР ДОЗЫ КОАГУЛЯНТА
Первый этап - определение устранимой жесткости. Берем 100 мл испытуемой воды, прибавляем 2 капли метилоранжа и титруем 0, 1н HCL до появления розовой окраски. Устранимая жесткость рассчитывается следующим образом: количество мл HCL (0, 1н), пошедшее на титрование 100 мл воды умножается на 2, 8.
Для точного определения дозы коагулянта целесообразно брать дозы 1% р-ра глинозема в соответствии с величиной устранимой (карбонатной) жесткости воды. В таблице расчета доз сернокислого алюминия показаны соотношения между устранимой жесткостью дозой коагулянта, а также показано количество сухого коагулянта, необходимого в том или ином случае для коагуляции 1л воды.
Коагуляцию проводят в 3 стаканах. В первый стакан с 200мл испытуемой воды прибавляют дозу 1% раствора глинозема, соответствующую устранимой жесткости воды, а в два других стакана последовательно - меньшие дозы коагулянта. Время наблюдения - 15 минут. Выбирают ту наименьшую дозу коагулянта, которая дает наиболее быстрое образование хлопьев и их оседание.
Пример: устранимая жесткость воды равно 7°. Этой величине жесткости по таблице соответствует доза 1% р-ра глинозема, 5, 6 мл на стакан 200мл воды, которую прибавляют в первый стакан, во второй стакан прибавляют дозу, соответствующую 6° жесткости - 4, 8 мл, а в третий стакан - 4мл. Стакан, в котором произойдет наилучшая коагуляция, покажет дозу 1% р-ра глинозема, необходимую для 200 мл воды, которую пересчитывают по той же таблице на сухой сернокислый алюминий в г на 1л воды.
ЛАБОРАТОРНАЯ РАБОТА СТУДЕНТОВ
Каждая пара студентов получает пробу воду, определяет устранимую жесткость воды, производит определение дозы коагулянта в 3 пробах воды, составляет протокол по следующему образцу:
ПРОТОКОЛ:
1. Название протокола - " Выбор дозы коагулянта"
2. Результаты определения оптимальной дозы коагулянта.
3. Расчет дозы, на большое количество воды (количество воды сухого коагулянта на 1м3 воды).
ХЛОРИРОВАНИЕ ВОДЫ
Существует 2способа хлорирования:
¾ нормальными дозами хлора, исходя из хлоропотребности воды;
¾ повышенными дозами хлора (перехлорирование).
Количество хлора, необходимое для обеззараживания воды, зависит от степени чистоты воды и, главным образом от загрязнения ее органическими веществами, а также от температуры воды. В гигиеническом отношении наиболее приемлемо хлорирование нормальными дозами, т.к. сравнительно небольшое количество вводимого хлора мало изменит вкус и запах воды и не потребует последующего дехлорирования воды.
Как правило, для хлорирования -воды берут такие количества хлорной извести, которые способны обеспечить наличие в воде 0, 3-0, 4 мг/л остаточного хлора на протяжении 30 минут контакта воды с хлором летом и 1-2 часов - зимой. Эти количества можно установить опытным хлорированием и последующим определением остаточного хлора в обработанной воде.
Хлорирование воды чаще всего производится 1% раствором хлорной извести.
Хлорная, или белильная известь представляет собой смесь гашеной извести - хлористого кальция и гипохлорита кальция: Са(ОН)2 + CaCl2 + CaOCl2
Гипохлорит кальция, контактируя с водой, выделяет хлорноватистую кислоту - НС1О. Соединение это нестойкое и распадается с образованием молекулярного хлора и атомного кислорода, которое и обладает основными бактерицидными эффектами. Хлор, который при этом выделяется, рассматривается как свободный активный хлор.
ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ АКТИВНОГО ХЛОРА В 1% РАСТВОРЕ ХЛОРНОЙ ИЗВЕСТИ
Определение активного хлора в растворах хлорной извести основано на способности хлора вытеснять йод из раствора йодистого калия. Выделившейся йод титруют 0, 01н р-ром гипосульфита.
Для определения активного хлора в растворе хлорной извести в колбу наливают 5мл отстоявшегося 1% раствора хлорной извести, прибавляют 25-50 мл дистиллированной воды, 5мл 5% раствора йодистого калия и 1мл серной кислоты (1: 3). Выделившийся йод титруют 0, 01н р-ром гипосульфита до слабо-розового окрашивания, затем добавляют 10-15 капель крахмала и титруют до полного обесцвечивания раствора. 1 мл 0, 01н раствора гипосульфита связывает 1, 27 мг йода, что соответствует 0, 355 мг хлора. Расчет ведется по формуле:
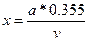 , где X - количество мг активного хлора, находившегося в 1 мл 1% раствора хлорной извести; а - количество мл 0, 01н р-ра гипосульфита, пошедшее на титрование; v - объем воды, взятой для анализа.
, где X - количество мг активного хлора, находившегося в 1 мл 1% раствора хлорной извести; а - количество мл 0, 01н р-ра гипосульфита, пошедшее на титрование; v - объем воды, взятой для анализа.
ОПРЕДЕЛЕНИЕ ПОТРЕБНОЙ ДОЗЫ ХЛОРА
При опытном хлорировании исходят ориентировочно из того, что для чистых вод с большим содержанием органических веществ (2-3 и даже 5 мг активного хлора на 1 л) в воду добавляют такое количество 1% раствора хлорной извести, чтобы активного хлора с избытком хватило для хлорирования исследуемой воды и осталось некоторое количество остаточного хлора.
Метод определения
В 3 колбы наливают по 200 мл исследуемой воды и добавляют пилоткой 1% р-р хлорной извести (1мл которого содержит примерно 2 мг активного хлора). В первую колбу добавляют 0, 1 мл хлорной извести, во вторую 0, 2 мл, в третью - 0, 3 мл, после чего воду перемешивают стеклянными палочками и оставляют на 30 минут. Через полчаса приливают в колбы по 1 мл 5% р-ра йодистого калия, серной кислоты и крахмала.Появление синего окрашивания указывает на то, что хлорпотребность воды полностью обеспечена и остался еще избыточный хлор. Окрашенная жидкость титруется 0, 01н р-ром гипосульфита и рассчитывается количество остаточного хлора и хлопотребность воды.
Пример расчета: в первой колбе посинение не наступило, во второй едва заметное, а в третьей колбе - интенсивное окрашивание. На титрование остаточного хлора в третьей колбе ушло 1 мл 0, 01н р-ра гипосульфита, следовательно, количество остаточного хлора равно 0, 355 мг. Хлорпотребность 200 мл исследуемой воды будет равна: 0, 6-0, 355=0, 245мг (если исходить из расчета, что 1 мл содержит 2 мг активного хлора, то в третью колбу внесли 0, 6мг активного хлора). Хлорпотребность исследуемой воды будет равна: (0, 245*1000)/200=1, 2 мг.
Прибавим к 1, 2 мг 0, 3 (контрольный остаточный хлор), получим потребную дозу хлора для исследуемой воды, равную 1, 5 мг на 1 л.
САМОСТОЯТЕЛЬНАЯ РАБОТА СТУДЕНТОВ
1. Ознакомиться с содержанием данного методического пособия.
2. Получить пробу воды для лабораторного анализа. Занести в протокол исследования сведения, полученные при обследовании водоисточника.
3. Провести определения физических свойств и химического состава краткого анализа.
4. Определить общую жесткость воды.
5. Провести определение содержания активного хлора в 1% р-ре хлорной извести.
6. Провести активное хлорирование с определением потребной дозы хлора.
7. Результаты исследования занести в протокол. Оценить качество исследуемой воды по физико-химическим показателям и данные обследования водоисточника. Составить заключение о возможности использования данной воды для хозяйственно-питьевых целей.
8. Рассмотреть ситуационные задачи по оценке воды по результатам санитарного обследования водоисточника и данным анализа воды.
ПРОТОКОЛ ИССЛЕДОВАНИЯ КАЧЕСТВА ВОДЫ ПОДЗЕМНЫХ ИСТОЧНИКОВ ВОДОСНАБЖЕНИЯ
Наименование источника водоснабжения________________________________________________________
Место взятия пробы__________________ наименование водоносного горизонта_______________________
Кем взята проба (фамилия, должность, организация)______________________________________________
Дата (число, час) взятия пробы_________________ время доставки пробы в лабораторию_______________
Дата производства анализа: начало___________________________ окончание_________________________
Адрес и наименование лаборатории_____________________________________________________________
1. Органолептические показатели качества воды
_________________
_________________
2. Показатели содержания токсических химических веществ
_________________
_________________
3. Микробиологические показатели воды
Число сапрофитных бактерий в 1мл
индекс бактерий группы кишечных палочек
Анализ проводили:
3аключение (основное)_______________________________________________________________________
Дата___________________ месяц_____________________________ год______________________________
Зав.отделением коммунальной гигиены_________________________________________________________
КОНТРОЛЬНЫЕ ВОПРОСЫ ПО ТЕМЕ
1. Физиологическое, санитарно-гигиеническое и эпидемиологическое значение воды.
2. Гигиеническая характеристика различных источников водоснабжения.
3. Требования к качеству питьевой воды (С ГОСТ 2874-82) и к качеству воды источников хозяйственно-питьевого водоснабжения (ГОСТ 17.1.3.00-77).
4. Методика санитарного обследования водоисточников (сущность санитарно-эпидемиологического обследования и санитарно-топографического обследования).
5. Понятие о биологических провинциях и эндемических заболеваниях. Биологически активные элементы в питьевой воде, их гигиеническая оценка.
6. Виды анализа воды (санитарно-химический, бактериологический, полный, краткий и т.д.).
7. Правила отбора проб воды для санитарно-химического и бактериологического анализов.
8. Гигиеническое значение физических и органолептических свойств воды и методы их определения (температура, цветность, запах, привкус, прозрачность и осадок воды при стоянии).
9. Активная реакция воды, ее нормы и методы определения.
10. Сухой остаток, его гигиеническое значение и метод определения.
11. Физиолого-гигиеническое значение жесткости воды и сущность метода ее определения.
12. Схема краткого санитарного анализа воды.
13. Биогенные элементы: азот аммиака, нитриты, нитраты, их значение и методы качественного определения.
14. Хлориды, их значение и методы определения.
15. Сульфаты, их значение и методы определения.
16. Соли железа, их значение и метод качественного определения.
17. Санитарное значение органических веществ в воде, источники их поступление в воду.
18. Методы очистки воды (отстаивание, коагуляция, фильтрация).
19. Методы обеззараживания воды.
20. Определение содержания активного хлора в 1% растворе хлорной извести.
21. Определение потребной дозы хлора для исследуемой воды