
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Сложные эфиры
|
|
Сложные эфиры — производные карбоновых кислот, в молекулах которых гидроксильная группа, входящая в состав карбоксильной группы, замещена на остаток спирта или фенола —OR':
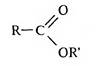
Номенклатура
Сложные эфиры называют по исходным кислоте и спирту или фенолу:
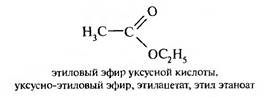
Способы получения
1. Взаимодействие галогенангидридов и ангидридов карбоновых кислот со спиртами и феноксидами щелочных металлов:
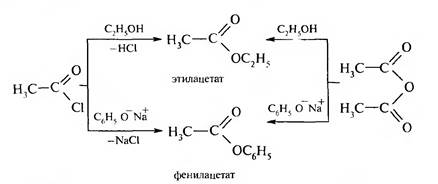
2. Взаимодействие карбоновых кислот со спиртами, катализируемое протоном кислоты (реакция этерификации):
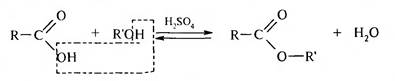
Равновесие наступает, когда прореагирует примерно 2/3 моля исходного вещества. Для смещения равновесия в сторону образования конечных продуктов отгоняют полученный эфир или берут какое-либо из исходных веществ в избытке.
Физические свойства
Сложные эфиры — чаще жидкости с приятным запахом с более низкими температурами кипения, чем соответствующие кислоты и спирты, что связано с отсутствием ассоциации.
Химические свойства
Сложные эфиры — типичные электрофилы. Из-за +М-эффекта атома кислорода, связанного с углеводородным радикалом, они проявляют менее выраженный электрофильный характер по сравнению с галогенангидридами и ангидридами кислот:
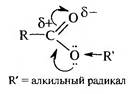
Электрофильность эфиров увеличивается, если углеводородный радикал образует с атомом кислорода сопряженную систему, т. н. активированные эфиры:
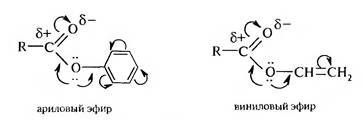
Сложные эфиры вступают в реакции нуклеофильного замещения.
1. Гидролиз сложных эфиров проходит как в кислой, так и в щелочной среде.
Кислотный гидролиз сложных эфиров — последовательность обратимых превращений, противоположных реакции этерификации:
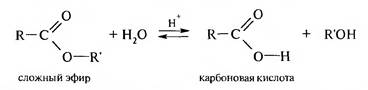
Механизм этой реакции включает протонирование атома кислорода карбонильной группы с образованием карбкатиона, который реагирует с молекулой воды:
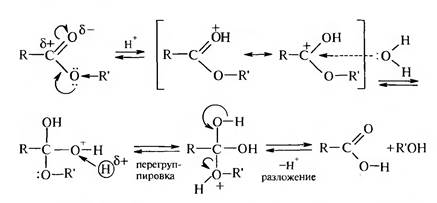
Щелочной гидролиз. Гидролиз в присутствии водных растворов щелочей проходит легче, чем кислотный потому, что гидроксид-анион более активный и менее объемный нуклеофил, чем вода. В отличие от кислотного, щелочной гидролиз необратим:
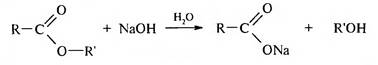
Щелочь выступает не в роли катализатора, а в роли реагента. Гидролиз начинается с нуклеофильной атаки гидроксид-ионом атома углерода карбонильной группы. Образуется промежуточный анион, который отщепляет алкоксид-ион и превращается в молекулу карбоновой кислоты. Алкоксид-ион, как более сильное основание, отрывает протон от молекулы кислоты и превращается в молекулу спирта:
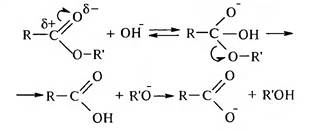
Щелочной гидролиз необратим потому, что карбоксилат-анион имеет высокую делокализацию отрицательного заряда и не восприимчив к атаке спиртового гидроксила.
Часто щелочной гидролиз сложных эфиров называют омылением. Термин произошел от названия продуктов щелочного гидролиза жиров — мыла.
2. Взаимодействие с аммиаком (аммонолиз) и его производными протекает по механизму, аналогичному щелочному гидролизу:
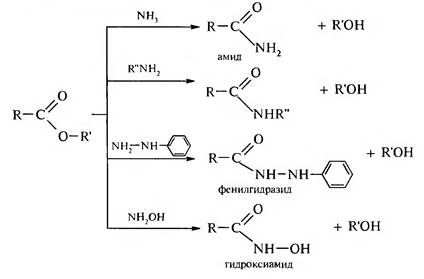
3. Реакция переэтерификации (алкоголиз сложных эфиров) катализируется как минеральными кислотами, так и щелочами:
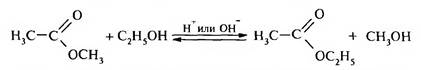
Для смещения равновесия вправо отгоняют более летучий спирт.
4. Сложноэфирная конденсация Кляйзена характерна для эфиров карбоновых кислот, содержащих атомы водорода в α -положении. Реакция протекает в присутствии сильных оснований:
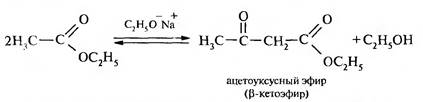
Алкоксид-ион отщепляет протон от α -углеродного атома молекулы эфира. Образуется мезомерно стабилизированный карбанион (I), который, выступая в роли нуклеофила, атакует атом углерода карбонильной группы второй молекулы эфира. Образуется продукт присоединения (II). Он отщепляет алкоксид-ион и превращается в конечный продукт (III). Таким образом, всю схему механизма реакции можно разделить на три стадии:
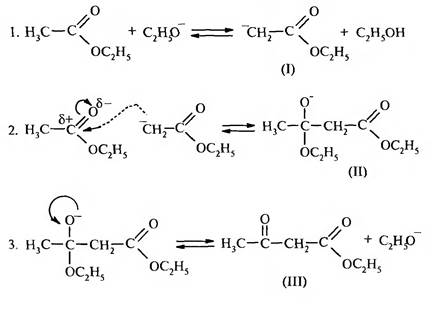
Если в реакцию вступают два сложных эфира, содержащие α -атомы водорода, то образуется смесь четырех возможных продуктов. Реакция используется для промышленного получения ацетоуксусного эфира.
5. Восстановление сложных эфиров:
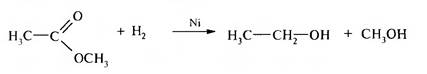
Первичные спирты образуются при действии газообразного водорода в присутствии скелетного никелевого катализатора (никель Ренея).
6. Действие магнийорганических соединений с последующим гидролизом приводит к образованию третичных спиртов:
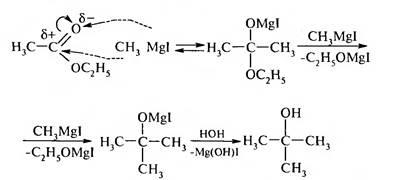
Сложные эфиры имеют большое значение как ацилируюшие реагенты, растворители, используются для синтеза альдегидов, кетонов, полимеров («органическое стекло» — плексиглас), лекарственных веществ: этилформиат — для производства витамина В. Бензилбензоат используют для лечения чесотки. Эти вещества известны как отдушки в парфюмерии (этилформиат, этилацетат) и компоненты пищевых эссенций: грушевой - изоамилацетат, яблочной — изоамилвалерат, ромовой — этилформиат, ананасовой — этилбутират.