
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Види та способи гартування.
|
|
Існує декілька видів та способів гартування. Вони різняться технологією та температурним режимом нагрівання і охолодження, фазовими та структурними змінами, характером дії та інше. Розрізняють об'ємне та поверхневе гартування.
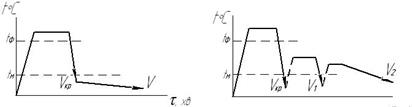
Найбільш широке застосування отримало гартування в одному охолоджувачі – безперервне або повне гартування. Для невеликих деталей складної форми і при необхідності зменшення деформації використовують ступінчате та ізотермічне гартування (рис. 12. а, б,).
а б
Рисунок 12. – Схеми гартування: а – ступінчате, б – ізотермічне.
При ступінчастому гартуванні вироби після нагрівання спочатку коротко охолоджують з критичною швидкістю, а надалі на повітрі, при цьому вирівнюється температура по перерізу виробу, зменшуються об'ємні напруження, уникає можливість утворення гартувальних тріщин, викривлення форми. Ізотермічне гартування аналогічне і відрізняється не принципово.
Поверхневе гартування виробів, на відміну від об'ємного, дозволяє зміцнювати тільки поверхневий шар на певну глибину. Його можна проводити двома способами. В одному випадку нагрівають тільки поверхневий шар, який потім гартують при охолоджуванні. В іншому - нагрівають весь виріб, але при гартуванні охолоджують тільки поверхневий шар із швидкістю більше критичної. Поверхневе гартування здійснюють індукційним способом, струмом високої частоти, плазмовим чи лазерним променем.
9. 4. Відпущення.
Термін " відпущення" звичайно використовують стосовно сталей і іншим сплавам, що зазнають при гартуванні поліморфне перетворення (двофазна алюмінієва бронза, деякі сплави на основі титана та ін.).
Термін " старіння", частіше всього, використовують стосовно сплавів, що не зазнають при гартуванні поліморфного перетворення (сплави на основі алюмінію, аустенітні сталі, нікелеві сплави і ін.).
Відпущення і штучне старіння- термічна обробка загартованих сплавів (головним чином стали), що включає нагрівання нижче 0, 4 Тпл, витримку і охолоджування. Швидкість охолоджування не впливає на структуру і властивості сплавів. Мета - досягнення оптимального поєднання міцності, пластичності і ударної в'язкості.
При відпущенні і штучному старінні в заздалегідь загартованих сплавах нагрів викликає процеси розпаду пересиченого твердого розчину (метастабільної фази), в результаті яких відбуваються фазові перетворення.
Відпущення і штучне старіння в 2...3 рази підвищують такі властивості сплаву як твердість, міцність, коерцитивну силу, питомий електричний опір і ін.
9.5. Термомеханічна обробка.
Термомеханічна обробка – це сукупність операцій деформації, нагріву і охолодження, в результаті яких формування остаточної структури і властивостей матеріалу відбувається в умовах збільшеної щільності і оптимального розподілу дефектів будови, створених пластичною деформацією.
В залежності від температури, при яких здійснюють деформацію і температури рекристалізації металу розрізняють високотемпературну (ВТМО) і низькотемпературну (НТМО) термомеханічну обробку.
При ВТМО сплав нагрівають до температур фазових перетворень у твердий розчин і деформують зі ступенем пластичної деформації 30 – 50%. Після деформації одразу проводять гартування, щоб уникнути розвитку рекристалізації.
По другому способу НТМО, сплав деформують в температурній зоні нижчій за температуру рекристалізації і фазових перетворень, ступінь пластичної деформації складає 75 – 95%. Гартування проводять одразу після деформації і виконують обов’язкове низькотемпературне відпущення.
ТМО дозволяє одночасно отримати дуже високу міцність з забезпеченням гарної пластичності. Також при цьому підвищується ударна в’язкість, тріщиностійкість, знижується поріг холодноламкості і крихкість.
9.6. Хіміко-термічна обробка.
Хіміко-термічна обробка (ХТО) – термічна обробка металів та сплавів в хімічно активних середовищах для зміни хімічного складу, структури і властивостей в поверхневих шарах.
Механізм ХТО включає:
- утворення в оточуючому середовищі (чи в окремому об’ємі) високої концентрації дифундуючого елемента в атомарному (іонізованому) стані;
- адсорбцію атомів (іонів) на поверхні матеріалу з утворенням хімічних зв’язків між іонами дифундуючого елемента і основного сплаву;
- дифузію адсорбованих атомів від поверхні в глибину оброблюваного матеріалу.
Концентрація активного елементу зменшується від поверхні в глибину металу. При цьому утворюється міцний легований поверхневий шар з поступовим переходом до основного металу.
Технологія ХТО найбільш результативна у випадку, коли дифундуючий елемент і основний метал взаємодіють з утворенням хімічних з'єднань чи твердих розчинів.
ХТО обробку металів класифікують: по виду дифундую чого елемента і по способу дифузійного насичення.
В залежності від насичуючого елементу виділяють такі види ХТО:
- цементація – насичення вуглецем – дозволяє збільшити працездатність виробів, що в процесі експлуатації витримують значні статичні, динамічні і перемінні навантаження а також абразивне зношення;
- азотування – азотом – підвищує твердість поверхневого шару (більш ніж цементація), його зносостійкість, границю витривалості і опір корозії в таких середовищах як пар, повітря, вода;
- нітроцементація – вуглецем і азотом одночасно;
- борірування – бором в певних середовищах – підвищує жаростійкість, корозійну стійкість, зносостійкість і твердість;
- силіціювання – кремнієм – збільшення корозійної стійкості в морській воді, азотній, сірчаній та соляній кислотах;
- алітірування – алюмінієм – для збільшення корозійної стійкості, та окалиностійкості;
- цинкування – цинком – для збільшення стійкості в атмосфері, воді, бензині та інших середовищах;
- нікелювання – нікелем – забезпечує підвищену стійкість проти газової корозії, окалиностійкість, високу корозійну стійкість та зносостійкість;
- хромування – хромом (аналогічно нікелюванню).
По способу дифузійного насичення застосовують:
- занурення в розплав;
- насиченням з розплавлених солей з електролізом чи без нього;
- насичення з сублімованої фази шляхом випаровування;
- насиченням з газової фази.
Хіміко-термічна обробка заклечається в нагріванні виробів до заданої температури і твердому, газовому чи рідкому середовищі, що легко виділяє дифундуючий елемент в атомарному стані, витримці при цій температурі та охолодженні з визначеною швидкістю.
На відзнаку від термічної обробки ХТО змінює не тільки структуру, але й хімічний склад поверхневих шарів сплаву, що дозволяє в більш широких межах змінювати властивості сплавів.
Хіміко-термічна обробка дозволяє збільшити поверхневу міцніть, твердість, опір поверхні ударнім навантаженням, зносостійкість, корозійну стійкість, окалиностійкість, жаростійкість.
Розділ ІІ. Конструкційні матеріали
Лекція 9
10. Загальна характеристика та класифікація металевих матеріалів.
Метали – прості речовини, які мають в звичайних умовах характерні властивості: високу електро- і теплопровідність, здатність відбивати електромагнітні хвилі, блиск, непрозорість, висока міцність та пластичність. Всім металам притаманний металевий тип хімічного зв’язку, який обумовлює кристалічну будову металів і наявність в кристалічних ґратках, не зв’язаних з атомними ядрами рухливих електронів, що забезпечує перелічені властивості. Слабкий зв'язок валентних електронів з атомами обумовлює хімічні властивості металів: вони легко утворюють основні окисли, солі, заміщують водень в кислотах та інше.
Металеві сплави в основі мають один чи більше металів, тому для них характерні ті ж властивості, що й для металів.
Метали і сплави в промисловості поділяють на дві основні групи: чорні та кольорові.
До чорних металів відносять сплави на основі заліза з різними хімічними елементами, а також кобальт, нікель і близький до них по властивостям марганець. Використання чорних металів широко розповсюджене, що зумовлено їх високим вмістом в земній корі, його невисокою вартістю, гарним поєднанням механічних і технологічних властивостей.
Кольорові метали більш різні за властивостями тому їх поділяють на:
- легкі метали, які мають невисоку щільність (γ ≤ 5000кг/м3): Ве, Mg, Al, Ti;
- тугоплавкі метали, з температурою плавлення більше ніж у заліза (1539°C): Ti, Cr, Zr, Nb, Mo, W, V;
- благородні метали – мають хімічну інертність: Ph, Pd, Pt, Ag, Au, Os;
- уранові метали – актіноіди, використовують в атомній техніці: U, Th, Pa;
- рідкоземельні метали – лантаноїди, використовують як присадку до сплавів: Ce, Pr, Nd, Sm;
- лужні метали, використовують як теплоносії чи каталізатори хімічних процесів: Li, K, Ca, Na.
11. Залізовуглецеві сплави.
11.1. Компоненти системи сплавів Fе – Fе3С та їх характеристика.
Основні компоненти залізовуглецевих сплавів це залізо (Fe) і вуглець (С).
Залізо (Fe) – метал білого кольору з сильно виявленими феромагнітними властивостями. Щільність заліза – 7800 кг/м3. Міцність невисока σ т.о. = 200...250МПа, твердість НВ = 60..80МПа, пластичність гарна δ = 40..50%. При нормальній температурі залізо має ОЦК решітку, але при збільшенні температури до 768º С (точка Кюрі) втрачає магнітні властивості. Втрата ця не пов'язана з перебудовою атомів у кристалічній решітці, однак ОЦК решітка при цьому зберігається. Щоб відрізнити магнітне Feα від немагнітного, немагнітне іноді називають Feβ . Залізо при зміні температури набуває поліморфних перетворень При температурі 911 °С Feβ перетворюється в Feγ з ГЦК решіткою. При температурі 1392 °С ГЦК решітка знову перетворюється в ОЦК. Цю модифікацію на відміну від низькотемпературної ОЦК решітки називають Feδ . При температурі 1539 °С залізо плавиться.
Критичні точки (температури), які відповідають фазовим перетворенням у залізі, мають спеціальні позначення. Так, температуру магнітного перетворення Feα → Feβ позначають через А2, температуру перетворення Feβ → Feδ - через А3 а температуру перетворення Feγ → Feδ - через А4. Крім того, коли йдеться про перетворення при нагріванні, то до позначення критичної точки додають індекс с (АС2,, АС3)а при перетвореннях, що відбуваються при охолодженні, - індекс r (Аr2, Аr3).Додавання до заліза інших компонентів зміщує положення критичних точок.
Вуглець (С) – це неметал з температурою плавлення 3500°С. Із залізом він утворює тверді розчини або хімічні сполуки, а в певних умовах може виділятись у вигляді графіту.
11.2. Діаграма стану залізовуглецевих сплавів. Характеристика фазового складу.
Гранична розчинність вуглецю в Feα при нормальній температурі (20°С) не перевищує 0, 006 %, а при t = 723°C граничний вміст вуглецю становить 0, 02%. Такий розчин є практично чистим залізом. Називають його ферит (Ф). Міцність фериту σ т.о. = 250..300 МПа, твердість 80...90 НВ, відносне видовження δ =30..40 %, відносне звуження ψ = 80%.
Твердий розчин вуглецю в Feγ називається аустеніт (А). Розчинність вуглецю в аустеніті з підвищенням температури збільшується від 0, 8% (727°С) до 2, 14 % (1147°С). Аустеніт немагнітний і має підвищену порівняно з феритом пластичність. Твердість аустеніту НВ = 160..200 МПа
Залізо з вуглецем утворює ряд хімічних сполук. З них практичне значення має карбід Fе3С, який містить 6, 67 % С. Цей карбід називають цементит (Ц). Цементит досить твердий (~ 800 НВ), але крихкий, міцність на розтяг σ т.о. ~ 40 МПа. Температура плавлення близько 1250 °С, при нормальній температурі цементит існує довго, а при t ≥ 950°С розпадається на залізо і графіт. Цементит є метастабільною фазою і на діаграмі стану зображується вертикальною лінією.
Отже, фазами в залізовуглецевих сплавах можуть бути ферит, аустеніт, цементит і графіт.
Діаграма стану системи сплавів Fе – Fе3С побудована в межах концентрації вуглецю від 0 до 6, 67 %, тобто до утворення першої хімічної сполуки - карбіду заліза Fе3С. Обмеження діаграми стану залізовуглецевих сплавів таким складом зумовлюється тим, що практично сплави цієї системи містять вуглецю менш як 5 %. Отже, компонентами залізовуглецевих сплавів можна вважати залізо (ферит) і цементит. Тому цю частину діаграми стану таких сплавів називають ще діаграмою залізо - цементит (Fе - Fе3С) (рис.13).
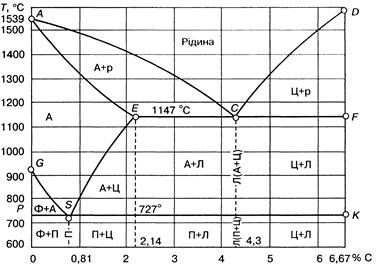 Сплави заліза з масовою часткою вуглецю до 4, 3 % починають тверднути на відрізку АС лінії ліквідус, виділяючи кристали твердого розчину аустеніту, а з масовою часткою вуглецю понад 4, 3 % - на відрізку СD лінії ліквідус, виділяючи кристали цементиту. Остаточно сплави тверднуть на лінії солідус АЕСF.
Сплави заліза з масовою часткою вуглецю до 4, 3 % починають тверднути на відрізку АС лінії ліквідус, виділяючи кристали твердого розчину аустеніту, а з масовою часткою вуглецю понад 4, 3 % - на відрізку СD лінії ліквідус, виділяючи кристали цементиту. Остаточно сплави тверднуть на лінії солідус АЕСF.
Рисунок 13. – Діаграма стану сплавів залізо – цементит (Fe – F3C)
Одразу після твердіння сплави, що лежать ліворуч від точки Е (2, 14% С), є однорідними і складаються з зерен аустеніту, а ті, що містяться праворуч від точки Е, становлять механічну суміш із зерен аустеніту і цементиту. При цьому в сплаві з концентрацією 4, 3 % вуглецю (точка С) утворюється однорідна евтектична суміш, яку називають ледебурит (Л).
Отже, точка Е поділяє діаграму стану залізовуглецевих сплавів на дві частини. Сплави ліворуч від цієї точки тверднуть відповідно до лінії AЕ і після затвердіння мають однорідну структуру, що складається з зерен аустеніту. Ці сплави називають сталями. Внаслідок однорідності структури сталі мають високу пластичність, яка дає змогу обробляти їх тиском (куванням, прокатуванням).
У сплавах, що містяться праворуч від точки Е, кристалізація закінчується при сталій температурі 1147 °С (лінія ЕСF) з утворенням евтектики - ледебуриту. Ці сплави називають чавунами. Наявність крихкої та більш легкоплавкої евтектики не дає змоги обробляти чавуни тиском, проте поліпшує їхні ливарні властивості.
Остаточна структура сталей і чавунів, що її спостерігають при нормальній температурі, зумовлюється рядом перетворень у твердому стані, які відбуваються при температурах, що відповідають лініям СS, SЕ і РSК діаграми стану залізовуглецевих сплавів.