
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Решение. 1. Напишем уравнение реакции осаждения трехвалентного хрома гидроксидом кальция:
|
|
1. Напишем уравнение реакции осаждения трехвалентного хрома гидроксидом кальция:
2Cr3+ + 3Ca(OH)2 = 2Cr(OH)3 + Ca2+.
2. Рассчитаем количество трехвалентного хрома, содержащегося в 1 м3 (или 1000 л) раствора. Составляем пропорцию:
2, 5 моль Cr3+ содержится в 1 л раствора
Х –«– –«– –«– –«– в 1000 л раствора
Х = 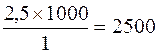 моль.
моль.
3. Рассчитаем количество молей Са(ОН)2, необходимых для полного осаждения трехвалентного хрома. Из уравнения реакции следует:
на 2 моля Cr3+ приходится 3 моля Са(ОН)2
на 2500 молей Сr3+ приходится Х молей Са(ОН)2
Х = 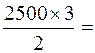 3750 молей Са(ОН)2.
3750 молей Са(ОН)2.
4. Рассчитываем массу гидроксида кальция, необходимого для осаждения Cr3+:
1 моль Са(ОН)2 весит 74 г
3750 молей Са(ОН)2 весят Х г
Х = 3750× 74 = 277500 г = 277, 5 кг.
Задача 3.1. Определите вид сточной воды (кислая или щелочная), если концентрация ионов ОН- равна (моль/л).
| Вариант | [ОН-], моль/л | Вариант | [ОН-], моль/л |
| 4× 10-3 | 2, 3× 10-3 | ||
| 5, 8× 10-8 | 3, 5× 10-13 | ||
| 0, 2× 10-7 | 8, 4× 10-6 | ||
| 4, 7× 10-2 | 0, 5× 10-2 | ||
| 3, 6× 10-5 | 5, 6× 10-1 | ||
| 7× 10-4 | 6× 10-3 | ||
| 2× 10-6 | 2, 8× 10-10 | ||
| 0, 5× 10-7 | 7, 8× 10-6 | ||
| 8, 2× 10-3 | 6× 10-8 | ||
| 3, 5× 10-2 | 5× 10-10 | ||
| 9× 10-7 | 4× 10-12 | ||
| 5, 3× 10-6 | 6, 9× 10-9 | ||
| 8× 10-11 | 7× 10-5 | ||
| 4, 5× 10-5 | 9, 5× 10-4 | ||
| 2, 5× 10-3 | 5, 7× 10-11 |
Задача 3.2. Определите соответствие санитарно-токсикологи-ческим нормам воды в водоеме, если в водоем вместимостью (А) с дождевыми водами объемом (В) занесено (Д) кг удобрения, исполь-зуемого на полях.
| Вариант | Удобрение | Объем водоема (А), м3 | Объем дождевых вод (В), м3 | Количество занесенных удобрений (Д), кг |
| Сульфат аммония ((NH4)2SО4) | 1, 5 | |||
| Хлористый аммоний (NH4Cl) | 2, 0 | |||
| Аммиачная селитра (NH4NO3) | 1, 0 | |||
| Кальциевая селитра (Са(NО3)2) | 1, 8 | |||
| Хлористый калий (KCl) | 2, 0 | 3, 5 | ||
| Сульфат аммония ((NH4)2SО4) | 1, 5 | |||
| Хлористый аммоний (NH4Cl) | 2, 0 | |||
| Аммиачная селитра (NH4NO3) | 1, 0 | |||
| Кальциевая селитра (Са(NО3)2) | 1, 8 | |||
| Хлористый калий (KCl) | 2, 0 | 3, 5 | ||
| Сульфат аммония ((NH4)2SО4) | 1, 5 | |||
| Хлористый аммоний (NH4Cl) | 2, 0 | |||
| Аммиачная селитра (NH4NO3) | 1, 0 | |||
| Кальциевая селитра (Са(NО3)2) | 1, 8 | |||
| Хлористый калий (KCl) | 2, 0 | 3, 5 | ||
| Сульфат аммония ((NH4)2SО4) | 1, 5 | |||
| Хлористый аммоний (NH4CI) | 2, 0 | |||
| Аммиачная селитра (NH4NO3) | 1, 0 | |||
| Кальциевая селитра (Са(NО3)2) | 1, 8 | |||
| Хлористый калий (KCl) | 2, 0 | 3, 5 | ||
| Сульфат аммония ((NH4)2SО4) | 1, 5 | |||
| Хлористый аммоний (NH4Cl) | 2, 0 | |||
| Аммиачная селитра (NH4NO3) | 1, 0 | |||
| Кальциевая селитра (Са(NО3)2) | 1, 8 | |||
| Хлористый калий (KCl) | 2, 0 | 3, 5 | ||
| Сульфат аммония ((NH4)2SО4) | 1, 8 | |||
| Хлористый аммоний (NH4CI) | 2, 5 | |||
| Аммиачная селитра (NH4NO3) | 1, 5 | |||
| Кальциевая селитра (Са(NО3)2) | 2, 8 | |||
| Хлористый калий (KCl) | 2, 5 | 3, 5 |
Задача 3.3. Для очистки сточной воды от токсичного шести-валентного хрома Cr (VI) в виде K2Cr2O7 с концентрацией с моль/л в качестве восстановителя использовали реагент. Напишите уравнение реакции и рассчитайте количество реагента, необходимого для полного восстановления Cr (VI), находящегося в объеме V м3 электролита.
| Вариант | Реагент | с (K2Cr2O7) моль/л | Вариант | Реагент | с (K2Cr2O7) моль/л |
| SO2 | 0, 5 | Na2SO3 | 2, 5 | ||
| FeSO4 | 1, 0 | SO2 | 3, 5 | ||
| Na2SO3 | 1, 3 | FeSO4 | 0, 8 | ||
| FeSO4 | 1, 7 | Na2SO3 | 3, 7 | ||
| Na2SO3 | 2, 3 | SO2 | 8, 2 | ||
| SO2 | 4, 5 | FeSO4 | 4, 2 | ||
| FeSO4 | 5, 8 | Na2SO3 | 5, 6 | ||
| Na2SO3 | 0, 6 | SO2 | 0, 7 | ||
| SO2 | 0, 9 | FeSO4 | 6, 0 | ||
| FeSO4 | 1, 5 | Na2SO3 | 5, 7 | ||
| Na2SO3 | 2, 0 | SO2 | 0, 9 | ||
| SO2 | 1, 4 | FeSO4 | 7, 0 | ||
| FeSO4 | 5, 5 | Na2SO3 | 2, 6 | ||
| Na2SO3 | 4, 6 | SO2 | 3, 4 | ||
| SO2 | 7, 0 | FeSO4 | 5, 5 |
Задача 3.4. При электролизе сточной воды объемом 1, 5 м3 на катоде выделился металл. Определите: силу тока, прошедшего через раствор (варианты 1-7), количество электричества, необходимое для электролиза сточной воды (варианты 8-15), массу металла выделившегося на катоде (варианты 16-21), электрохимический эквивалент металла (варианты 22-25), время электролиза (варианты 26-30).
| Вариант | I, A | τ | Me n + | m, г | η, % |
| - | 2 ч | Ni2+ | |||
| - | 40 с | Cu2+ | 1, 5 | ||
| - | 2, 5 ч | Co2+ | |||
| - | 35 с | Cd2+ | |||
| - | 15 ч | Fe2+ | |||
| - | 50 мин | Bi3+ | |||
| - | 5 ч | Zn2+ | |||
| - | - | Ni2+ | |||
| - | - | Y3+ | |||
| - | - | Hg+ | |||
| - | - | Ta5+ | |||
| - | - | Al3+ | |||
| - | - | Cu+ | 0, 253 | ||
| - | - | Pb2+ | 345, 5 | ||
| - | - | Fe3+ | 65, 5 | ||
| 20 мин | Cu2+ | - | |||
| 1, 5 ч | Co2+ | - | |||
| 40мин | Cd2+ | - | |||
| 45 мин | Ni2+ | - | |||
| 60 с | Pb2+ | - | |||
| 2 ч | Cd2+ | - | |||
| 25 мин | - | ||||
| 1, 6 ч | - | ||||
| 65 мин | - | ||||
| 120 мин | - | ||||
| - | Сu+ | ||||
| - | Ni2+ | 540, 5 | |||
| - | Co2+ | ||||
| - | Pb2+ | ||||
| - | Cd2+ | 130, 9 |
Задача 3.5. Рассчитайте массу гидроксида кальция Ca(OH)2 необходимого для полного осаждения иона тяжелого металла, содержащегося в ванне гальванического производства объемом V м3.
| Вариант | Men+ | c (Me), моль/л | V, м3 | Вариант | Men+ | c (Me), моль/л | V, м3 |
| Ni2+ | 0, 5 | 0, 5 | Cu2+ | 2, 5 | 1, 0 | ||
| Cu2+ | 1, 0 | 1, 0 | Co2+ | 3, 5 | 0, 8 | ||
| Co2+ | 1, 3 | 1, 2 | Mn2+ | 0, 8 | 0, 6 | ||
| Cd2+ | 1, 7 | 1, 1 | Ni2+ | 3, 7 | 1, 2 | ||
| Fe2+ | 2, 3 | 1, 3 | Pb2+ | 8, 2 | 1, 5 | ||
| Cr3+ | 4, 5 | 1, 4 | Cd2+ | 4, 2 | 1, 4 | ||
| Mn2+ | 5, 8 | 0, 9 | Nb5+ | 5, 6 | 1, 1 | ||
| Ni2+ | 0, 6 | 1, 5 | Al3+ | 0, 7 | 0, 5 | ||
| Y3+ | 0, 9 | 1, 0 | Cd2+ | 6, 0 | 1, 3 | ||
| Cu+ | 1, 5 | 1, 1 | Cr3+ | 5, 7 | 0, 9 | ||
| Ni2+ | 2, 0 | 1, 2 | Сu+ | 0, 9 | 0, 8 | ||
| Al3+ | 1, 4 | 1, 3 | Ni2+ | 7, 0 | 1, 0 | ||
| Cu+ | 5, 5 | 1, 4 | Co2+ | 2, 6 | 1, 2 | ||
| Pb2+ | 4, 6 | 0, 8 | Pb2+ | 3, 4 | 1, 3 | ||
| Fe3+ | 7, 0 | 0, 7 | Cd2+ | 5, 5 | 1, 4 |