
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Және элементтеріне қысқаша сипаттама.
|
|
Периодтық системада сутектің алатын орны ерекше.
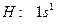 . Сілтілік металдарғ а ұ қ сас қ абілетіне қ арай сутек +1 тотығ у дә режесін
. Сілтілік металдарғ а ұ қ сас қ абілетіне қ арай сутек +1 тотығ у дә режесін 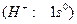 жә не оғ ан қ оса –1 тотығ у дә режесін
жә не оғ ан қ оса –1 тотығ у дә режесін 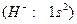 кө рсетеді. Сондық тан оны сілтілік металдар жә не галогендер тобына орналастыруғ а болады.
кө рсетеді. Сондық тан оны сілтілік металдар жә не галогендер тобына орналастыруғ а болады.
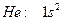 , конфигурациясы сілтілік-жер металдарына, ал қ асиеттері (инерттілігі) бойынша асыл газдарғ а жақ ын.
, конфигурациясы сілтілік-жер металдарына, ал қ асиеттері (инерттілігі) бойынша асыл газдарғ а жақ ын.
Периодтар бойынша атомдардың электрон қ абаттарынның саны ө згермейді.
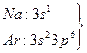 3-қ абат. Бірақ ядро заряды
3-қ абат. Бірақ ядро заряды 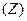 +11-ден +18-ге дейін ө седі, атомдар кө лемдері сығ ылады, бұ нда 2 процесс бә секелеседі: 1) 1
+11-ден +18-ге дейін ө седі, атомдар кө лемдері сығ ылады, бұ нда 2 процесс бә секелеседі: 1) 1 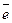 -ды тебу (
-ды тебу (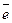 - тебу), 2) электронды – ядролық тартылу. Біріншісі атом радиусын ұ лғ айтады, екіншісі азайтады, нә тижесінде екіншісі жең еді. Радиустың азаюымен қ асиеттері ө згереді. Осығ ан сә йкес период бойымен иондану потенциалы, электрон тартқ ыштық, СЭТ, бейметалдық қ асиеті жә не т.б. артады.
- тебу), 2) электронды – ядролық тартылу. Біріншісі атом радиусын ұ лғ айтады, екіншісі азайтады, нә тижесінде екіншісі жең еді. Радиустың азаюымен қ асиеттері ө згереді. Осығ ан сә йкес период бойымен иондану потенциалы, электрон тартқ ыштық, СЭТ, бейметалдық қ асиеті жә не т.б. артады.
А топтарында (негізгі топшаларда) жоғ арыдан тө мен тұ тас алғ анда атом радиусы ұ лғ аяды, есесіне иондану потенциалы, электрон тартқ ыштық, СЭТ, бейметалдық қ асиеттері азаяды. Бұ л тә уелділікті мұ қ ият қ арастырғ анда ішкі максимум жә не минимум болатынын байқ аймыз. Топ бойынша қ асиеттің біркелкі емес ө згеруі екіншілей периодтық пен, ал период бойынша біркелкі емес ө згеруі іштей периодтық қ ұ былысымен байланысты.
Период бойымен солдан оң ғ а қ арай тотығ у дә режелерінің тұ рақ тылығ ы ө згереді: жұ п топтарда жұ п тотығ у дә режелері, ал тақ топтарда тақ тотығ у дә режелері тұ рақ ты.
Мысалы, бор топшасы ү шін +1, +3, ал кө міртек топшасы ү шін +2, +4 тотығ у дә режелері тұ рақ ты.
Период бойынша солдан оң ғ а қ арай жоғ арғ ы тотығ у дә режесінің тұ рақ тылығ ы кемиді, себебі: 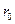 (орбиталь радиус) жә не т.б. қ асиеттері азаяды, ол ө з кезегінде
(орбиталь радиус) жә не т.б. қ асиеттері азаяды, ол ө з кезегінде 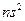 - электрондарының байланыс тү зуге қ атысуын қ иындатады.
- электрондарының байланыс тү зуге қ атысуын қ иындатады.
Мысалы, 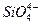 ,
, 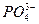 ,
, 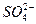 ,
, 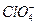 қ атарында тұ рақ тылық кеміп, тотық тырғ ыштық қ асиеті артады.
қ атарында тұ рақ тылық кеміп, тотық тырғ ыштық қ асиеті артады.
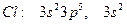 электронының байланыс тү зуге қ атысуы қ иынырақ.
электронының байланыс тү зуге қ атысуы қ иынырақ. 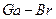 қ атарында (
қ атарында (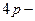 элементтері)
элементтері) 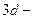 сығ ылу,
сығ ылу, 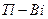 қ атарында (
қ атарында (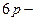 элементтері)
элементтері) 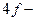 сығ ылу болады.
сығ ылу болады. 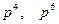 электрондарының тұ рақ тылығ ы аз.
электрондарының тұ рақ тылығ ы аз.
Сыртқ ы 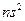 электрондарының байланыс тү зуге қ атысуы қ иын.
электрондарының байланыс тү зуге қ атысуы қ иын. 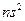 электрондарының арасында активтігі ең тө мені
электрондарының арасында активтігі ең тө мені 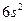 - электрондары, сондық тан оларды инертті
- электрондары, сондық тан оларды инертті 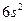 жұ бы деп атайды.
жұ бы деп атайды.
Электрондық конфигурациялары бойынша негізгі топша элементтері электрондары жетімсіз жә не артық элементтер болып бө лінеді. Оларды IIIA жә не IVA топтарының арасынан ө тетін Цинтл шекарасы деп аталатын тү зу бө леді.
|
|
| IIIA | IVA | 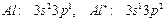
| | | | ||
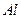
| 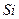
|
орбиталь саны электрон санынан артық, металдық қ асиет кө рсетеді.
|
|
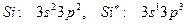
| | | | |
Электрон жеткілікті. Электронның жеткілікті жә не артық болуы (IVА-ның оң жағ ында) бейметалдық қ асиет кө рсетуін тудырады.
Сутек.
 .
.
Д.И.Менделеевтің қ азіргі периодтық кестесінде сутек VIIА тобында фтордың ү стінде орналасқ ан. Бұ л орын периодтылық тың қ азіргі физикалық мағ ынасына сә йкес келеді. Сутек-сілтілік металдармен жә не галогендермен ұ қ састығ ынан басқ а ө зіндік қ асиеті бар айрық ша элемент.
1) сілтілік металдармен ұ қ састығ ы:
а) жалғ ыз валенттік электроны болуы (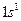 );
);
ә) оң зарядты  ионын (
ионын ( сияқ ты) тү зуі;
сияқ ты) тү зуі;
б) оптикалық спектрлерінің ұ қ састығ ы;
в) молекулалық орбитальдарының 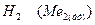 сипатының бірдейлігі;
сипатының бірдейлігі;
г) тотық сыздандырғ ыштық қ асиет кө рсетуі.
2) галогендермен ұ қ састығ ы:
а) 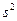 болуғ а 1
болуғ а 1 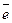 жетпейді, галогендерде –
жетпейді, галогендерде – 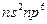 болуғ а;
болуғ а;
ә) сутек -1 тотығ у дә режесін кө рсетеді;
б) сутектің иондану энергиясының 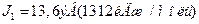 мә ні жоғ ары;
мә ні жоғ ары;
в) тотық тырғ ыштық қ асиет кө рсетеді (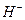 );
);
г) екі атомды молекула – 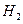 , сутек галогендер сияқ ты газ.
, сутек галогендер сияқ ты газ.
3) сутектің айырмашылығ ы:
а) ион  тү рінде жалаң ядро (протон) болатын жалғ ыз элемент;
тү рінде жалаң ядро (протон) болатын жалғ ыз элемент;
ә) сутек тіпті 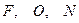 - мен де иондық қ осылыс тү збейді (
- мен де иондық қ осылыс тү збейді (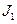 ө те жоғ ары);
ө те жоғ ары);
б)  оний - иондарын тү зеді (
оний - иондарын тү зеді (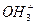 - гидроксоний,
- гидроксоний, 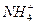 - аммоний,
- аммоний, 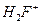 - фтороний), тек +1 тотығ у дә режесіндегі сутек қ осылыстарына тә н ерекше байланыс тү рі – сутектік байланыс тү зіледі.
- фтороний), тек +1 тотығ у дә режесіндегі сутек қ осылыстарына тә н ерекше байланыс тү рі – сутектік байланыс тү зіледі.
Сутек ең кө п химиялық қ осылыс тү зеді. Табиғ атта кең тарағ ан, ол су, саз балшық, кө мір, мұ най, барлық жануарлар мен ө сімдік организмдерінің қ ұ рамына кіреді (жер қ ыртысындағ ы мө лшері 0, 88%, таралуы бойынша 9-орын алады). Одан басқ а сутек Кү ннің жә не кө птеген жұ лдыздардың жартысынан астамын қ ұ райды.
Табиғ и сутек изотоптар қ оспасы болғ анымен, негізінен (~99, 98 масс.%) протийден тұ рады.
Қ алыпты жағ дайда сутек – тү ссіз, иіссіз, дә мсіз жең іл газ. Сутек молекуласының беріктігі жоғ ары (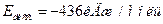 ).
).
Ө неркә сіпте алынуы:
1) конверсия ә дісі;
2) қ атты отынды газификациялау;
3) кө мірсутектерін тотық тыру;
4) кокс газын жә не мұ най ө ң деу газдарын терең салқ ындату;
5) сілті ерітіндісін электролиздеу.
Лабораторияда сұ йылтылғ ан 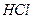 жә не
жә не 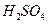 -ке
-ке 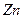 -пен ә сер етіп алады.
-пен ә сер етіп алады.
Химиялық ө неркә сіпте 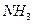 ,
, 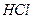 ,
,  ө ндірісінде, қ атты жә не сұ йық отынды жә не майларды гидрогендеу ү шін қ олданылады. Қ иын балқ итын металдарды дә некерлеуде жә не кесуде пайдаланылады. Сұ йық сутек тө менгі температура техникасында, реактивті техникада реактивті отын ретінде қ олданылады, ол «экологиялық таза» жанармай. Сутек - болашақ тың химиялық технологиясының жә не энергетикасының негізі.
ө ндірісінде, қ атты жә не сұ йық отынды жә не майларды гидрогендеу ү шін қ олданылады. Қ иын балқ итын металдарды дә некерлеуде жә не кесуде пайдаланылады. Сұ йық сутек тө менгі температура техникасында, реактивті техникада реактивті отын ретінде қ олданылады, ол «экологиялық таза» жанармай. Сутек - болашақ тың химиялық технологиясының жә не энергетикасының негізі.
Молекулалық сутектің химиялық активтігі тө мен, ал атомдық сутек активті. Кә дімгі жағ дайда 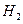 фтормен, хлормен (жарық та) тікелей ә рекеттеседі. Қ ыздырғ анда кө птеген металдармен, бейметалдармен жә не кү рделі заттармен ә рекетке тү седі.
фтормен, хлормен (жарық та) тікелей ә рекеттеседі. Қ ыздырғ анда кө птеген металдармен, бейметалдармен жә не кү рделі заттармен ә рекетке тү седі.
Сутектің барлық бинарлы қ осылыстарын 3 негізгі класқ а бө луге болады: 1) тұ з тә різді (ионды) гидридтер – 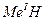 ,
, 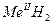 ;
;
2) металл тә різді (металдық байланыс) – кө птеген ауыспалы металдар гидридтері;
3) ұ шқ ыш (ковалентті) IVА-VIIА топтары элементтерінің гидридтері.
Осығ ан сә йкес олардағ ы химиялық байланыс табиғ аты, қ ышқ ыл-негіздік қ асиеті, қ ұ рылымы, агрегаттық кү йі ө згереді.
Сутектік байланыс тың тү зілуі сұ йық тарда олардың физикалық қ асиеттеріне ә сер ететін ассоциаттар: 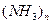 ,
, 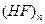 ,
, 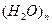 тү зілуін тудырады. Мысалы, егер сұ йық суда сутектік байланыс болмаса, судың қ айнау температурасы +1000С емес, -800С болар еді.
тү зілуін тудырады. Мысалы, егер сұ йық суда сутектік байланыс болмаса, судың қ айнау температурасы +1000С емес, -800С болар еді.
Су.
Сутектің негізгі қ осылысы – су тек 0, 00760С жә не 610, 381 Па – ү штік нү ктеде ғ ана бірмезгілде ү ш фазада бола алады. Судың максималь тығ ыздығ ы +40С-та. Су тығ ыздығ ы аномалиясының қ ататын суаттарда ө мір сү ретін жә ндіктердің ө мірі ү шін маң ызы ө те зор.
Су – сұ йық, полюсті молекула, идеал амфолит, реакцияғ а ө те қ абілетті зат. Тотық тырғ ыш, тотық сыздандырғ ыш болумен бірге, гидролиз, аквакомплекс тү зу, тотығ у-тотық сыздану процестеріне қ атысады. Суда кө птеген бейорганикалық қ ышқ ылдар, негіздер жә не тұ здар ериді. Су бірқ атар химиялық процестерде катализатор болады.