
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Электролиз
|
|
Электролизом называется совокупность процессов, протекающих при прохождении постоянного электрического тока через систему, состоящую из двух электродов и расплава или раствора электролита. Во время электролиза положительно заряженные ионы перемещаются к катоду, который соединяется с отрицательным полюсом внешнего источника постоянного тока, а отрицательно заряженные ионы перемещаются к аноду, который соединяется с положительным полюсом источника постоянного тока. На поверхности катода идет процесс восстановления, на аноде – окисление.
Рассмотрим электролиз расплава хлорида натрия.
При погружении в расплав, состоящий из ионов Na+ и Cl-, двух графитовых электродов, подключенных к источнику тока, в электролите начнется направленное движение ионов, и на электродах будут протекать окислительно-восстановительные процессы.
Схема электролиза расплава натрия:
NaCl = Na+ + Cl-
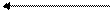
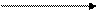
 катод (-) (+) анод
катод (-) (+) анод
Na + + e- = Na0 2Cl- - 2e- = Cl2
Суммарное уравнение реакции:
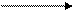 2Na+ + 2Cl- электролиз 2 Na + Cl2
2Na+ + 2Cl- электролиз 2 Na + Cl2
 2NaCl электролиз 2Na + Cl2
2NaCl электролиз 2Na + Cl2
При электролизе водных растворов электролитов полярные молекулы воды притягиваются и к катоду, и к аноду, и также могут участвовать в процессах на электродах.