
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Вычисление стандартных электродных реакций, исходя из известных
|
|
Если имеется набор полуреакций с известными значениями стандартных электродных потенциалов, то можно определить стандартный электродный потенциал любой новой полуреакции, которую можно представить как линейную комбинацию имеющихся.основанием к такому подходу является определение электродного потенциала полуреакции Ox + ne = Red как ЭДС окислительно - восстановительной реакции Ox + n/2Н2 = Red + n Н+, осуществляемой в электрохимической цепи.
Например:
Дано: EoFe3+/Fe = -0, 04 B; EoFe2+/Fe = -0, 44 B
Найти EoFe3+/Fe2+.
Решение: (1) Fe3+ +3e = Fe n1 × EoFe3+/Fe =- 3× 0, 04 = -0, 12 B
(2) Fe2+ +2e = Fe n2 × EoFe2+/Fe =- 2× 0, 44 = -0, 88 B
(3) Fe3+ +e = Fe2+ (3) = (1) – (2) Þ
Þ n3 × EoFe3+/Fe2+ = n1 × EoFe3+/Fe - n2 × EoFe2+/Fe =0, 76 B
Дано: EoCr3+/Cr 2 + = -0, 41 B; EoCr2O72-/ Cr3+ = +1, 33 B
Найти EoCr2O72-/ Cr2+.
Решение: (1) x1|Cr2O72- + 14H+ + 6e = 2Cr3+ + 7H2O EoCr2O72-/ Cr3+
(2) x2| Cr3+ + e = Cr2+ EoCr3+/Cr 2 +
_____________________________________________________________________________________________
(3) Cr2O72- + 14H+ + 8e = 2Cr2+ + 7H2O EoCr2O72-/ Cr2+
(3) = (1) +2 (2) Þ 8× EoCr2O72-/ Cr2+= 6× EoCr2O72-/ Cr3+ +2 × EoCr3+/Cr 2 +=6× 1, 33 + 2× (-0, 41)=
= 7, 16 B
EoCr3+/Cr 2 + = 1/8× 7, 16 = 0, 895 B
Расчёт реальных потенциалов различных систем
| система | Уравнение Нернста |
| 1. H2O + e– ® 1/2H2(г) + OH– 2. H2O - 2e– ® 1/2О2(г) + 2H+ 3.MnO4- + 8H+ ®Mn2+ + 4H2O | 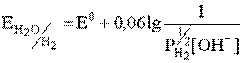 ,
или ,
или  когда р(н2) = 1 когда р(н2) = 1
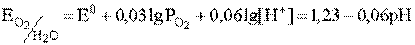
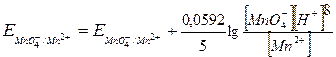 ; ; 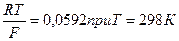 
|