
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Термические превращения углеводородов в газовой фазе
|
|
8.3.1. Превращения алканов. Термические реакции превращения алканов приводят к образованию низших алканов и алкенов.
Метан СН 4 термически очень устойчив. Начало его термической деструкции при атмосферном давлении происходит при температуре 560 оС. Однако с заметной скоростью данная реакция протекает при температурах выше 1000 оС. Основные продукты такого процесса – этан С 2 Н 6, ацетилен С 2 Н 2, этилен С 2 Н 4, углерод и водород. Первичная реакция описывается уравнением:
 2СН4 С2Н6 + Н2. (8.22)
2СН4 С2Н6 + Н2. (8.22)
Реакция развивается по схеме:



 СН3 + СН4 С2Н6 + Н; (8.23)
СН3 + СН4 С2Н6 + Н; (8.23)



 Н + СН4 Н2 + СН3. (8.24)
Н + СН4 Н2 + СН3. (8.24)
Деструкция этана начинается уже при температуре 500 оС, пропана – при 450 оСпо двум направлениям:

 СН3СН = СН2;
СН3СН = СН2;
 СН3СН2СН3 (8.25)
СН3СН2СН3 (8.25)
 СН2 = СН2 + СН4.
СН2 = СН2 + СН4.
Начиная с бутана, распад алканов по связи С – С становится преобладающим. Относительная скорость крекинга стремительно возрастает с ростом числа атомов углерода. Соотношение между числом атомов водорода в молекуле алкана и скоростью крекинга описывается следующей зависимостью:
Скорость реакции, относит. ед. 1 4 9 10 32 46 120
Число атомов углерода в молекуле 5 6 7 8 10 12 20
Термокрекинг н-бутана происходит следующим образом. За счет разрыва связи С – С в середине молекулы образуются первичные радикалы (инициирование реакции):


 2СН3СН2;
2СН3СН2;
 Н3СН2СН2СН3
Н3СН2СН2СН3 
 (8.26)
(8.26)
 СН3 + СН2СН2СН3.
СН3 + СН2СН2СН3.
Затем процесс развивается по двум возможным направлениям. По первому – радикалы С 3 и выше самопроизвольно распадаются по 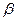 -правилу с образованием более устойчивых метильных и этильных радикалов или атомов водорода и соответствующих алкенов:
-правилу с образованием более устойчивых метильных и этильных радикалов или атомов водорода и соответствующих алкенов:







 СН2СН = СН2 + Н;
СН2СН = СН2 + Н;

 СН3СН2СН2
СН3СН2СН2  (8.27)
(8.27)



 СН2 = СН2 + СН3.
СН2 = СН2 + СН3.
 |
По второму направлению устойчивые по отношению к распаду, но очень реакционноспособные радикалы СН3 . и С2Н5 . и атомы водорода вступают в реакции с исходными молекулами, отрывая от них атом водорода:







 Н(СН3; С2Н5) + С4Н10 Н2(СН4; С2Н6) + С4Н9. (8.28)
Н(СН3; С2Н5) + С4Н10 Н2(СН4; С2Н6) + С4Н9. (8.28)
 Бутильные радикалы далее распадаются по
Бутильные радикалы далее распадаются по 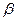 -правилу:
-правилу:



 СН3СН2 – СН2СН2 СН3СН2 + СН2 = СН2. (8.29)
СН3СН2 – СН2СН2 СН3СН2 + СН2 = СН2. (8.29)
Образующиеся мелкие радикалы вновь реагируют с исходными веществами. Так развивается цепной процесс.
Основная часть продуктов цепной реакции образуется на стадии развития цепи и суммарный процесс крекинга н-бутана можно описать следующей схемой:

 СН4 + СН2 = СНСН3;
СН4 + СН2 = СНСН3;
 н-С4Н10 (8.30)
н-С4Н10 (8.30)
 СН3СН3 + СН2 = СН2.
СН3СН3 + СН2 = СН2.
Термическое разложение алканов С 3 – С 5 с увеличением глубины процесса самотормозится вследствие накопления пропилена, который реагирует с активными радикалами, ведущими цепную реакцию с образованием менее активного алкильного радикала:





 СН2 = СНСН3 + СН3 СН2 = СН – СН2 + СН4. (8.31)
СН2 = СНСН3 + СН3 СН2 = СН – СН2 + СН4. (8.31)
 |
Термический распад алканов С 6 и выше с увеличением глубины процесса, наоборот, ускоряется вследствие образования алкенов, содержащих ослабленную С – С связь, находящуюся в 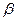 -положении по отношению к кратной связи.
-положении по отношению к кратной связи.
8.3.2. Превращения циклоалканов. Термодинамически более выгодным является распад циклоалканов до элементов и дегидрирование циклопентанов до циклопентадиенов, а циклогексанов до аренов. Однако скорость таких реакций, требующих разрыва С – Н связей, на несколько порядков ниже, чем скорость крекинга по С – С связи. Поэтому главными продуктами крекинга цикланов являются низшие алканы, алкены, диены и водород.





 3СН2 = СН2
3СН2 = СН2

 СН2 = СН – (СН2)3СН3 (8.32)
СН2 = СН – (СН2)3СН3 (8.32)
СН2 = СН2 + СН2 = СНСН2СН3
СН3 – СН3 + СН2 = СН – СН = СН2.
При этом первичный распад молекулы приводит к образованию бирадикала:


 СН2 – (СН2)4 – СН2. (8.33)
СН2 – (СН2)4 – СН2. (8.33)
Далее бирадикал распадается на стабильные молекулы:
 |



 3СН2 = СН2
3СН2 = СН2




 СН2 – (СН2)4 – СН2 (8.34)
СН2 – (СН2)4 – СН2 (8.34)

 СН2 =СН(СН2)3СН3
СН2 =СН(СН2)3СН3
 |
Реакция протекает по цепному механизму. Скорость этой реакции мала ввиду высоких энергозатрат на стадии инициирования и отсутствия низкоэнергетических реакций продолжения цепи.
Накопление алкенов, содержащих сопряженную с двойной ослабленную связь С – С, инициируетрадикально-цепной механизм дальнейшего течения процесса:



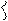 СН2 =СН – СН2 – СН2 – СН2 – СН3 СН2=СНСН2 + СН2СН2СН3; (8.35)
СН2 =СН – СН2 – СН2 – СН2 – СН3 СН2=СНСН2 + СН2СН2СН3; (8.35)







 Н + СН2СН2СН3 (R; Н)
Н + СН2СН2СН3 (R; Н)  + СН3СН2СН3 (RН; Н2). (8.36)
+ СН3СН2СН3 (RН; Н2). (8.36)
и далее:



 СН2 = СН(СН2)3СН2
СН2 = СН(СН2)3СН2
 | 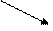 |





 СН2 = СН2 + СН2 = СНСН2СН2 СН2 = СНСН(СН2)2СН3 (8.37)
СН2 = СН2 + СН2 = СНСН2СН2 СН2 = СНСН(СН2)2СН3 (8.37)




 или
или 

Н + Н. (8.38)
 |




Стабилизация радикалов СН2 = СНСН2СН2 и СН 2 СН 3 (R) идет путем отрыва атома Н от исходной молекулы (реакция (8.36). При этом они превращаются в 1-бутен и этан. Кроме того, радикал С 2 Н5  может стабилизироваться, отщепляя атом водорода и образуя при этом этилен. Атом водорода также атакует исходную молекулу циклана, образуя молекулу водорода по реакции (8.36). Циклогексил-радикал превращается по реакции (8.37). Чередование этих реакций – цепной процесс. Распад радикала С 6 Н 11
может стабилизироваться, отщепляя атом водорода и образуя при этом этилен. Атом водорода также атакует исходную молекулу циклана, образуя молекулу водорода по реакции (8.36). Циклогексил-радикал превращается по реакции (8.37). Чередование этих реакций – цепной процесс. Распад радикала С 6 Н 11  по
по 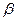 -связи С – Н приводит к дегидрированию (реакция (8.38).
-связи С – Н приводит к дегидрированию (реакция (8.38).
Алкилциклоалканы распадаются по радикально-цепному механизму. Зарождение цепи в этом случае происходит из-за разрыва связи С – С в боковой цепи или отрыва радикала СН 3  в метилпроизводных цикланов. Бициклические цикланы подвергаются дециклизации, крекингу и дегидрированию.
в метилпроизводных цикланов. Бициклические цикланы подвергаются дециклизации, крекингу и дегидрированию.
8.3.3. Превращения алкенов. Алкены почти отсутствуют в исходной нефти и образуются при деструкции алканов и циклоалканов. Термические превращения алкенов определяют конечный состав продуктов процесса.
При температурах 450– 500 оС термодинамически возможны реакции распада длинноцепочечных алкенов до низших алкенов, алкадиенов и алкинов, и реакции образования аренов. При более высоких температурах возможно образование и ацетилена.
Низшие алкены (этилен и пропилен) превращаются следующим образом.
1. Дегидрирование
700-800 оС
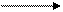 СН3СН = СН2 СН2 = СН = СН2 + Н2; (8.39)
СН3СН = СН2 СН2 = СН = СН2 + Н2; (8.39)
пропадиен (аллен)
1000 оC
 СН2 = СН2 CН
СН2 = СН2 CН 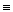 СН + Н2. (8.40)
СН + Н2. (8.40)
ацетилен
Механизм этих реакций – радикально-цепной. Инициирование реакции пиролиза этилена происходит при разрыве связи С – Н, и поэтому требуется высокая температура.


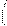

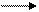 СН2 = С Н СН2 = СН + Н. (8.41)
СН2 = С Н СН2 = СН + Н. (8.41)

Н
Пропилен распадается по более слабой 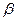 -связи:
-связи:


 СН2 = СНС – Н СН2 = СНСН2 + Н. (8.42)
СН2 = СНС – Н СН2 = СНСН2 + Н. (8.42)
 |
Н
Кроме того, образовавшийся аллильный радикал стабилизирован за счет сопряжения неспаренных электронов с 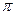 - электронами двойной связи. Поэтому распад пропилена происходит в более мягких условиях.
- электронами двойной связи. Поэтому распад пропилена происходит в более мягких условиях.
Звено цепи состоит из двух реакций:


 СН2 = СН СН
СН2 = СН СН 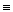 СН + Н; (8.43)
СН + Н; (8.43)



 СН2 = СН2 + Н СН2 = СН + Н2 (8.44)
СН2 = СН2 + Н СН2 = СН + Н2 (8.44)
и




 СН2 = СН – СН2 СН2 = С = СН2 + Н; (8.45)
СН2 = СН – СН2 СН2 = С = СН2 + Н; (8.45)
 |





 СН2 = СН – СН3 + Н СН2 = СН – СН2 + Н2. (8.46)
СН2 = СН – СН3 + Н СН2 = СН – СН2 + Н2. (8.46)
 |
2. Полимеризация. Реакция термодинамически возможна при атмосферном давлении при температуре до 500 оС, а при повышенном давлении – при более высоких температурах.
 2СН2 = СН2 СН2 = СНСН2СН3. (8.47)
2СН2 = СН2 СН2 = СНСН2СН3. (8.47)
Процесс идет по двум возможным механизмам:
а) через бирадикал
< 500 оC CH2=CH2









 СН2 = СН2
СН2 = СН2  СН2 СН2
СН2 СН2 
 CH2(CH2)2CH2
CH2(CH2)2CH2  СН2 = СНСН2СН3 (8.48)
СН2 = СНСН2СН3 (8.48)
 |
б) по радикально-цепному варианту:



 СН2 = СН2 СН2 = СН2
СН2 = СН2 СН2 = СН2

 СН2 =СН
СН2 =СН  СН2 = СНСН2СН2
СН2 = СНСН2СН2  СН2 =СН
СН2 =СН  + CН2 = СНСН2СН3.(8.49)
+ CН2 = СНСН2СН3.(8.49)

 > 500 оC
> 500 оC
3. Дегидроконденсация:
700 оС
 2СН2 = СН2 СН2 = СН – СН = СН2 + Н2. (8.50)
2СН2 = СН2 СН2 = СН – СН = СН2 + Н2. (8.50)
Механизм этой реакции – радикально-цепной:







 СН2=СН + СН2=СН2 СН2=СНСН2 – СН2 Н + СН2=СН – СН=СН2; (8.51)
СН2=СН + СН2=СН2 СН2=СНСН2 – СН2 Н + СН2=СН – СН=СН2; (8.51)
 |






 СН2=СН2 + Н СН2 = СН + Н2 . (8.52)
СН2=СН2 + Н СН2 = СН + Н2 . (8.52)
Соотношение этих трех типов реакций зависит от температуры и давления в системе. При низких температурах и высоком давлении идет полимеризация низших олефинов, и наоборот, при высокой температуре и низком давлении образуется ацетилен. В промежуточных условиях преобладает процесс дегидроконденсации.
Алкены С 4 и С 5 кроме указанных реакций подвергаются крекингу по 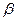 -связям (С – С и/или С – Н):
-связям (С – С и/или С – Н):

 Н2С= СН – СН = СН2 + Н2;
Н2С= СН – СН = СН2 + Н2;
 Н2С = СН – СН – СН3 (8.53)
Н2С = СН – СН – СН3 (8.53)
 Н2С= СН = СН2 + СН4.
Н2С= СН = СН2 + СН4.
Механизм этих реакций – радикально-цепной.
Высшие алкены при 400–450 оС в реакциях полимеризации, дегидрирования и дегидроконденсации практически не участвуют, а в основном распадаются по 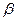 -связям С – С:
-связям С – С:


 СН2 = СН – СН = СН2 + С3Н8;
СН2 = СН – СН = СН2 + С3Н8;

 СН2 = СН(СН2)4СН3 (8.54) СН2 = СН – СН3 + СН2 = СНСН2СН3
СН2 = СН(СН2)4СН3 (8.54) СН2 = СН – СН3 + СН2 = СНСН2СН3
Первичный распад молекул идет по 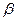 -связи С – С:
-связи С – С:


 СН2 = СН – СН2 – СН2(СН2)2СН3 СН2 = СНСН2 + СН2(СН)2СН3; (8.55)
СН2 = СН – СН2 – СН2(СН2)2СН3 СН2 = СНСН2 + СН2(СН)2СН3; (8.55)


 СН2(СН)2СН3 + СН2 =СН(СН2)4СН3 СН2 =СН–СН(СН2)3СН3 + С4Н10 (8.56)
СН2(СН)2СН3 + СН2 =СН(СН2)4СН3 СН2 =СН–СН(СН2)3СН3 + С4Н10 (8.56)






 СН2=СН–СН–СН2–СН2–СН2–СН3 СН2=СН–СН=СН2 + СН2-СН2СН3; (8.57)
СН2=СН–СН–СН2–СН2–СН2–СН3 СН2=СН–СН=СН2 + СН2-СН2СН3; (8.57)
 |






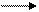 СН2СН2СН3 + СН2 = СН(СН2)4СН3 СН2 =СН–СН(СН2)3СН3 + С3Н6. (8.58)
СН2СН2СН3 + СН2 = СН(СН2)4СН3 СН2 =СН–СН(СН2)3СН3 + С3Н6. (8.58)

Отличия в энергиях 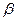 -,
-, 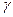 - и т. д. (кроме
- и т. д. (кроме 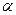 -) С – Н связей значительно меньше, чем в соответствующих С – С связях. Поэтому передача цепи может идти путем отрыва не только аллильного, но и любого вторичного атома водорода, вероятность которого возрастает с увеличением длины цепи алкена (статистический фактор).
-) С – Н связей значительно меньше, чем в соответствующих С – С связях. Поэтому передача цепи может идти путем отрыва не только аллильного, но и любого вторичного атома водорода, вероятность которого возрастает с увеличением длины цепи алкена (статистический фактор).
Состав продуктов крекинга алкенов зависит также от возможной изомеризации радикалов. При этом цепной механизм крекинга высших алкенов протекает независимо от наличия двойной связи.
Циклоалкены более устойчивы, чем алициклические алкены. Циклогексен устойчив до 600 оС. При более высоких температурах он распадается по нецепному механизму через бирадикал или цепным путем дегидрируется вплоть до бензола.
8.3.4. Превращения алкадиенов и алкинов. При невысоких температурах (< 400 0С) и давлениях, близких к атмосферному и выше, наиболее реакционноспособными являются алкадиены. Они вступают в реакции диенового синтеза по молекулярному механизму.
 НС = CН2 СН2
НС = CН2 СН2



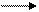 +; (8.59)
+; (8.59)
 НС = СН2 СН2
НС = СН2 СН2
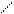
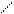
 СН2 СН = СН2
СН2 СН = СН2

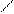
 НС СН СН = СН2
НС СН СН = СН2





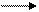 +. (8.60) НС СН2
+. (8.60) НС СН2
СН2
При температурах выше 700 оС и атмосферном давлении диеновый синтез незначителен и основное значение переходит к радикально-цепным реакциям.


 2СН
2СН 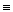 СН СН
СН СН 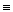 С + СН = СН2; (8.61)
С + СН = СН2; (8.61)


 СН
СН 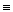 С + СН
С + СН 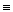 СН СН
СН СН 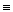 С – СН=СН. (8.62)
С – СН=СН. (8.62)





 СН
СН 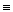 С – С
С – С 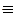 СН + Н
СН + Н
 |





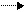


 СН
СН 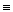 С – СН=СН + СН
С – СН=СН + СН 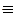 СН СН
СН СН 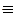 ССН=СН2 + СН
ССН=СН2 + СН 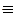 С
С



 СН
СН 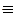 С – СН=СН – СН = СН
С – СН=СН – СН = СН






 Н
Н 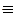 СН
СН 


 + СН
+ СН 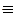 С. (8.63)
С. (8.63)

В результате последних реакций образуются сильноненасыщенные соединения с большей молекулярной массой, чем исходные вещества, и арены. При конденсации аренов, алкенов и алкинов получают замещенные и поликонденсированные арены:
 |


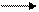






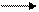 2СН
2СН 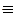 СН + СН = СН – СН = СН2 + Н2. (8.64)
СН + СН = СН – СН = СН2 + Н2. (8.64)
Процессы дегидроконденсации, диеновый синтез и циклизация сильноненасыщенных соединений, в конце концов, приводят к ароматизации продуктов термических превращений углеводородов.
8.3.5. Превращения аренов. Незамещенные и метилзамещенные арены более устойчивы, чем алканы. Термодинамически возможен распад аренов до элементов, а при высоких температурах и раскрытие цикла. Однако, исключая электрокрекинг при очень высоких температурах, незамещенные арены подвергаются дегидроконденсации. Алкилзамещенные арены, имеющие С – С связь, сопряженную с ароматическим кольцом, разлагаются быстрее алканов:


 T
T




 2 + Н2. (8.65)
2 + Н2. (8.65)
дифенил
Механизм этого процесса – радикально-цепной:
 С6Н6 С6Н5
С6Н6 С6Н5  + Н
+ Н  ; (8.66)
; (8.66)

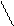











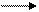










 + + Н; (8.67)
+ + Н; (8.67)





 Н + С6Н6 С6Н5 + Н2 . (8.68)
Н + С6Н6 С6Н5 + Н2 . (8.68)
 |
Аналогично протекает дегидроконденсация нафталина:
























 2. (8.69) – Н2 – Н2
2. (8.69) – Н2 – Н2
Дегидроконденсация аренов, диеновый синтез и дегидроконденсация алкенов лежат в основе коксообразования при термических процессах.
Толуол, также как и бензол, подвергается дегидроконденсации:

 С6Н5(СН2)2С6Н5 – дифенилэтан;
С6Н5(СН2)2С6Н5 – дифенилэтан;

 2С6Н5СН3 (8.70)
2С6Н5СН3 (8.70)
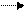 – Н2 С6Н5 – СН2 – С6Н4 – СН3 – фенилтоллилметан.
– Н2 С6Н5 – СН2 – С6Н4 – СН3 – фенилтоллилметан.
За счет водорода, выделившегося при дегидроконденсации, частично происходит деметилирование:
 С6Н5СН3 + Н2 С6Н6 + СН4. (8.71)
С6Н5СН3 + Н2 С6Н6 + СН4. (8.71)
В начальный период превращение толуола идет с небольшой скоростью, так как радикальная реакция протекает по нецепному механизму:


 С6Н5СН3 С6Н5СН2 + Н; (8.72)
С6Н5СН3 С6Н5СН2 + Н; (8.72)






 Н2 + С6Н5СН2
Н2 + С6Н5СН2


 Н + СН3 (8.73)
Н + СН3 (8.73)













 Н
Н  + СН3
+ СН3
СН3








 СН3 + СН3 СН4 + С6Н5СН2 (8.74)
СН3 + СН3 СН4 + С6Н5СН2 (8.74)
 |
Бензильный радикал малоактивен и вступает в реакции рекомбинации с образованием дибензила, вследствие чего цепь обрывается.
С увеличением глубины процесса в системе повышается концентрация дибензила. За счет распада алифатической связи С – С в дибензиле и развития цепного механизма скорость превращения толуола возрастает:

















 СН2
СН2  СН3 С6Н5СН3С6Н4СН3 + Н;
СН3 С6Н5СН3С6Н4СН3 + Н;




 С6Н5СН3 + С6Н5СН2
С6Н5СН3 + С6Н5СН2 













 СН2
СН2  С6Н5СН2С6Н5 + СН3; (8.75)
С6Н5СН2С6Н5 + СН3; (8.75)



СН3







 С6Н5СН2
С6Н5СН2


 СН3 (Н) + С6Н5СН3 СН4(Н2) + С6Н5СН2 С6Н5(СН2)2С6Н5 . (8.76)
СН3 (Н) + С6Н5СН3 СН4(Н2) + С6Н5СН2 С6Н5(СН2)2С6Н5 . (8.76)

Алкилпроизводные аренов с длинными заместителями распадаются с разрушением алкильных цепей:
 С6Н5 (СН2)3СН3 С6Н5 – СН = СН2 + С2Н6, (8.77)
С6Н5 (СН2)3СН3 С6Н5 – СН = СН2 + С2Н6, (8.77)
стирол
при этом разрушается ослабленная 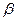 -связь С – С:
-связь С – С:


 С6Н5 – СН2 – СН2 – СН2 – СН3 С6Н5СН2 + СН2СН2СН3 (8.78)
С6Н5 – СН2 – СН2 – СН2 – СН3 С6Н5СН2 + СН2СН2СН3 (8.78)
и далее:






 С6Н5 (СН2)3СН3 + С6Н5СН2 С6Н5СН(СН2)2СН3 + С6Н5СН3. (8.79)
С6Н5 (СН2)3СН3 + С6Н5СН2 С6Н5СН(СН2)2СН3 + С6Н5СН3. (8.79)
При распаде радикалов по 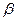 -связи С – Н выделяется водород. Присоединение водорода к арену ведет к реакции гидродеалкилирования алкиларена:
-связи С – Н выделяется водород. Присоединение водорода к арену ведет к реакции гидродеалкилирования алкиларена:







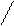

 H
H 



