
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
II.2. Параллельные реакции
|
|
Параллельные реакции – реакции, в которых исходные вещества одновременно превращаются по нескольким направлениям с образованием различных продуктов. Например: при нитровании, сульфировании, галоидировании ароматических органических соединениймогут получаться орто-, мета- и паразамещенные; при крекинге нефти – газообразные углеводороды, при взаимодействии СО и Н2 – углеводороды, спирты, альдегиды и т.д. Схема параллельной реакции первого порядка:
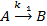 и
и 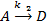
Для скоростей такой реакции можно записать (с учетом принципа независимости):
υ 1=k1CA, и υ 2= k2CA.
Тогда:
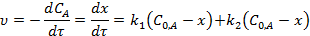
или

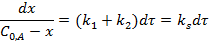
Интегральные формы кинетического уравнения реакции 1-го порядка:
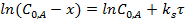

Текущая концентрация исходного вещества:
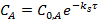
Общая концентрация продуктов реакции:
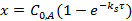
Для скорости образования продуктов реакции, с учетом их отсутствия в начальный момент, можно записать:
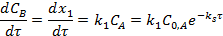
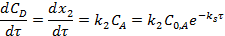
После дифференцирования:
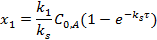

Отношение концентраций продуктов постоянно, не зависит от времени и определяется отношением констант скоростей реакций:
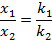
Зная константу ks и концентрации продуктов реакции в момент времени τ можно найти константы скоростей для каждой реакции. Зависимости концентраций веществ от времени для параллельной реакции первого порядка представлены на рисунке 6.
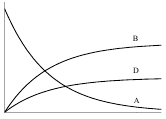
Рис. 6. Зависимость концентраций веществ А, В, D от времени для параллельной реакции первого порядка (k1˃ k2).