
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Химическая связь
|
|
Различают 3 основных типа химической связей: ковалентную, ионную и металлическую.
Механизм возникновения ковалентной связи:
Н + Н = Н2; DH = -436 кДж/моль.
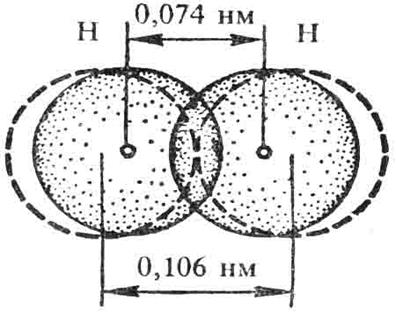
Рис.2. Схема перекрывания электронных орбиталей при образовании молекулы водорода
Наибольшее перекрывание электронных облаков осуществляется вдоль линии, соединяющей ядра двух атомов.
Химическая связь тем прочнее, чем больше перекрывание электронных орбиталей (рис.2.)
Изображение химической связи:
1) Н + Н ® Н: Н




2) 1s1 1s1
 |  |


 1s2
1s2








 или
или
3) H — H
.. ......
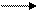

 Пример:: Cl ∙ + ∙ Cl:: Cl: Cl:
Пример:: Cl ∙ + ∙ Cl:: Cl: Cl:
 ........
........
неподеленная неспаренный общая
пара электронов электрон поделенная пара электронов
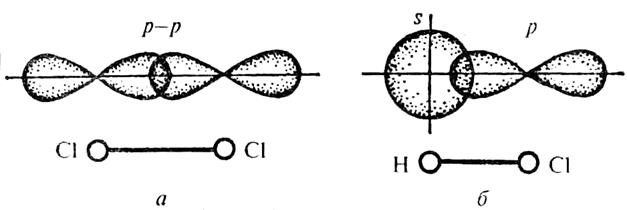
Рис.3. Схема образования химической связи в молекулах хлора Cl2 (a) и хлороводорода HCl (б)
Химическая связь, осуществляемая электронными парами, называется ковалентной. Различают неполярную ковалентную связь и полярную ковалентную связь (рис.3.)
Неполярная связь: H2, Cl2, O2, N2: H: H
..
Полярная связь: HCl, H2O, H2S: Hd+ : Cld-: (ЭОCl = 2, 83; ЭОН = 2, 1)
..
Ковалентная связь образуется за счет: а) перекрывания электронных облаков; б) по донорно-акцепторному механизму.
 +
+





 ....
....
 H: N: + H+ ® H: N: H (NH3 + H+ ® NH+4)
H: N: + H+ ® H: N: H (NH3 + H+ ® NH+4)




 ....
....
донор акцептор
Механизм образования ковалентной связи за счет двухэлектронного облака одного атома (донора) и свободной орбитали другого атома (акцептора) называется донорно-акцепторным.