
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Не-Q- та Q-інфаркт інфаркт міокарда.
|
|
Між першим класичним описанням клініки стенокардії У.Геберденом (1972) і першим випадком прижиттєвої діагностики коронаротромбозу В.П.Образцовим і М.Д.Стражеско (1910) минуло понад 100 років. Власне В.П.Образцов і М.Д.Стражеско вперше зауважили, що диференційно-діагностичною ознакою між коронарним тромбозом і стенокардією є наявність ангінозного статуса, який відсутній при ізольованих приступах стенокардії. В 1912 році американський дослідник Джеймс Херрік опублікував незалежне описання клініки гострого коронарного тромбоза, а у 1918 році – ЕКГ-описання експериментальної коронарної оклюзії і тривалий час на Заході саме він несправедливо вважався піонером в цій області. У 1920 році Гарольд Парді в Нью-Йорку вперше опублікував спостереження значного підйому сегмента ST у хворого з клінічними ознаками гострого інфаркта міокарда. Проте, не дивлячись на успіхи в клінічній і ЕКГ-діагностиці, підходи до лікування інфаркта міокарда тривалий час залишались крайнє консервативними. Від ідеї про необхідність повного і тривалого спокою таким хворим (П.Уайт, Р.Брайтон, С.Левін, Б.Лаун), через впровадження методик селективної коронароангіографії (М.Соунг), зовнішнього масажу серця і трансторакальної дефібриляції (В.Неговський, У.Коувенховен, П.Золле) і організацію палат інтенсивної терапії із застосуванням нітратів, бета-адреноблокаторів і периферійних вазодилататорів до моменту першого застосування Є.І.Чазовим (1976) методик реперфузійної терапії минуло понад 40 років. Летальність внаслідок гострого інфаркта міокарда за цей час вдалося знизити з 30-40% до 12-15%, а в багатьох клініках до 5-10%.
Визначення і термінологія. Гострий інфаркт міокарда (ГІМ) – одна з найбільш грізних форм ІХС. Інфаркт міокарда – це ішемічний некроз ділянки м’яза серця, який виникає внаслідок гострої невідповідності між потребою міокарда в кисні і доставкою його по коронарних судинах. Інфаркт міокарда – більш вузьке поняття, ніж некроз міокарда. Останній включає в себе як власне інфаркт міокарда (коронарний, ішемічний), так і так звані некоронарогенні некрози міокарда, які можуть спостерігатись при вторинній коронарній недостатності (дисметаболічні, стероїдні, адреналінові некрози тощо). При трансмуральному інфаркті міокарда розвивається некроз основної маси ішемізованого міокарда. При нетрансмуральному (великовогнищевому, субендокардіальному) інфаркті міокарда більша частина ішемізованого інфаркта міокарда не є некротизованою.
Хоча трансмуральний і нетрансмуральний інфаркти міокарда мають відповідні ЕКГ-критерії, останнім часом ці поняття застосовуються переважно як патологоанатомічні, оскільки часто спостерігається розбіжність з даними ЕКГ. Тому в клініці тепер рекомендують застосовувати терміни “інфаркт міокарда із зубцем Q” та “інфаркт міокарда без зубця Q”. Картина ЕКГ не дозволяє точно встановити глибину і поширеність пошкодження серцевого м’яза. Інфаркт може бути нетрансмуральним за наявності зубця Q і, навпаки, при трансмуральному інфаркті міокарда зубців Q, QS може не бути.
Виникнення нового інфаркта міокарда в межах 60 діб від початку захворювання називають “рецидивуючим інфарктом міокарда”, а через два місяці і більше – “повторним інфарктом міокарда”. Через два місяці після інфаркта міокарда встановлюють діагноз “стенокардія навантаження” (з вказанням функціонального класу за Канадською класифікацією з врахуванням тесту з дозованим фізичним навантаженням) та “постінфарктного кардіосклерозу”. Через чотири місяці після інфаркта міокарда хворий направляється на МСЕК, де вирішується питання подальшої тактики – “приступити до праці”, “визнати непрацездатним (інвалідність ІІІ-ІІ групи)” або “продовжити непрацездатність”.
Етіологія і патогенез. Адекватність коронарного кровоплину метаболічним запитам міокарда визначається трьома основними факторами: величиною коронарного кровоплину, складом артеріальної крові (насамперед ступенем її оксигенації) і потребою міокарда в кисні. Величина коронарного кровоплину зумовлюється рівнем кров’яного тиску в аорті і опором коронарних судин. Потреба міокарда в кисні може зростати при підвищенні артеріального тиску, фізичному або психоемоційному навантаженні. Ймовірність розвитку гострого інфаркта міокарда (ГІМ) є найбільшою у ранкові години, що пов’язують із циркадними (добовими) змінами тонусу коронарних судин, концентрації катехоламінів і здатності крові до коагуляції.
Найбільш частою причиною розвитку ГІМ є розрив атеросклеротичної бляшки з тромбозом коронарних судин та з помірно чи більш вираженим стенозуванням їх (див. патогенез нестабільної стенокардії). Власне тромбування всього просвіту коронарної артерії на фоні недостатнього колатерального кровопостачання й призводить до “Q-інфаркта міокарда”.
 |
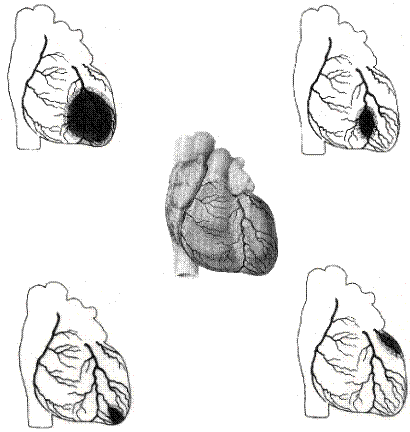 |
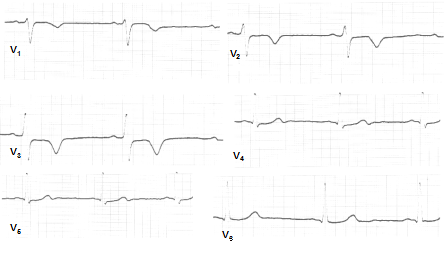
Рис. Не-Q-інфаркт міокарда.
Рис. Дестабілізація (тромбоз) коронарного кровоплину в різних басейнах
лівої коронарної артерії.
 |  |  | |||
 |  | ||
Рис. Дестабілізація (тромбоз) коронарного кровоплину в різних басейнах правої та лівої коронарної артерії.
У патогенезі інфаркта міокарда важливу роль відіграє арахідонова кислота, яка входить до складу ліпідів людини. Встановлено, що в процесі її обміну утворюються сполуки, які можуть сильно впливати на кровообіг, зокрема на тромбоцити та судинну стінку. Тромбоксан А2 – сполука, яка утворюється в тромбоцитах підчас їх адгезії і агрегації у відповідь на дію психоемоційного чи фізичного стреса та гіперкатехоламінемії. Тромбоксан А2 володіє двома важливими властивостями: він дуже сильно посилює агрегацію тромбоцитів та інтенсивно звужує судини. В процесі метаболізму арахідонової кислоти утворюються також простациклін-сполука з властивостями, протилежними до тих, які має тромбоксан А2. Простациклін утворюється здоровими ендотеліальними клітинами артеріальних судин. Його дія протилежна тромбоксану А2. Він протидіє адгезії та агрегації тромбоцитів і розширяє кровоносні судини. Рівновага між утворенням тромбоксану А2 (ТХА2) і простацикліну (РgІ2) має вирішальне значення для підтримання нормального кровотоку у коронарних артеріях. Істотну роль у порушенні згаданої вище рівноваги відіграють циклічні перекиси високоненасичених жирних кислот. Це сильні інгібітори утворення простацикліну в стінках артеріальних судин. Підвищення концентрації перекисів у плазмі й тканинах викликає зсув рівноваги в напрямку ТХА2, чим й запускається каскад реакцій, внаслідок яких тромбоцити агрегують на інтимі артерій, звільняючи при цьому гідролази, які руйнують стінку артерії. Якщо цьому не протидіє РgI2, процес йде в напрямку утворення спочатку пристінкового, а в подальшому оклюзійного тромбу. Отже, основним механізмом розвитку ГІМ сьогодні визнається тромбоз коронарних артерій за умов недостатнього захисного впливу коронарних колатералей. Виражена мережа колатералей може загальмувати темпи інфарктування та обмежити розміри некрозу, впливаючи таким чином на виживання хворих. Колатералі краще розвинуті по нижній стінці лівого шлуночка (тому передні інфаркти є більш обширні і частіше закінчуються смертю). У пацієнтів з тривалим анамнезом коронарної хвороби розміри інфаркта міокарда менші, ніж у хворих молодшого віку без “коронарного” анамнезу. Реперфузія інфаркт-залежної коронарної артерії (спонтанна або з допомогою тромболітичної терапії) у перші 6 годин поліпшує внутрішньосерцеву гемодинаміку та обмежує розміри інфаркта міокарда. Після відновлення кровоплину в інфаркт-залежній коронарній артерії систолічна функція серця відновлюється не одразу. Цей процес називається “оглушенням міокарда” (stunning myocardium-syndrome), він триває від декількох хвилин до декількох днів і залежить від тривалості ішемії до моменту реперфузії. Його слід відрізняти від феномена гібернації міокарда, який виникає при хронічному зниженні кровоплину до міокарда (виражений коронаросклероз). Він характеризується дисфункцією (порушенням сегментарної скоротливості) певної ділянки міокарда.
Підчас інфаркта міокарда стимулюються захисні реакції організму, зокрема, відбувається інфільтрація некротизованої тканини нейтрофілами і моноцитами (в рамках запальної реакції). Некротизований міокард поступово заміщується сполучною тканиною. Цей процес закінчується формуванням шраму (рубця) на 4-6 тижнях від початку ГІМ.