
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Квантовые числа
|
|
квантовая теория создана Планком
Энергетическое состояние каждого электрона характеризуется набором квантовых чисел
радиальное (главное) (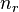 ), орбитальное (
), орбитальное ( ), магнитное (
), магнитное ( ) и спиновое квантовые числа
) и спиновое квантовые числа
Главное квантовое число n – (от 1 до 7 для атомов в основном состоянии) определяет энергетическое состояние атома. Соответствует уровням K, L, M...Q. Кажому значению n соответствует ряд комбинаций др квантовых чисел
Орбитальное квантовое число l (это буква) – (на 1 (а это цифра) меньше главного числа, те от 0 до n-1) определенное квантование момента импульса – тип подуровня. Бывает s, p, d, f
Магнитное квантовое число ml – (любое целое число, удовлетворяющее неравенство –l < ml < +l) проекция момента импульса на любое выделенное в пространстве направление
Спин ms – квантовый угловой момент электрона. Вращение вокруг своей оси. Бывает целый и полуцелый.
Число компонент волновой функции, описывающей элементарную частицу в квантовой механике, растёт с ростом спина элементарной частицы. Элементарные частицы со спином 0 описываются однокомпонентной волновой функцией (скаляр)
со спином 1\2 описываются двухкомпонентной волновой функцией (спинор)
со спином 1 1\2 описываются четырёхкомпонентной волновой функцией (вектор)
со спином 2 описываются шестикомпонентной волновой функцией (тензор).
Максимальное число электронов в подуровне определяется принципом Паули (два электрона не могут иметь все 4 одинаковых квантовых числа), следовательно максимальное число е в подуровне 2(2l+1) и в уровне 2n^2
Следовательно для s, p, d, f максимальные числа – 2, 6, 10, 14
Каждый атом имеет специфический суммарный угловой момент
J = S + L
S – вектор суммы всех угловых моментов всех оболочек
L – суммарный вектор всех условных моментов всех оболочек