
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
ББК 28.072 я 73
|
|
Доркина Е.Г., Парфентьева Е.П., Скульте И.В, Саджая Л.А., Сергеева Е.О., Терехов А.Ю.
Домашние задания
По биологической
Химии
для студентов 3-го курса очного отделения
V семестр
Студент ________________________________
___________курс, __________________ группа
Преподаватель __________________________
Пятигорск, 2011
УДК 577.1 (076.1)
ББК 28.072 я 73
Д 66
Рецензент: канд. биол. наук, доц. Назарова Л.Е.
Д 66 Доркина Е.Г., Парфентьева Е.П., Скульте И.В, Саджая Л.А., Сергеева Е.О., Терехов А.Ю.
Д 66 Домашние задания по биологической химии для студентов 3-го курса очного отделения / Е.Г. Доркина [и др.]. – Пятигорск: Пятигорская ГФА, 2011. - 65 с.
Домашние задания по биологической химии составлены в соответствии с Программой по биохимии для студентов 3-го курса очной формы обучения, представлены в виде упражнений, задач, схем, таблиц, рисунков и предназначены для самостоятельной творческой внеаудиторной работы студентов с целью лучшего усвоения и закрепления знаний.
УДК 577.1 (076.1)
ББК 28.072 я 73
 Допущено к внутривузовскому изданию
Допущено к внутривузовскому изданию
Председатель ЭМС
Проф. __________ В.В. Гацан
Протокол № 256 от 7 июля 2011 г.
© Пятигорская государственная фармацевтическая академия, 2011 г.
Занятие №2. Тема: «Физико-химические свойства и строение белков. Качественные реакции на функциональные группы белков и аминокислот»
1. Дайте определение белкам и укажите их элементный состав, заполнив таблицу:
| Элементный химический состав белка | Содержание в процентах |
| Углерод | |
| Кислород | |
| Азот | |
| Водород | |
| Сера |
2. Назовите высокомолекулярное соединение, имеющее следующий состав элементов: С(51-55%); О(21-23%); N (15-18%); Н (6-7%); S (0, 3-2, 5%).
3. Дайте характеристику методам определения молекулярной массы белков:
| Название метода | Характеристика |
| Аналитические методы | |
| Электронная микроскопия | |
| Измерение осмотического давления белка | |
| Диффузный метод | |
| Измерение скорости седиментации |
4. Запишите неионизированную форму белковой молекулы:
5.

Дайте определение амфиону (цвиттериону).
6. Каких зарядов («+» или «-») больше на молекуле кислого белка? Напишите схему изменения заряда кислого белка в зависимости от изменения рН раствора.
7. Выберите серусодержащие аминокислоты и напишите их формулы. Укажите классы, к которым они относятся:
- треонин
- тирозин
- цистеин
- триптофан
- метионин.
8. В приведённом списке аминокислот выберите аминокислоту, не обладающую оптической активностью. Напишите её структурную формулу. Укажите класс, к которому она относится.
-лейцин
-цистеин
- глицин
- аргинин
-аланин.
9. Выберите протеиногенные и непротеиногенные аминокислоты (глутамин, β -аланин, аргинин, треонин, γ -аминомасляная кислота, гомосерин, глицин, орнитин)и заполните следующую таблицу:
| Протеиногенные аминокислоты | Непротеиногенные аминокислоты | ||
| название | формула | название | формула |
10. Напишите формулы и укажите отличия в физических свойствах следующих аминокислот:
| Название | Формула | Физические свойства |
| L/+/-аланин | ||
| В /-/- аланин |
11. Дайте названия следующим аминокислотам и укажите классы, к которым они относятся.
| Формула аминокислоты | Название аминокислоты | Название класса |
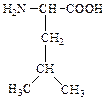
| ||
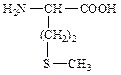
| ||
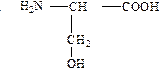
| ||
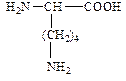
| ||
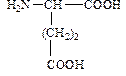
|
12. Напишите в транс-форме и назовите трипептид, состоящий из следующих аминокислот:
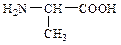
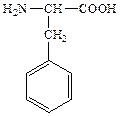
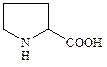
13. Напишите название данного трипептида. Какая связь образуется между аминокислотами этого пептида? В образовании каких связей могут принимать участие боковые радикалы этих аминокислот?
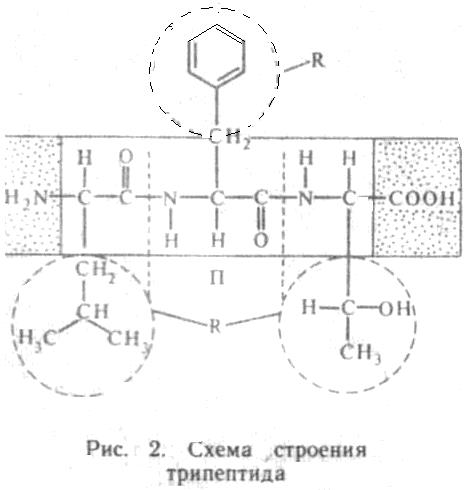
13. Опишите образование пептидной связи на примере аланина и метионина:
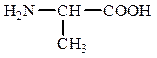 +
+ 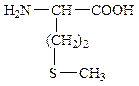 →
→
Дайте название полученному дипептиду и охарактеризуйте пептидную связь с электронной точки зрения.
14. Изобразите пептидную связь в виде пограничных мезомерных структур.
15. Опишите, как происходит образование водородных связей между пептидными группами атомов в белковой молекуле в случае а) и б), изображённых на рисунке:
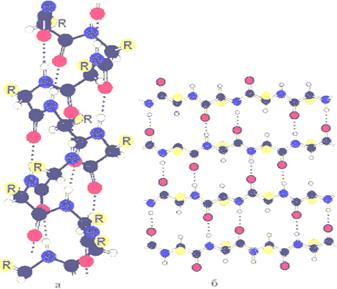
Какой тип вторичной структуры формируется в 1-ом и 2-ом случае?
16. Назовите ковалентные и нековалентные связи в белковой молекуле:
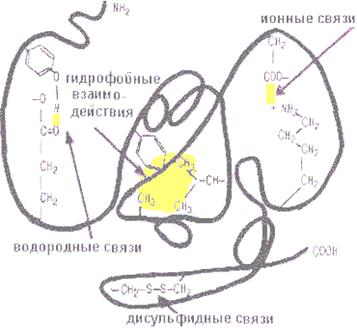
Заполните следующую таблицу:
| Ковалентные связи | Нековалентные связи | |||
| 1. | 2. | 1. | 2. | 3. |