
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Методы определения порядка реакции
|
|
Для определения порядка реакции необходимо иметь данные об изменении концентрации реагирующих веществ во времени или кинетическую кривую.
1.3.1. Метод «подбора уравнений»
Аналитический вариант. Полученные данные о зависимости концентрации реагента от времени подставляются в уравнение (12) для расчета константы скорости реакции первого порядка. Если получающиеся константы не зависят от времени, то предположение верно. Если вычисленные константы зависят от времени, то аналогичный расчет последовательно повторяется с использованием кинетических уравнений для второго и третьего порядка.
Графический вариант. Для экспериментально полученной зависимости
концентрации реагента А от времени строим графики, соответствующие
уравнениям разных порядков:

Рис.5. Графики определения порядка реакции
Выбираем график, на котором получена прямая линия и порядок определяется по типу графика.
1.3.2. Метод Раковского
В этом методе изучают зависимость периода полупревращения от Со. Для реакций первого порядка (14) 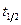 не зависит от начальной концентрации вещества.
не зависит от начальной концентрации вещества.
Для реакции 2-го порядка уравнение (18) может быть записано:
 или
или 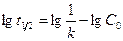 (22)
(22)
Для реакции 3-го порядка:
 или
или  (23)
(23)
В соответствии с уравнениями (22 и 23) зависимость 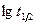 от
от  представляет прямую линию, тангенс угла наклона которой равен (n-1), где n является порядком реакции. Построение графика зависимости
представляет прямую линию, тангенс угла наклона которой равен (n-1), где n является порядком реакции. Построение графика зависимости 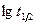 от
от  путем определения времени полупревращения на основе данных для одного опыта (рис.6). Кривая 6а разбивается равномерно и определяется среднее время полупревращения для каждого периода. По тангенсу угла наклона определяется порядок реакции.
путем определения времени полупревращения на основе данных для одного опыта (рис.6). Кривая 6а разбивается равномерно и определяется среднее время полупревращения для каждого периода. По тангенсу угла наклона определяется порядок реакции.

Рис.6. Определение порядка реакции по периоду полупревращения:
а - определение  и
и 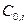 по кинетической кривой; б - определение порядка реакции.
по кинетической кривой; б - определение порядка реакции.
1.3.3. Дифференциальный метод Вант-Гоффа
Метод основан на использовании уравнения для скорости реакции в дифференциальной форме. Так графический вариант метода Вант-Гоффа основан на использовании уравнения 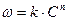 , после логарифмирования которого получают:
, после логарифмирования которого получают:
 (24)
(24)
На графике в координатах  полученная зависимость изображается прямой линией с тангенсом угла наклона к оси
полученная зависимость изображается прямой линией с тангенсом угла наклона к оси 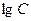 , соответствующим порядку реакции (
, соответствующим порядку реакции ( ). Скорость ω определяется тангенсом угла наклона касательной к кривой C = f (t) относительно оси времени как показано на рис.7.
). Скорость ω определяется тангенсом угла наклона касательной к кривой C = f (t) относительно оси времени как показано на рис.7.
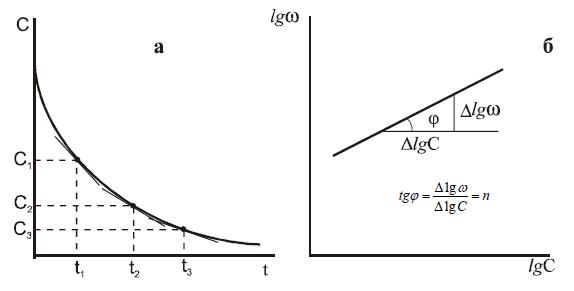
Рис 7. Определение порядка реакции по методу Вант-Гоффа: a - определение скорости реакции в различные моменты времени; б - определение порядка реакции.