
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Дифференциального кинетического уравнения
|
|
Определим константы дифференциального кинетического уравнения для следующей реакции:
аА + bB → продукты.
Зависимость скорости от концентраций выражается уравнением (2.3)
 .
.
Прологарифмируем это выражение
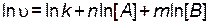 . .
| (2.4) |
Так как величины k, n и m для рассматриваемой реакции (при T = const) являются постоянными и не зависят от концентрации реагентов, то для их нахождения достаточно определить зависимость скорости реакции от концентрации одного из реагентов при фиксированной концентрации другого реагента.
Пусть в трех опытах концентрация вещества А будет постоянной и равной [ A ]0, тогда в уравнении (2.4) сумма (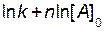 ) будет тоже величиной постоянной, обозначим ее
) будет тоже величиной постоянной, обозначим ее
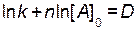 .
.
Тогда уравнение (2.4) можно переписать как
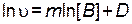 . .
| (2.5) |
Зависимость (2.5) представляет собой в координатах ln[ B ] —  уравнение прямой линии, тангенс угла наклона которой к оси абсцисс численно равен порядку реакции по веществу В.
уравнение прямой линии, тангенс угла наклона которой к оси абсцисс численно равен порядку реакции по веществу В.
По экспериментальным данным строят график зависимости  от ln[ B ] (рис. 3) и находят порядок реакции по веществу B
от ln[ B ] (рис. 3) и находят порядок реакции по веществу B
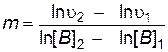 .
.
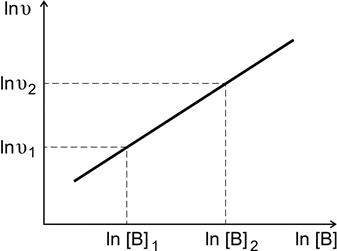
Рис.3. Определение порядка реакции по веществу В
В последующих опытах определяют скорость реакции при различных исходных концентрациях вещества А и постоянной концентрации [ B ]0. Находят порядок реакции по веществу А
 .
.
Из уравнения (2.3) с учетом найденных порядков реакции по веществам А и В рассчитывают константу скорости
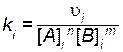 ,
,
где  , [ A ] i, [ B ] i - экспериментальные данные, относящиеся к одному опыту.
, [ A ] i, [ B ] i - экспериментальные данные, относящиеся к одному опыту.