
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Распознавание простейших
|
|
К сожалению, на настоящий момент сравнительно мало известно о молекулярных основах взаимодействия факторов естественного иммунитета со структурами патогенных простейших. Охарактеризованные вещества, удовлетворяющие определению структуры распознавания приведены в таблице 8.
Таблица 8. Патоген-ассоциированные молекулярные структуры простейших.
| ПАМС | Вид | Стадия | Структура | ТПР |
| Гликозил-инозитол-фосфат (ГИФ) | L. major | Промастиготы | Липополиглюкан | ТПР2 |
| T.cruzi | Трипомастиготы | ГИФ+алкилацилглицерин | ТПР2 | |
| Эпимастиготы | ГИФ+церамид | ТПР4 | ||
| P.falciparum | Мерозоит | ГИФЛ, ГИФ+белок | ТПР2 ТПР4 | |
| T.gondii | Тахизоиты | ГИФЛ, ГИФ | ТПР2 ТПР4 | |
| P.falciparum, T.gondii | ГИФ | CD1d, Vа14/Vb8ТКР | ||
| Геномная ДНК | T.cruzi | Все стадии | CpG-мотивы | ТПР9 |
| Гемозоин | P.falciparum | Мерозоиты | Бета-гематин | ТПР9 |
| Профилин | T.gondii | Тахизоиты | Профилин | ТПР11 |
| PfEMP1 | P.falciparum | Мерозоиты | Поверхностный белок эритроцитов (синтезируется P.falciparum) | CD36, ICAM, VCAM, CD31, тромбоспондин, Е-селектин и т.д. |
| Фосфатидил-серин | L.major, P.falciparum | Маркер апоптоза | CD36, скавенжер-рецепторы | |
| Изопентинил пирофосфат | P.falciparum | Мерозоиты | g/dТКР | |
| Сахариды клеточной поверхности | МР |
1. Гликозил-инозитолфосфат (ГИФ)
В отличие от патогенных грибов и бактерий, значимые для медицины простейшие не имеют выраженной клеточной стенки (особенно внешних, по отношению к ЦПМ, структур). Роль КС у них играет пелликула – структура, расположенная непосредственно под ЦПМ, имеющая различное строение у отдельных групп простейших: от однослойных псевдомембранных структур (Euglena) до многослойных мембранных и везикулярных слоев сложно ассоциированных с цитоскелетом (Balantidium). Таким образом, первой структурой, которая контактирует с внешней средой у патогенных простейших является ЦПМ. Уже ранние исследования взаимодействия простейших с иммунной системой показали способность мембранной фракции стимулировать клетки лимфоидной и миелоидной природы. Позже эта активность была ассоциирована с гликозил-фосфатидил-инозитолом (ГФИ). ГФИ является молекулой, закрепляющей белки в мембране эукариотических клеток (в т.ч. у человека) и интенсивно экспрессирована на ЦПМ (до 107/клетку). ГФИ состоит из сахаридной цепи и липидного компонента (глицериновые эфиры жирных кислот или церамид).
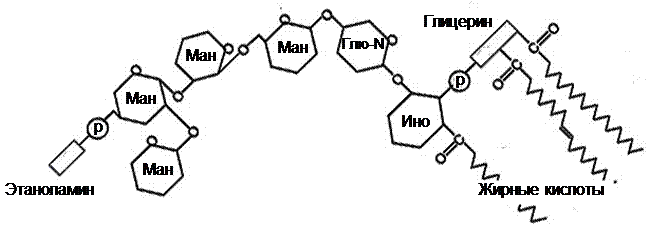
Видоспецифичность ГФИ обеспечивается количеством остатков маннозы, боковыми радикалами, липидной составляющей (ненасыщенные и насыщенные жирные кислоты).
Для примера (см. рисунок 16) приведем схему строения внешней оболочки T.cruzi (трипомастиготы). Поверхность клетки покрыта муцинами, закрепленными в мембране посредством ГИФ; кроме того присутствует большое количество ГИФЛ, липидный компонент которого распознается ТПР2 или ТПР4 в комплексе с CD14. Аналогично, сами якорные ГИФ или их соединения с белками и, особенно, липидами, распознаются как маркер присутсвия других патогенных простейших основных групп.

Рисунок 16. Схема строения внешней оболочки T.cruzi (трипомастиготы).
Помимо сигнальных рецепторов, ГФИ также распознаются некоторыми эффекторными рецепторами:
фосфатазы и липазы клеточной поверхности - расщепляют ГИФ на компоненты, лишенные сигнальной активности, что весьма важно для регулирования активации иммунной системы и ассоциированной токсичности, например, при малярии;
лектиновые рецепторы с опсонизирующими, фагоцитарными и лизирующими функциями;
CD1d, Vа14/Vb8ТКР – ГФИ-специфичные рецепторы на ЕКТ-клетках, которые играют важную роль в быстрой организации «правильного» микроокружения путем секреции цитокинов Th1 спектра (в данном случае).
 2. Геномная ДНК простейших, содержащая неметилированные CpG мотивы распознается ТПР9 внутриклеточно (в эндосомах). Следует иметь ввиду, что ДНК некоторых простейших, например, возбудителя малярии, характеризуется низким содержанием CpG и не активирует клетки иммунной системы.
2. Геномная ДНК простейших, содержащая неметилированные CpG мотивы распознается ТПР9 внутриклеточно (в эндосомах). Следует иметь ввиду, что ДНК некоторых простейших, например, возбудителя малярии, характеризуется низким содержанием CpG и не активирует клетки иммунной системы.
3. Гемозоин – продукт ферментации гемоглобина возбудителем малярии (стадия трофозоита), который накапливается внутри эритроцита в виде кристаллов коричневого цвета. При фагоцитозе зараженных или разрушенных эритроцитов попадает в эндосомы, где распознается ТПР9.
4. Профилин – актин-связывающий белок эукариот, регулирующий полимеризацию актина, присутствует у всех представителей Apicomplexa и распознается ТПР11 (у человека не функционирует).
5. PfEMP1 – название вариантного поверхностного белка эритроцитов, продуцируемого возбудителями малярии, которые позволяют инфицированным эритроцитам задерживаться на эндотелии сосудов и избегать разрушения в селезенке. PfEMP распознается CD36, CD31, ICAM, VCAM, Е-селектином, тромбоспондином, гиалуроновой кислотой, хондроитин-сульфатом А и др. молекулами. Эти рецепторные взаимодействия важны для фагоцитоза и инициации иммунного ответа.
6. Фосфосерин – распознается скавенжер-рецепторами (CD36) для утилизации апоптических клеток. Используется паразитами для проникновения в в клетки ретикуло-эндотелиальной системы путем «невоспалительного» фагоцитоза (т.е. без индукции приобретенного иммунного ответа).
7. Пирофосфаты клеточной поверхности – распознаются рецепторами гамма-дельта Т-клеток (особенно актуально для слизистых оболочек).
8. Неустановленные сахара клеточной поверхности (манноза) – распознаются маннозным рецептором (МР), факторами системы комплемента, рецепторами ЕК, скавенджер-рецепторами и др.
Распознавание соответствующих лигандов сигнальными рецепторами приводит к активации дендритных клеток и макрофагов, синтезу цитокинов и развитию адаптивного иммунного ответа, Необходимо отметить, что ограничение инвазии ассоциируется с ответом по Th1 типу, т.е. с развитием сильного иммунного воспаления, образованием цитотоксических Т-лимфоцитов, цитофильных антител и эффекторов ГЗТ. Вместе с этим, активация макрофагов ведет к резкому повышению цитотоксического потенциала и генерации противомикробных веществ, способствующих немедленному уничтожению паразитов.
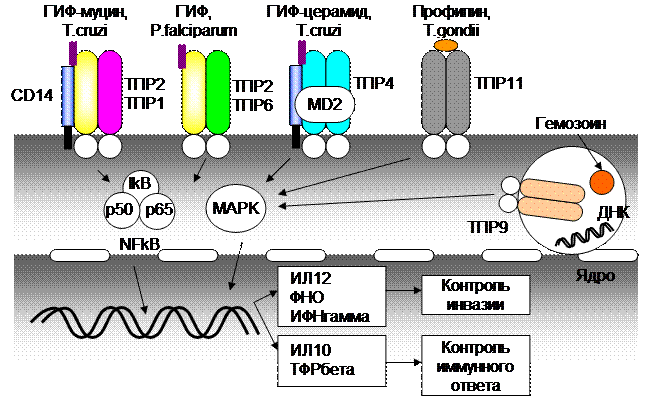
Следует отметить, что наряду с развитием иммунного ответа Th1 типа, происходят синтез и секреция противовоспалительных цитокинов (ИЛ10, ТФРбета), активация и пролиферация Т-регуляторных клеток, которые ограничивают интенсивность иммунного воспаления и играют важную роль в организации персистенции и установлении равновесия между иммунным ответом и инвазией паразита. Сохранение возбудителя в организме объясняется высокой степенью адаптации возбудителя, устойчивостью его к основным эффекторным механизмам системы естественного иммунитета (комплемент, фагоцитоз, антитела), манипулированием адаптивным иммунным ответом (иммунологическое отклонение, иммуносупрессия). Тем не менее, иммунная система способна ограничить степень инвазии, на что указывает значительно более тяжелые формы заболеваний у животных, нокаутированных по My88, а также у людей с ИДС (дефекты экспрессии МР, синтеза NO, цитокинов: ИЛ12, ФНОа).
В заключение следует указать некоторые примеры практического применения знаний о закономерностях распознавания простейших иммунной системой:
А) приготовление вакцин с молекулами ПАМС простейших:
| Малярия Трипаносомозы Лейшманиоз Токсоплазмоз | монофосфорил-липид А CpG ДНК Флагеллин | + антигены простейших |
Б) Терапия кризов при малярии, болезни Чагаса:
антитела к ГИФ,
блокирующие антитела к ТПР2, 4