
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
АТФ адф
|
|
Рисунок 11 – Схема біосинтезу коензиму А
Нормальна концентрація та поширення у тканинах. Вміст вітаміну В5у плазмі крові становить15 – 45 мг/100 мл. У невеликій кількості він наявний у всіх тканинах організму. Найбільші концентрації відмічені у печінці, серці, нирках.
Екскреція. Продукти катаболізму пантотенової кислотиневідомі. За умов нормального харчування із сечею виділяється від 2, 5 до 5 мг/добу вітаміну В5, із потом екскретується 3 – 4 мг/100 мл, секретується з молоком 200 – 300 мг/100 мл.
Поширення у природі та добова потреба
Вітамін В5 значно поширений у тканинах рослин та тварин.
Джерела:
· продукти тваринного походження: печінка, нирки, яєчний жовток, знежирене молоко, сир, курятина, риба;
· продукти рослинного походження: хлібні злаки, боби, хліб із висівками, солодка картопля;
· дріжджі;
· більшість овочів і фруктів бідні на вітамін В5;
· близько 57 % вітаміну руйнується під час виготовлення борошна та 33 % при кулінарній обробці м'яса;
· більше ніж 3, 4 мг на добу синтезується мікрофлорою кишечнику, за відсутності дисбактеріозу.
Добова потреба у пантотеновій кислоті невідома через її значне поширення у природі.
Рекомендоване добове споживання на 2500 кал:
· дорослі: 5 – 12 мг;
· новонароджені: 1 –2 мг;
· діти: 4 – 5 мг;
· вагітні жінки 15 – 20 мг.
Потреба у вітаміні підвищується при гострих захворюваннях, опіках, серйозних пораненнях, лікуванні антибіотиками, під час видужання після хвороби, у період вагітності та лактації. Для забезпечення достатньої кількості вітаміну у дітей, що інтенсивно ростуть, у період формування мозку та інших внутрішніх органів, молоко матері повинно вмішувати до 5 мг пантотенової кислотина 1 л. Потреба у вітаміні В5 збільшується при стресових станах, великих фізичних навантаженнях, заняттях спортом.
Біологічна роль
Біологічна роль пантотенової кислотипов'язана з її входжен-ням до структури коферменту А (коферменту ацилювання), якийбере участь у реакціях активації та перенесення ацетильного (СН3С=О) залишку та радикалів інших кислот. Внасладок утво-рення ацил-КоА карбонова кислота активується, складаються вигідні термодинамічні умови для її використання у ендерго-нічних процесах. Як компонент HS-КоА вітамін В5 необхіден для перебігу декількох фундаментальних біохімічних процесів.
1. Формування «активного» ацетату (ацетил-КоА). Коен-зим Алегко взаємодіє з ацетатом із утворенням метаболічно активного Ацетил-КоА:
О
║
СН3 - С ~ S-КоА.
Ацетил-КоАмістить у своїй структурі високоенергетичний сульфатний зв'язок, еквівалентний макроергічному фосфату АТФ. Близько 80 ферментів залежать від пантотенової кислоти. У формі активного ацетату вітамін бере участь у:
· циклі трикарбонових кислот – у реакції з оксалоацетатом утворює цитрат;
· реакціях ацетилювання;
· синтезі нейтральних жирів, ацетилхоліну, фосфоліпідів, холестеролу, кетонових тіл;
· біосинтезі та елонгації жирних кислот;
· β -окисненні жирних кислот;
· окиснювальному декарбоксилюванні пірувату та α -кетоглу-тарату;
· утворенні стероїдних гормонів кори надниркових залоз;
· активації амінокислот із розгалуженими ланцюгами – ізолейцину, лейцину, валіну;
· біосинтезі гіпурової кислоти.
2. Формування «активного» сукцинату (сукциніл-КоА). Сукциніл-КоА – продукт окиснювального декарбоксилювання α -кетоглутарату у циклі лимонної кислоти, який бере участь у нижче наведених метаболічних процесах:
· Синтезі гему. Сукциніл-КоА взаємодіє з гліцином і утворює δ -АЛК - ключовий метаболіт синтезу гему.
· Розщепленні кетонових тіл у позапечинкових тканинах.
Прояви вітамінної недостатності
У людини ізольований дефіцит пантотенової кислотивиникає рідко через її значне поширення у харчових продуктах і біосинтез мікрофлорою ШКТ. Недостатність вітаміну В5 проявляється у вигляді:
· дерматитів, депігментації волосся, алопеції;
· виснаження, зупинення росту, анемії;
· ураження слизових оболонок;
· дистрофічних змін залоз внутрішньої секреції, зокрема надниркових залоз, серця, нирок, ШКТ;
· порушень нервової системи – невритів, паралічів;
· печіння у стопах є характерним проявом дефіциту вітаміну.
Основні причини гіповітамінозу В5:
· захворювання ШКТ, при яких відбувається порушення природної мікрофлори кишечнику або всмоктування вітаміну;
· довготривале нераціональне харчування, лікування антибіотиками;
· часто є супутником інших гіповітамінозів.
Антивітамінивітаміну В5: пантоїлтаурин, ω -метилпанто-тенат.
Застосування вітаміну В5
Пантотенову кислоту використовують для лікування дерматитів, захворювань печінки, серця, у парфумерії.
4.5. Вітамін В6
(піридоксин, адермін, антидерматитний)
Хімічна структура та властивості
· За структурою вітамін В6є 2-метил-3-оксі-4, 5-діоксиметил-піримідином. Відповідно до Міжнародної номенклатури тер-міном «вітамін В6» позначають три похідні 3-оксипіридину, які мають однакову вітамінну активність: піридоксин (піридоксол), піридоксаль, піридоксамін.
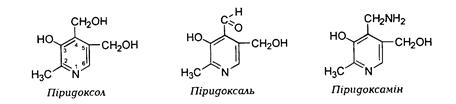
· Вітамін В6добре розчинний у воді та етанолі.
· Водні розчини вітаміну стійкі до кислот і лугів, але чутливі до дії ультрафіолетового світла при нейтральному рН.
· Вітамін стійкий до температури, але втрачається під час консервування.
Біологічно активні форми
Коферментні властивості притаманні лише фосфорильова-ним формам піридоксалю та піридоксаміну – ПАЛФ (піридоксальфосфат)і ПАМФ (піридоксамінфосфат). У природі вони зустрічаються в основному в комплексі з білками.
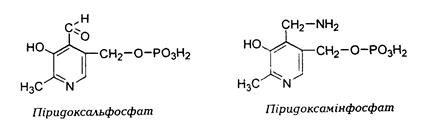
Фосфорилювання піридоксалю та піридоксаміну відбуваєть-ся у печінці, мозку та інших тканинах за участі АТФ, Zn++ і специфічних кіназ.
Утворення піридоксальфосфату:
Дегідрогеназа Кіназа, Zn++
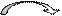

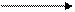 Піридоксин Піридоксаль Піридоксаль-Ф
Піридоксин Піридоксаль Піридоксаль-Ф
Фосфопротеїн Фосфопротеїн-Н2 АТФ АДФ+ Фн
У тканинах тварин відбувається взаємоперетворення коферментів піридоксальфосфату і піридоксамінфосфату, наприклад, у реакціях трансамінування та декарбоксилювання.
Біосинтез
Вітамін В6синтезується багатьма мікроорганізмами і росли-нами. В організмі людини він не утворюється, але у невеликій кількості синтезуватися мікроорганізмами кишечника.
Метаболізм
Всмоктування. Вітамін В6легко абсорбується у тонкому ки-шечнику простою дифузією і розноситься кров’ю до тканин. Частина – депонується у зв'язаному з білком вигляді, переважно у печінці, більшість перетворюється у коферментні форми.
Екскреція. Піридоксаль і піридоксаміну невеликій кількості (0, 5 - 0, 7 мг/добу) виводяться з сечею. Основний біологічно неактивний метаболіт, який екскретується - 4-піридоксинова кислота (3, 0 мг/добу).
Поширення у природі та добова потреба
Вітамін значно поширений у тканинах рослин і тварин. У рослинних продуктах переважає піридоксин, а у тваринних – піридоксальта піридоксамін. У багатьох продуктах тваринного походження піридоксинзнаходиться у комплексі з білками, але у ШКТ під дією ензимів він легко вивільняється і всмоктується.
Джерела:
· продукти рослинного походження: дріжджі, хліб, морква, червоний перець, картопля, горох, квасоля, крупи, капуста. У наших умовах основними джерелами вітаміну В6 є хліб та картопля;
· продукти тваринного походження: м'ясо, печінка, нирки, риба, жовток яйця.
Добова потреба у піридоксині для людини точно не встановлена, оскільки частково потреби у ньому задовольня-ються за рахунок синтезу мікрофлорою кишечнику. Розрахована добова потреба становить близько 2, 0 мг/добу. Вважається, що вона залежить від надходження білків з їжею, оскільки кофермент бере участь у багатьох реакція обміну амінокислот.
Добова потреба:
· дорослі: 2, 0 мг;
· новонароджені: 0, 3 – 0, 4 мг;
· жінки у другій половині
вагітності: 2, 5 мг.
Потреба значно підвищується при довготривалому лікуванні туберкульозу ізоніазидом, який є антивітаміном вітаміну В6.
Біологічна роль
Піридоксальфосфатдіє як кофермент, в основному у реакціях амінокислотного обміну.
· Трансамінування. ПАЛФі ПАМФ, що взаємоперетворю-ються, є коферментами амінотрансфераз у зворотних реакціях трансамінування амінокислот.
· Декарбоксилювання. Кофермент(ПАЛФ) декарбоксилаз у реакціях незворотного декарбоксилювання амінокислот із утворенням відповідних біогенних амінів:
o Тирозин → Тирамін + СО2.
o Гістидин → Гістамін + СО2.
o Глутамінова кислота → ГАМК + СО2.
· Коферментдеаміназ (дегідраз), які каталізують реакції нео-киснювального дезамінування гідроксіамінокислот серину та треоніну.
· Коферменткінуренінази, що перетворює 3-ОН-кінуренін на 3-ОН-антралову кислоту, з якої утворюється нікотинова кис-лота. Тому при нестачі В6 синтез ніацину з триптофануприпиняється. У крові підвищується рівень кінуреніну та 3-ОН-кінуреніну, які у позапечінкових тканинах перетворю-ються на ксантуринову кислоту. Остання виділяється з сечею, що є надійним критерієм діагностики дефіциту В6.
· Транссульфурування. Бере участь у перенесенні сульфгід-рильних (-SH) груп, наприклад, у реакції:
Гомоцистеїн + Серин → Гомосерин + Цистеїн.
· Коферментдисульфурази, яка каталізує неокиснювальне дезамінування цистеїну, при якому виділяється H2S.
· Бере участь у взаємоперетвореннях гліцину та серину серин-гідрокси-метилтрансферазою.
· Біосинтезі арахідоновоїкислотиз ліноленової.
· Синтез сфінгомієліну. ПАЛФ– кофермент у активації серину, останній необхідний для синтезу сфінгомієліну.
· Коферментрацемаз амінокислот:
D-Глутамінова кислота → L-Глутамінова кислота
D-Аланін → L-Аланін.
· Внутрішньомітохондріальний синтез жирних кислот – кофермент елонгації жирних кислот у мітохондріях.
· Необхідний для «активного транспорту» амінокислот через клітинну мембрану та їх абсорбції у кишечнику.
· Структурний компонент фосфорилази м'язів: чотири молекули піридоксальфосфату разом із однією молекулою ензиму утворюють тетрамерну структуру.
· Сприяє транспорту іонів К+ через мембрану у клітини.
· Діє як кофермент аміноацетонсинтетази в утворенні аміноацетону з ацетил-КоА та гліцину.
· Синтез КоА-SH з пантотенової кислоти. При гіповітамінозі В6 вміст коензиму А у печінці значно знижується.
· Синтез порфіринів. Піридоксальфосфатє коферментом δ - амінолевулінатсинтази – ключового ферменту синтезу ге-му. Недостатність вітаміну викликає розвиток анемії.
Прояви вітамінної недостатності
У людини гіповітаміноз В6 зустрічається рідко і не описано якоїсь специфічної хвороби його недостатності. Дефіцит піри-доксину краще вивчений на тваринах.
Клінічні та біохімічні прояви недостатності вітаміну В6:
у щурів спостерігається акродинія – специфічний дерматит, який вражає шкіру лапок, хвіст, ніс, вуха, дегенеративні зміни у ЦНС.
У людини:
· епілептиформні напади у немовлят, яких вигодовують незбалансованими за вітаміном В6 штучними сумішами. Зниження активності ПАЛФ-залежної глутаматдекарбок-силази призводить до зменшення утворення тормозного медіатора γ -аміномасляної кислоти у мозку, підвищеннязбудливості нервової системи, що є причиною судом.
· Пелагроподібні дерматити, які не лікуються нікотиновою кислотою, але швидко зникають після введення піридоксину.
· Піридоксинзалежна анемія. Недостатність вітаміну В6 супроводжується розвитком гіпохромної мікроцетарної «сидеробластичної» анемії, яка характеризується високим вмістом залізау крові, гемосидерозом печінки, селезінки, кісткового мозку. ПАЛФ- кофермент декарбоксилювання α -аміно-β -кетоадипінової кислоти до δ -АЛК у синтезі гему. Зниження утворення гемупризводить до неможливості утилізації залізаі його накопичення у тканинах.
· ГіповітамінозВ6 супроводжується також гомоцистеїнурією, цистатіонінурією, оксалурією, порушенням обміну крипто-фану, гіперхолестеролемією, зниженням імунітету.
· Ранньою лабораторною ознакою дефіциту вітаміну є зменшення виділення з сечею 4-піридоксинової кислоти та зниження активності еритроцитарних амінотрансфераз.
Основні причини гіповітамінозу В6
· Випадки ізольованого дефіциту, що пов′ язані з дієтою, не описані, однак при обмеженому вживанні хліба, переважно-му харчуванні м′ ясом та молочними продуктами надход-ження вітаміну знижується.
· Захворювання, при яких порушується всмоктування вітамі-ну, або станах, при яких він надмірно використовується.
· Використання лікарських засобів – антагоністів вітаміну: протисухотних препаратів, пеніциламіну, L-ДОФА, естро-генів. Тривале лікування туберкульозу ізоніазидомє причиною розвитку у хворих вітамін-В6-дефіцитного синдрому, що пов'язане з антивітамінною дією препарату. Легка форма недостатності піридоксину виникає у жінок, які вживають естрадіоловмісні оральні контрацептиви.
· Дефіцит вітаміну може розвинутися у стресовому стані, під час лихоманки, гіпертиреозу, вагітності, мальабсорбції, при захворюваннях, які супроводжуються катаболізмом білків.
· У алкоголіків розпад вітаміну В6 підсилюється за рахунок дії ацетальдегіду на активність його оксидази.
ГіпервітамінозВ6 розвивається при надмірному вживанні вітаміну (від 2 г/добу) і супроводжується онімінням шкіри навколо рота, порушенням вібраційної чутливості.
Антивітамінивітаміну В6
· Дезоксипіридоксин, циклосерин, ізонікотиноілгідразид (ізоніазид).
Застосування вітаміну В6.
Піридоксин використовують для лікування і профілактики гіповітамінозу В6 під час лікування ізоніазидом, антибіотиками; уроджених піридоксинзалежних анемій, токсикозів вагітності, невритів, дерматитів, псоріазу, променевої, морської, повітряної хвороби, м'язових дистрофій, гіпероксалурії, захворювань печінки.
4.6. Вітамін Вc (фолієва кислота)
Синоніми. Залежно від виду тварин або штаму бактерій, для росту яких необхідна фолієва кислота, вітамін називається фолацин, фактор росту L. casei, вітамін М (фактор кровотво-рення у мавп), вітамін В9, вітамін Вс (фактор росту курчат), птероїлглутамінова кислота.
Хімічна структура та властивості
· фолієва кислотаскладається з 3 структурних компонентів: птеридинового ядра (2-аміно-4-окси-6-метилптеридину), параамінобензойної кислоти (ПАБК), глутамінової кислоти.
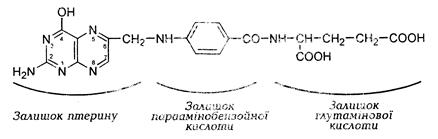
· Форми фолієвої кислоти відрізняються кількістю залишків глутамінової кислоти у її складі. Можливе зв'язування птеридин-ПАБКз 1, 3, 7 залишками глутамінової кислоти.
· Вітамін обмежено розчинний у воді, краще у спиртових розчинах.
· Фолацин термічно нестійкий.
Біологічно активні форми
Коферментною формою фолієвої кислоти є її відновлене похідне – 5, 6, 7, 8 – тетрагідрофолева кислота(ТГФК). Відновлення вітаміну відбувається за рахунок приєднання чотирьох атомів водню до птеридинового залишку.
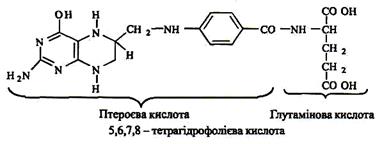
Синтез коферменту відбувається у два етапи: спершу утворюється 7, 8-дегідрофолієва кислота (Н2-Фолат, FH2), потім - 5, 6, 7, 8-ТГФК(Н4-Фолат, FH4). Обидві реакції каталізують ферменти – фолатредуктази, які використовують НАДФН2 як донор водню та аскорбінову кислоту як кофактор:
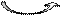
 НАДФН+Н+ Віт.С НАДФ+ НАДФН+Н+ Віт.С НАДФ+
НАДФН+Н+ Віт.С НАДФ+ НАДФН+Н+ Віт.С НАДФ+
 Фолат Н2-Фолат Н4-Фолат.
Фолат Н2-Фолат Н4-Фолат.
Фолатредуктаза Дегідрофолатредуктаза
Біосинтез
· Фолієва кислота синтезується мікроорганізмами ШКТ. Деякі з них не утворюють ПАБК, остання повинна надходити ззовні. За участі АТФ та КоА-SН ПАБК реагує з глутаміновою кислотою з утворенням ρ -аміно-бензоїл глутамінової кислоти. Поєднання останньої із залишком птерину утворює фолієву кислоту (птероїл моноглутамінову кислоту). Птерин може утворюватися із гуанозину.