
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Устройство кислотных аккумуляторов
|
|
Кислотный аккумулятор изображен на рис. 5.8.
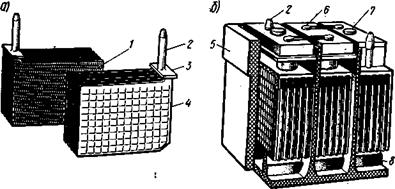
Рис. 5.8. Кислотный аккумулятор: а – пластины; б – общий вид
Кислотный аккумулятор (рис. 5.8) состоит из эбонитового или пластмассового корпуса 5, отрицательных 1 и положительных 4 пластин, собранных с помощью соедини
тельных мостиков (бареток) 3 вполублоки, и электролита, в который погружены пласти-
ны.
С помощью борнов 2 (полюсных выводов) и межэлементных соединений (перемы-
чек) 6 блоки пластин соединяют в электрическую цепь. Для изоляции разноименных пла-
стин в аккумуляторе применяют сепараторы из различных пластмасс, на крышках аккуму-
лятора устанавливают вывинчивающиеся пробки 7, в нижней части пластины опираются на изоляционные призмы 8.
Положительные и отрицательные пластины отливают в виде решеток из химически чистого свинца с 5-10 %-ной присадкой сурьмы. Решетки пластин заполняют активными массами: активная масса положительных пластин состоит из свинцового сурика Рb02 и сульфата аммония, отрицательных - из свинцового глета (губчатый свинец) с добавлением сернокислого бария. Отрицательные пластины механически более прочны, поэтому в бло-
ке их на одну больше, они располагаются с обеих сторон.
Электролитом служит раствор химически чистой серной кислоты в дистиллирован
ной воде.
Когда серную кислоту вливают в воду, в результате химической диссоциации часть молекул кислоты распадается на положительные и отрицательные ионы Н  и SO
и SO  .
.
Таким образом в электролите присутствуют ионы-носители электрического заряда и целые молекулы кислоты Н  SO
SO  .
.
Во время разряда аккумулятора в нем протекают следующие реакции:
у отрицательных пластин Рb + SO  = Рb SO
= Рb SO  ,
,
у положительных пластин РbО  + Н
+ Н  + Н
+ Н  SO
SO  = Рb SO
= Рb SO  + 2 Н
+ 2 Н  О. Положительные и отрицательные ионы электролита вступают в реакцию с активны
О. Положительные и отрицательные ионы электролита вступают в реакцию с активны
ми массами пластин, изменяя их состав и отдавая электрический заряд на пластину. На всех пластинах образуется сульфат свинца Рb SO  .
.
Количество ионов SO  в электролите уменьшается; поэтому его плотность в про-
в электролите уменьшается; поэтому его плотность в про-
цессе разряда заметно снижается.
Аккумулятор будет источником электроэнергии до тех пор, пока текут реакции разряда, а они возможны, если еще не вся активная масса пластин РbО  и Рb превращены в Рb SO
и Рb превращены в Рb SO  , т. е. пока в растворе есть ионы. Полный разряд не рекомендуется.
, т. е. пока в растворе есть ионы. Полный разряд не рекомендуется.
При подключении аккумулятора к источнику постоянного тока под действием за
рядного тока протекают обратные реакции заряда:
у отрицательных пластин Рb SO  + Н
+ Н  = Рb + Н
= Рb + Н  SO
SO  ;
;
у положительных пластин Рb SO  + 2 Н
+ 2 Н  О + SO
О + SO  = РbО
= РbО  + 2 Н
+ 2 Н  SO
SO  .
.
В результате Рb SO  распадается на исходные материалы пластин, и в раствор выделяется кислота, поэтому плотность увеличивается до исходного значения (1, 24-1, 31 г/см
распадается на исходные материалы пластин, и в раствор выделяется кислота, поэтому плотность увеличивается до исходного значения (1, 24-1, 31 г/см  ) в зависимости от климатических условий), причем ЭДС заряженного аккумулятора составляет 2, 1 В.
) в зависимости от климатических условий), причем ЭДС заряженного аккумулятора составляет 2, 1 В.
Опытным путем установлена зависимость между ЭДС и плотностью электро
лита для кислотного аккумулятора:
Е = 0, 84 + d,
где d: плотность электролита, г/см3.
Напряжение аккумулятора в режимах разряда и заряда:
Uр = 0, 84 + d – Iр Rвн,
Uз = 0, 84 + d + Iз Rвн,
где: Iр – ток разряда, А;
Iз – ток заряда, А;
Rвн – внутреннее сопротивление аккумулятора.
Обычно принимают Rвн = 0, 005 Ом.