
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Экспериментальная часть. Оборудование и реактивы:
|
|
Оборудование и реактивы:
1. Раствор CuSO4, 0, 1н. В мерной колбе ёмкостью 1л. растворяют в воде 12, 48г. CuSO4× 5Н2О и доводят объём раствора до метки.
2. 0, 05н. раствор трилона Б.
3. Ацетатный буфер.
4. Индикатор ПАН, 0, 1% спиртовой раствор.
Ход работы:
1. В три конические колбы на 25мл. помещают 20г. воздушно-сухой почвы: песчаной (колба №1), глинистой (колба №2) и торфа (колба №3). В каждую колбу наливают по 50 мл. раствора CuSO4, перемешивают 1 – 3мин. и оставляют на 30мин.
2. Пока устанавливается адсорбционное равновесие между почвой и раствором определяют расход раствора трилона Б на титрование исходного раствора CuSO4 – V0, мл. С этой целью в коническую колбу вносят 5мл. исходного раствора CuSO4, добавляют 3 – 4 капли 2 – 3 капли индикатора ПАН и титруют 0, 05н. раствором трилона Б до перехода сиренево-розовой окраски в зеленую. Определение повторяют дважды и V0 находят как среднее значение двух титрований:
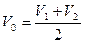 , мл.
, мл.
3. Готовят три сухие конические колбы. В каждую помещают воронку со складчатым фильтром и отфильтровывают образцы почвы.
4. В коническую колбу отбирают пипеткой 5мл. фильтрата, добавляют 3 – 4 капли ацетатного буфера и 2 – 3 капли раствора индикатора ПАН. Титруют раствором трилона Б до перехода сиренево-розовой окраски в зеленую. При этом определяют объём трилона Б, затраченный на титрование фильтрата после адсорбции V1. Такое титрование производят для каждого из трех фильтратов. Результаты титрований заносят в табл.3:
Таблица 3
Результаты измерений
| Вид почвы | Масса почвы а, г. | Объем пробы Vпр, мл. | Расход трилона Б, мл | Адсорбция меди G, мг/г. | |
| V0, мл. | V1, мл. | ||||
| Песок | |||||
| Глина | |||||
| Торф |
Примечание: Vпр – объем пробы взятой для титрования;
V0 – используют среднее значение двух титрований.
5. Последовательность расчёта количества адсорбированной меди.
Расчёт основан на законе эквивалентности, т.е. при титровании в точке эквивалентности количество прореагировавших моль-эквивалентов меди и трилона Б равны.
Находят количество моль-эквивалентов меди в 5мл. исходного раствора nCu:
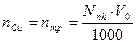
где Nтр – нормальность раствора трилона Б, моль-экв/л. Эквивалент меди равен 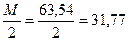 г.
г.
Первоначальное содержание меди во всем растворе, добавленном к почве, m1, мг определяют из соотношения:
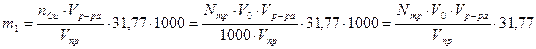 мг. Cu
мг. Cu
где Vр-ра – объём раствора CuSO4добавленный к почве, мл.
соответственно, количество эквивалентов меди 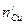 в пробе фильтрата после адсорбции составляет:
в пробе фильтрата после адсорбции составляет:
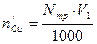
Содержание меди во всем растворе после установления адсорбционного равновесия m2, мг находят аналогично:
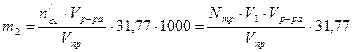 мг. Cu
мг. Cu
Количество адсорбированной меди G в мг. на 1г. почвы рассчитывают по формуле:

Полученные значения G для разных видов почвы заносят в таблицу 1 и делают вывод о влиянии характера почвенного слоя на его способность удерживать и накапливать катион Сu2+.
(Практикум…, 1987)
Контрольные вопросы
1. Какова положительная и отрицательная роль меди в растениях?
2. Какие Вам известны источники поступления меди в почву?
3. Что является основным процессом, контролирующим содержание водорастворимых форм тяжелых металлов в почвах?