
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Определение перманганатной окисляемости
|
|
Оборудование и реактивы:
1. Перманганат калия KMnO4, 0, 01моль-экв/л (0, 01н) раствор. Навеску KMnO4 0, 33–0, 35г переносят в мерную колбу на 1л, растворяют в воде и доводят объем раствора до метки. Раствор выдерживают 7–10 дней в темном месте в плотно закрытой склянке. Образовавшийся осадок отфильтровывают через стеклянный фильтр. Раствор хранят в темной бутыли.
2. Щавелевая кислота Н2С2О4, 0, 01моль-экв/л (0, 01н) раствор. Готовят из фиксанала или по навеске Н2С2О4´ 2Н2О, х.ч. Щавелевая кислота в растворе постепенно разлагается и долго храниться не может. Для получения более устойчивого раствора рекомендуется использовать в качестве растворителя разбавленную 1: 15 серную кислоту.
3. Серная кислота Н2SO4, 4 моль-экв/л (4н) раствор.
Ход работы:
1. Устанавливают нормальность раствора перманганата.
В коническую колбу помещают 20 мл 0, 01н раствора щавелевой кислоты, приливают 5мл 4н раствора Н2SO4 и нагревают до 80-90°С (не кипятить). Затем медленно титруют раствором перманганата калия, подложив под колбу лист белой бумаги для лучшего наблюдения изменения окраски.
Отсчеты в бюретке с раствором перманганата производят по верхнему краю мениска (то же самое при установлении ² нуля²). Титрование проводят при интенсивном перемешивании. К концу титрования колбу при необходимости подогревают и продолжают титрование до появления устойчивого (в течении не менее 30сек.) бледно-розового окрашивания. Определение повторяют 2-3 раза и рассчитывают нормальность раствора перманганата: 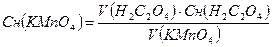 ; моль-экв/л.
; моль-экв/л.
где V(Н2С2О4) – объем раствора щавелевой кислоты, мл.
Cн(Н2С2О4) KMnO4– нормальность раствора щавелевой кислоты, моль-экв/л.
V(KMnO4) – объем раствора перманганата калия, пошедший на титрование, мл.
2. Окисление пробы воды.
В коническую колбу на 250мл помещают несколько стеклянных шариков или капилляров для равномерного кипения и вносят пипеткой 20-25мл анализируемой воды, приливают 10мл 4н серной кислоты и 20мл раствора перманганата калия. Колбу закрывают воронкой, нагревают до кипения и кипятят 10мин. К горячему раствору прибавляют 20мл 0, 01н раствора щавелевой кислоты. Обесцвеченную смесь титруют при 80-90°С 0, 01н раствором перманганата калия до появления устойчивого светло-розового окрашивания. Если раствор при кипячении обесцветится или побуреет, определение повторяют, предварительно разбавив пробу или используя больший объём раствора KMnO4 для окисления. Определение повторяют и тогда, когда перманганата расходуется более 60% добавленного количества, т.е. расход на титрование превышает 12мл. При титровании разбавленных проб не должно быть израсходовано меньше 20% добавленного количества перманганата калия, т.е. меньше 4мл.
Окисляемость в мг О2/л вычисляют по формуле:
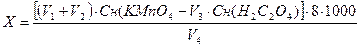 ,
,
где V1 – объем раствора KMnO4, прибавленный до кипячения, мл;
V2 – объем раствора KMnO4, израсходованный на титрование, мл;
V3 – объем добавленного раствора Н2С2О4, мл;
V4 – объем пробы воды, взятый на анализ, мл;
Сн(KMnO4) – нормальность раствора перманганата калия, моль-экв/л;
Cн(Н2С2О4) – нормальность раствора щавелевой кислоты, моль-экв/л;
8 – эквивалент кислорода, г.
Для определения окисляемости используют водопроводную воду (после двухчасового отстаивания), речную и талую воду из снега с различной степенью загрязнения. При анализе водопроводной воды объём пробы увеличивают до 50 мл.