
Главная страница Случайная страница
КАТЕГОРИИ:
АвтомобилиАстрономияБиологияГеографияДом и садДругие языкиДругоеИнформатикаИсторияКультураЛитератураЛогикаМатематикаМедицинаМеталлургияМеханикаОбразованиеОхрана трудаПедагогикаПолитикаПравоПсихологияРелигияРиторикаСоциологияСпортСтроительствоТехнологияТуризмФизикаФилософияФинансыХимияЧерчениеЭкологияЭкономикаЭлектроника
Дата: 05.04.13
|
|
Пропись № 1 Sol. Novocaini 2%-100 ml
Р-р Новокаина 2%-100 мл
Описание: представляет собой бесцветную, прозрачную жидкость без запаха, без механических примесей. Общий объем – 100 мл.
ОПРЕДЛЕНИЕ ПОДЛИННОСТИ:
На новокаин: реакция азосочитания. К 1 мл раствора прибавляют 5 – 6 капель разведенной кислоты хлористоводородной, 2 – 3 капли 0, 1М раствора натрия нитрита, а затем 10 капель натрия гидроксида. Появляется вишнево-красное окрашивание.
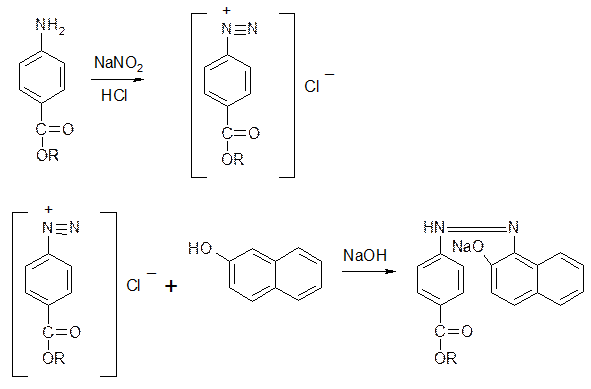
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ: аргентометрически методом Фаянса. Метод основан на способности соляной кислоты (новокаина гидрохлорид) реагировать с серебра нитратом с образованием серебра хлорида.
К 0, 5 мл препарата прибавляют 1 каплю бромфенолового синего, по каплям разведенную уксусную кислоту до зеленовато-желтого окрашивания и титруют 0, 1 моль/л раствором серебра нитрата до фиолетового окрашивания.
HCl + AgNO3 → AgCl↓ + HNO3
f = 1
T = 0, 1*272, 8/1000 = 0, 02728 г/мл
Vтеор. = 0, 01/0, 02728 = 0, 37
 |
Расчет отклонения:
Абс.ошибка: 2, 0 – 1, 96 = 0, 04;
Относит.ошибка: 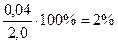 (по П №305 допустимо 5%).
(по П №305 допустимо 5%).
Заключение: Данная лекарственная форма приготовлена удовлетворительно.
Пропись № 2 Rp: Sol. Argentii nitratis 3% -50, 0 мл
D.S: для обработки.
Раствор Серебра нитрата 3% 50 мл
Описание: на анализ поступила бесцветная прозрачная жидкость без механических включений во флаконе из темного стекла.
ОПРЕДЛЕНИЕ ПОДЛИННОСТИ:
На Ag+: Определяют с раствором хлористоводородной кислоты. Для этого к примерно 0, 5 мл исследуемого раствора добавляют 10 капель раствора хлористоводородной кислоты.
 |
AgNO3 + HCL AgCl + HNO3
Выпадает белый творожистый осадок, который легко растворим в разбавленном растворе аммония гидроксида.
 AgCl + 2NH4OH [Ag(NH3)]Cl + 2H2O
AgCl + 2NH4OH [Ag(NH3)]Cl + 2H2O
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ: роданометрический метод, основанный на образовании окрашенного продукта между избытком титранта и индикатором.
К 0, 5 мл исследуемого раствора добавляют 1-3 капли ЖАК титруют 0, 1М раствором аммония роданида до образования красно-бурого окрашивания.
 AgNO3 + NH4NCS AgNCS + NH4NO3
AgNO3 + NH4NCS AgNCS + NH4NO3
 3 NH4NCS + FeNH4(SO4)2 Fe(NCS) 3 + 2NH4SO4
3 NH4NCS + FeNH4(SO4)2 Fe(NCS) 3 + 2NH4SO4
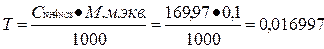
Fэкв=1
Vтеор. = 0, 015/0, 016997 = 0, 88
На титрование ушло 0, 86мл 0, 1М раствора аммония роданита, соответственно содержание исследуемого вещества в граммах равно:
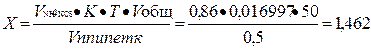
Расчет отклонения:
Абс.ошибка: 1, 5 – 1, 462 = 0, 039;
Относит.ошибка: 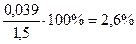
Ошибка не превышает допустимое приказом № 305 отклонение для массы навески свыше 1 до 2 (5%).
Заключение: Данная лекарственная форма приготовлена удовлетворительно.